Содержание
- 2. Положение в Периодической системе
- 3. Строение атома С. О. : +2, +3
- 4. Нахождение в природе. ХАЛЬКОПИРИТ Fe ЧЁРНЫЙ ПИРИТ ПИРИТ ГЕМАТИТ
- 5. Важнейшие железные руды магнитный железняк Fe3O4 красный железняк Fe2O3 бурый железняк Fe2O3 ∙ 3H2O железный колчедан
- 6. Важнейшие соединения железа Соль Мора: FeSO4·(NH4)2SO4·6H2O. Представляет собой парамагнитные, неярко сине-зелёные моноклинные кристаллы. Устойчива на воздухе.
- 7. Роль железа в жизнедеятельности организмов. Ионы Fe необходимы для питания и дыхания растений Повышают яркость зелёной
- 8. Роль железа в жизнедеятельности организмов. Ион Fe3+ - красная окраска листьев, плодов.
- 9. Роль железа в жизнедеятельности организмов.
- 10. Простое вещество
- 11. Физические свойства Твердое Серо-серебристое Блестящее Хорошо проводит тепло и электрический ток Достаточно ковкое и пластичное Обладает
- 12. Свойство металла при повышении температуры приобретать разные кристаллические решетки, а, следовательно, и разные физико-механические свойства, принято
- 14. Химические свойства Металл средней активности
- 15. Химические свойства 3Fe + 2O2 = Fe3O4 2Fe + 3Cl2 = 2FeCl3 Fe + 2HCl =
- 16. Концентрированные азотная и серная кислоты при комнатной температуре пассивируют железо, а при нагревании реакции протекают следующим
- 17. Оксиды железа
- 18. Гидроксиды железа
- 19. ГИДРОКСИД ЖЕЛЕЗА (II) Fe(OH)2. Получают гидроксид железа (II) следующим образом: FeSO4 + 2NaOH → Fe(OH)2↓ +
- 20. Доказательство амфотерности Fe2O3 и Fe(OH)3. Fe2O3 + 3H2SO4 →Fe2(SO4)3 + 3H2O Fe2O3 + 2NaOH + 3H2O
- 21. Качественные реакции на Fe 2+ FeCl2+2NaOH?Fe(OH)2 + 2NaCl зеленый 2. FeCl2 + K3(Fe(CN)6) ? красная кровяная
- 22. Качественные реакции на Fe 3+ FeCl3+3NaOH?Fe(OH)3 + 3NaCl бурый 2. FeCl3 + K4(Fe(CN)6) ? желтая кровяная
- 25. Скачать презентацию






















 Кинетика химических реакций. (Лекция 12)
Кинетика химических реакций. (Лекция 12) Углеводороды. Природный газ. Алканы
Углеводороды. Природный газ. Алканы Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура соединений
Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура соединений Исследование химического состава шоколада и способов его приготовления
Исследование химического состава шоколада и способов его приготовления Природные источники углеводородов
Природные источники углеводородов Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ
Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ Химические свойства карбокатионов
Химические свойства карбокатионов Аттестационная работа. Многогранники: от молекулы до кристалла
Аттестационная работа. Многогранники: от молекулы до кристалла Химия переходных элементов
Химия переходных элементов ОКСИДИ – це бінарні сполуки , що складаються з двох елементів , одним з яких є Оксиген . Загальна формула оксидів : E2On n – вале
ОКСИДИ – це бінарні сполуки , що складаються з двох елементів , одним з яких є Оксиген . Загальна формула оксидів : E2On n – вале Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие
Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров
ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров Презентация по Химии "Азотная кислота" - скачать смотреть
Презентация по Химии "Азотная кислота" - скачать смотреть  Історія виникнення мила Розмаїтого Дмитра, 9-Б клас
Історія виникнення мила Розмаїтого Дмитра, 9-Б клас  Электрохимические методы анализа. Лекция 3
Электрохимические методы анализа. Лекция 3 Тривиальные названия неорганических соединений
Тривиальные названия неорганических соединений Структура аминокислот
Структура аминокислот Дифференцированный подход в обучении химии
Дифференцированный подход в обучении химии Физико-химические методы анализа
Физико-химические методы анализа Кинетические методы анализа
Кинетические методы анализа Полипропилен. Молекулалық құрылымы
Полипропилен. Молекулалық құрылымы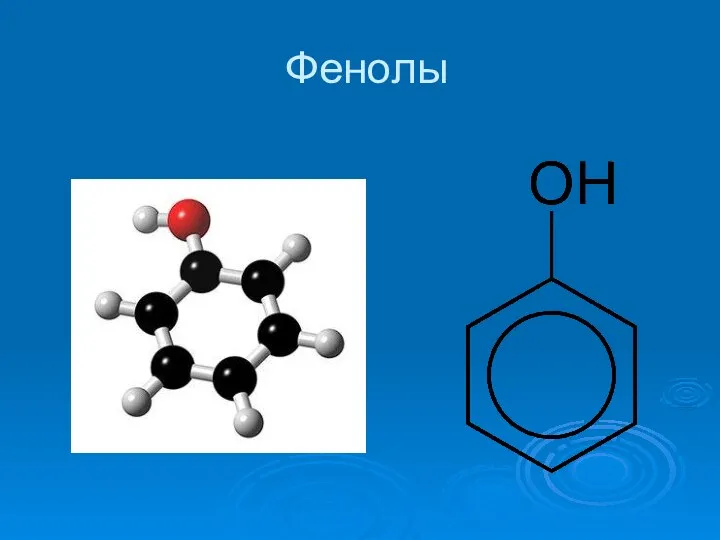 Фенолы. Физические свойства. Получение
Фенолы. Физические свойства. Получение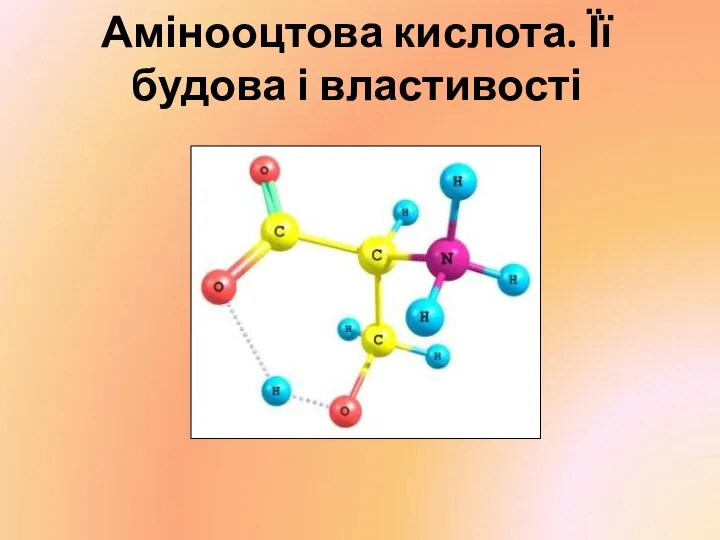 Амінооцтова кислота. Її будова і властивості
Амінооцтова кислота. Її будова і властивості Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері
Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері Пища, с точки зрения химика
Пища, с точки зрения химика Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией
Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией  Классификация минералов по химическому принципу
Классификация минералов по химическому принципу