Содержание
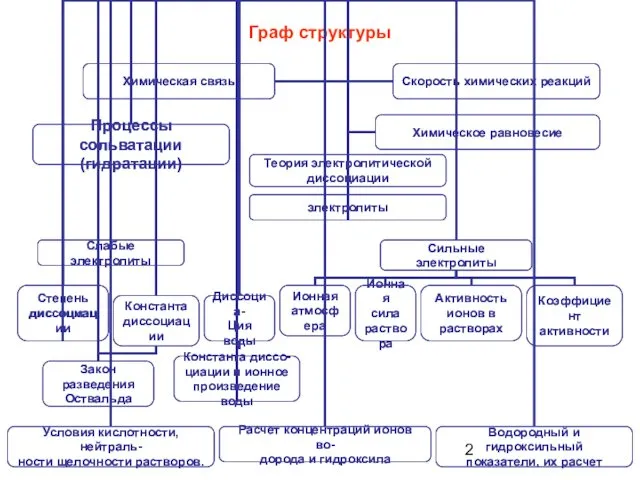
- 2. Граф структуры
- 3. Растворы - гомогенные термодинамически устойчивые системы, состоящие из двух и большего числа компонентов, состав которых изменяться
- 4. Раствор может иметь любое агрегатное состояние: жидкое газообразное (газовая смесь). твердое
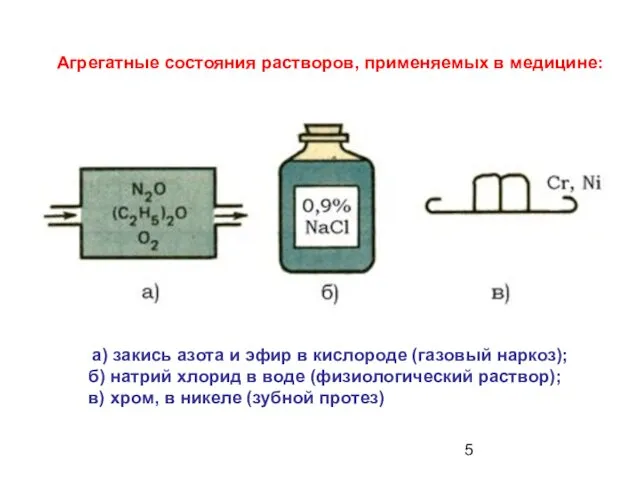
- 5. Агрегатные состояния растворов, применяемых в медицине: а) закись азота и эфир в кислороде (газовый наркоз); б)
- 6. Характеризуются гомогенностью состава и отсутствием поверхности раздела между растворенным веществом и растворителем. Размер растворенных частиц (ионов
- 7. 2. По наличию или отсутствию электролитической диссоциации Растворы электролитов — в которых вещества диссоциируют на ионы
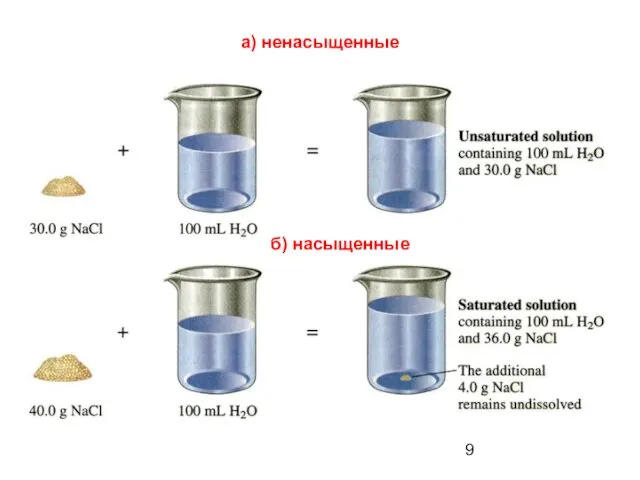
- 8. а) Ненасыщенный - раствор, в котором еще можно растворить добавочное количество данного вещества. б) Насыщенный -
- 9. б) насыщенные а) ненасыщенные
- 10. в) пересыщенные – содержащие значительно больше растворенного вещества чем его требуется для насыщения при данной температуре
- 11. Растворимость Растворимость – способность вещества растворяться в том или ином растворителе. Мерой растворимости вещества при данных
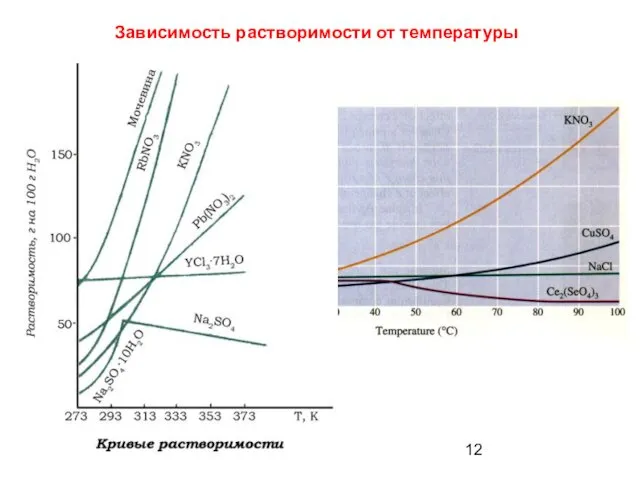
- 12. Зависимость растворимости от температуры
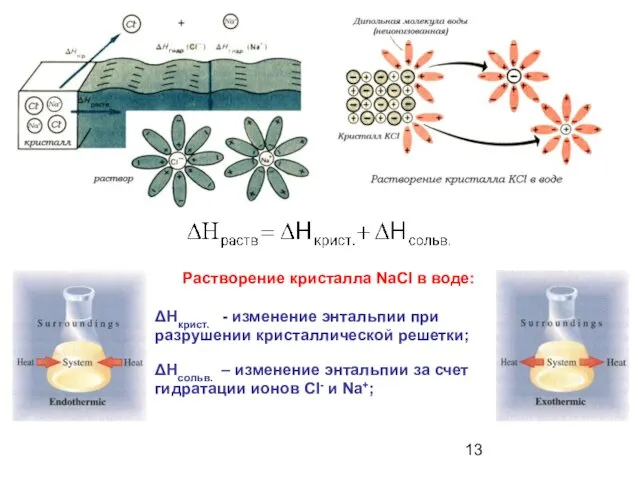
- 13. Растворение кристалла NaCl в воде: ΔНкрист. - изменение энтальпии при разрушении кристаллической решетки; ΔНсольв. – изменение
- 14. Процентная – масса вещества в 100 г раствора Процентная концентрация выражается числом, граммов растворенного вещества, содержащимся
- 15. «% - сотая часть » 2 мл 3% раствора – 60 мг 7 мл 4% раствора
- 16. 2. Молярная концентрация – число моль вещества в 1 л раствора Задача: Рассчитать молярность 0.9% раствора
- 17. 3. Нормальная концентрация – число моль-экв вещества в 1 л раствора
- 18. Фактор эквивалентности – fэкв(Х) – число, обозначающее, какая доля реальной частицы вещества Х эквивалентна одному иону
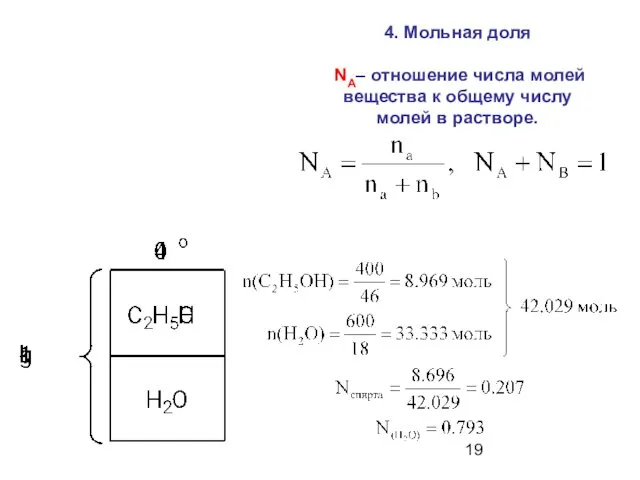
- 19. 4. Мольная доля NA– отношение числа молей вещества к общему числу молей в растворе.
- 20. 5. Моляльность m - число моль вещества в 1000 г растворителя (не зависит от температуры, поэтому
- 21. 6. Титр раствора Т – число грамм вещества в 1 мл раствора (г/мл). См = 1000
- 22. Осмолярная концентрация - суммарное молярное количество всех кинетически активных частиц, содержащихся в 1 литре раствора, независимо
- 23. Растворы электролитов Электролиты – вещества, растворы и расплавы которых проводят электрический ток вследствие диссоциации на ионы.
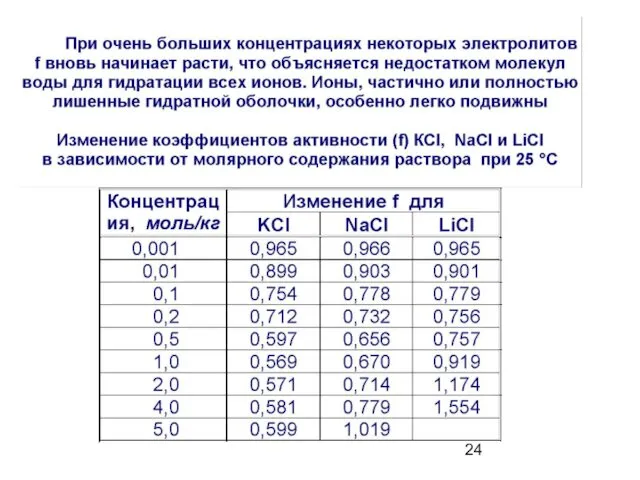
- 25. Ионная сила растворов Ионная сила растворов - величина, измеряемая полусуммой произведений концентраций всех находящихся в растворе
- 26. Уравнение Дебая-Хюккеля Дебай Петер (24.III.1884–2.XI.1966) Йозеф Хюккель (9.09.1896— 16.021980)
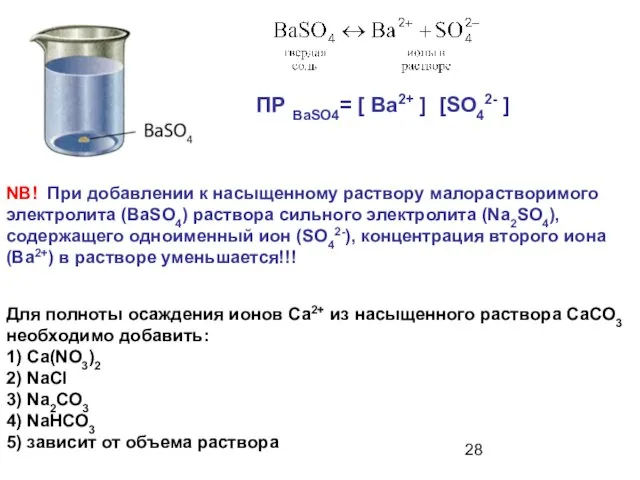
- 27. NB! При добавлении к насыщенному раствору малорастворимого электролита раствора сильного электролита, не имеющего с ним общих
- 28. NB! При добавлении к насыщенному раствору малорастворимого электролита (BaSO4) раствора сильного электролита (Na2SO4), содержащего одноименный ион
- 29. 2. Слабые электролиты диссоциируют обратимо, ступенчато. α – степень диссоциации Кд – константа диссоциации Степень диссоциации
- 30. Закон разбавления Оствальда Нобелевская премия (1909г) « в знак признания работ по катализу, а также за
- 31. При α Вывод закона разведения Оствальда
- 32. 2. Степень диссоциации кислоты HX равна 0,25. Какое суммарное число ионов H+ и X- приходится в
- 33. Задача: Рассчитать концентрацию ионов водорода [Н+] в 9% растворе уксуса (пл.=1), Кд=1.75∙10-5.
- 34. Задача: Рассчитать концентрацию ионов водорода [Н+] в 9% растворе уксуса (пл.=1) Ответ: [Н+]=5.12∙10-3 моль-экв/л
- 36. Скачать презентацию























![Задача: Рассчитать концентрацию ионов водорода [Н+] в 9% растворе уксуса (пл.=1), Кд=1.75∙10-5.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/475082/slide-32.jpg)
![Задача: Рассчитать концентрацию ионов водорода [Н+] в 9% растворе уксуса (пл.=1) Ответ: [Н+]=5.12∙10-3 моль-экв/л](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/475082/slide-33.jpg)
 Балалардың тыныс алу жүйесінің ауруларын емдеу, денсаулығын нығайту алдын алу
Балалардың тыныс алу жүйесінің ауруларын емдеу, денсаулығын нығайту алдын алу Кардиологиялық аурулардың дәрігерлік- еңбектік сараптамасы(ЖИА)
Кардиологиялық аурулардың дәрігерлік- еңбектік сараптамасы(ЖИА) Клиническая анатомия зубов верхней челюсти
Клиническая анатомия зубов верхней челюсти Implant
Implant Злокачественные опухоли челюстно-лицевой области у детей. Клиника, диагностика и лечение. Реабилитация больных после удаления
Злокачественные опухоли челюстно-лицевой области у детей. Клиника, диагностика и лечение. Реабилитация больных после удаления Физиология тромбоцитов. Свертывание и переливание крови
Физиология тромбоцитов. Свертывание и переливание крови Эпштейна-Барр-вирусная инфекция
Эпштейна-Барр-вирусная инфекция Диуретиктер
Диуретиктер Заболевания гортани
Заболевания гортани СРС: Хроническая болезнь почек
СРС: Хроническая болезнь почек Банкеттерге қызмет көрсету ерекшеліктері
Банкеттерге қызмет көрсету ерекшеліктері Влияние Интернета на детей. Интернет-зависимость
Влияние Интернета на детей. Интернет-зависимость Острые заболевания нижних дыхательных путей: пневмонии и бронхиты
Острые заболевания нижних дыхательных путей: пневмонии и бронхиты Нанотехнологии в медицине
Нанотехнологии в медицине Как найти боль клиента
Как найти боль клиента ОВТВ цитотоксического действия
ОВТВ цитотоксического действия Хроническое заболевание головного мозга эпилепсия. Классификация эпилептических припадков
Хроническое заболевание головного мозга эпилепсия. Классификация эпилептических припадков Принципы диагностики вирусных болезней
Принципы диагностики вирусных болезней Артериальная и венозная гиперемия. Ишемия, стаз
Артериальная и венозная гиперемия. Ишемия, стаз Бронхиальная астма
Бронхиальная астма Ревматоїдний артрит
Ревматоїдний артрит Психология влияния
Психология влияния Тромбоэмболия легочной артерии. Современные подходы к диагностике и лечению
Тромбоэмболия легочной артерии. Современные подходы к диагностике и лечению BIS Биспектральный индекс
BIS Биспектральный индекс Эффективность и переносимость блокатора рецепторов к альдостерону- эплеренона у больных с острым инфарктом миокарда
Эффективность и переносимость блокатора рецепторов к альдостерону- эплеренона у больных с острым инфарктом миокарда Пневмококковая инфекция
Пневмококковая инфекция Vitamin D
Vitamin D Средства, активирующие ЦНС
Средства, активирующие ЦНС