Содержание
- 2. Підприємство ТОВ “БІОФАРМА ПЛАЗМА ” розпочало свою діяльність з 1896 року. Його перша назва - “Бактеріологічний
- 3. Сьогодні ТОВ «БІОФАРМА ПЛАЗМА» - провідний виробник лікарських засобів з плазми: Альбумін-Біофарма, розчин для інфузій 10%
- 4. ІМУНОГЛОБУЛІН АНТИСТАФІЛОКОКОВИЙ ЛЮДИНИ, Immunoglobulinum antistaphylococcum humanum, розчин для ін’єкцій; ІМУНОГЛОБУЛІН АНТИЦИТОМЕГАЛОВІРУСНИЙ ЛЮДИНИ, Immunoglobulinum anticytomegalovirusum humanum, розчин
- 5. Географія присутності Продукція експортується в країни СНГ (крім РФ), В'єтнам, Монголію
- 6. Якість підтверджуються сертифікатами Федерального інституту вакцин та біопрепаратів ім.Пауля Ерліха, м.Лонген, Німеччина
- 7. ТОВ «БІОФАРМА ПЛАЗМА» сертифіковано на відповідність вимогам GMP
- 8. ТОВ «БІОФАРМА ПЛАЗМА» сертифіковано на відповідність вимогам міжнародного стандарту ISO 9001
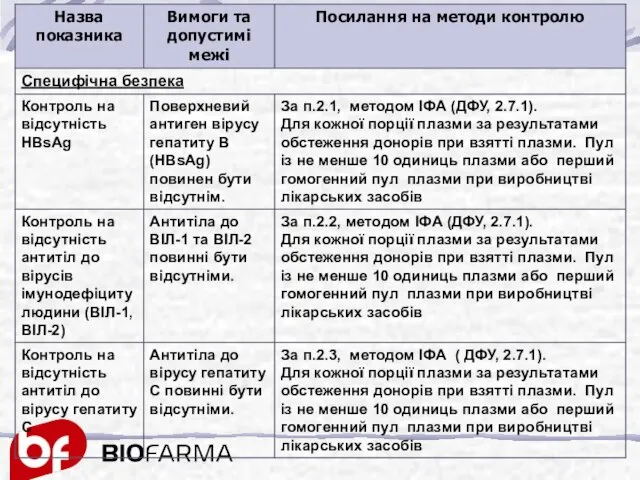
- 9. СПЕЦИФІКАЦІЯ вхідного контролю Плазма людини для фракціонування Основний внутрішній документ відділу контролю якості, який детально регламентує
- 10. Вимоги до якості
- 17. Для гарантування відповідності вимогам НАЛЕЖНОЇ ВИРОБНИЧОЇ ПРАКТИКИ (GMP) ТОВ «БІОФАРМА ПЛАЗМА» укладає Договір на поставку основної
- 18. Плазма для фракціонування поділяється на категорії: -свіжозаморожена плазма (СЗП), що використовується для виділення лабільних білків плазми
- 19. -специфічна плазма - свіжозаморожена або заморожена плазма донорів-реконвалесцентів або гіперімунізованих донорів, яка містить специфічні антитіла у
- 20. Осади білкових фракцій плазми повинні отримуватись методом фракціонування спирто-водними осаджувачами при температурі нижче 0оС. З метою
- 21. п. 3. Якість продукції, що постачається п. 3.1. Постачання плазми донорської крові (плазми для фракціонування), осадів
- 22. Інструкції з фракціонування консервованої крові на її компоненти (плазма, еритроцити, тромбоцити, лейкоцити) та їх консервування, затвердженої
- 23. п. 3.2. Кожна поставка сировини повинна супроводжуватися наступною документацією: Сертифікатом якості на всю поставку, який повинен
- 24. терміни карантинізації; об’єм поставки; підтвердження тестів на відсутність збудників інфекцій, які переносяться при гемотрансфузіях; кількість білка;
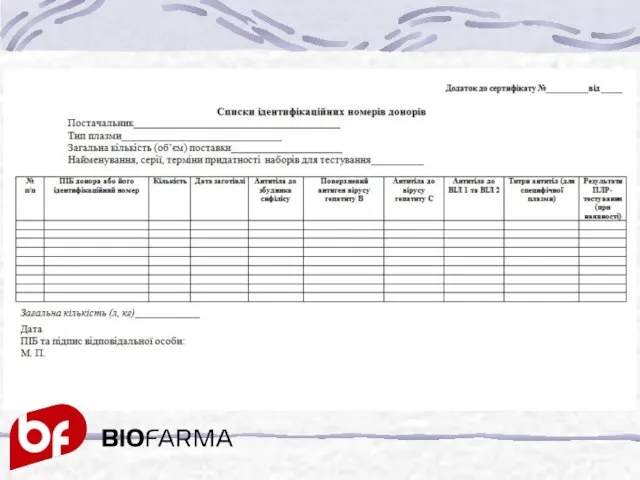
- 26. Списком ідентифікаційних номерів донорів, який є додатком до кожного сертифікату якості на плазму та еритроцитарну масу,
- 28. Паспортом на осади II+III та IVфракції, який повинен містити дати та номера завантажень та вагу осадів.
- 29. п. 3.3. Сертифікат якості та список ідентифікаційних номерів донорів мають бути підписаними головним лікарем Продавця або
- 30. п. 4. Оформлення документів та поставка сировини п. 4.3. Сировина поставляється в промаркованій тарі (ящику), яка
- 31. Невідповідності, які найчастіше зустрічаються при поставках плазми 1.Неналежне оформлення сертифікатів якості: - недотримання встановленого контрактом зразку
- 32. 2. Неналежне оформлення списків ідентифікаційних номерів донорів: - список донорів «не прив’язаний» до сертифікату (повинен бути
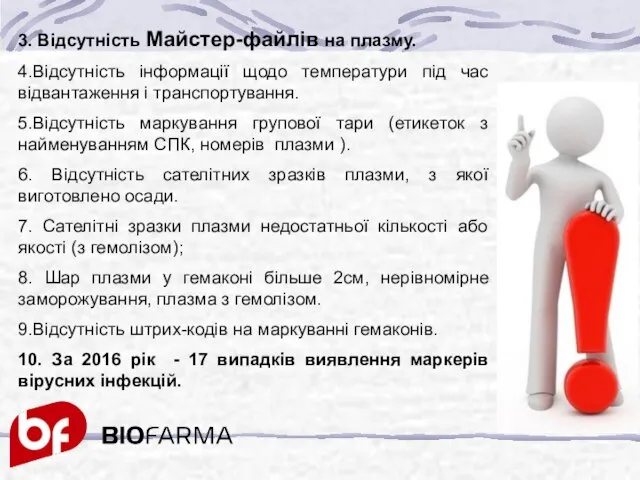
- 33. 3. Відсутність Майстер-файлів на плазму. 4.Відсутність інформації щодо температури під час відвантаження і транспортування. 5.Відсутність маркування
- 34. 11.Невідповідність вимог на СПК до кількості специфічних антитіл проти D-антигену еритроцитів в ізоімунній плазмі (низькі титри)
- 36. ПОРЯДОК проведення експертизи реєстраційних матеріалів на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію), а також
- 37. Спеціальні вимоги до матеріалів реєстраційного досьє для біологічних лікарських засобів 8.1. Лікарські засоби, отримані з крові
- 38. Додатково до матеріалів реєстраційного досьє може надаватись: Мастер-файл на плазму, що є окремим документом, який не
- 39. якщо заявник не є власником Мастер-файла на плазму, то власник повинен надати свій Мастер-файл заявнику для
- 40. 8.1.1. У Мастер-файлі на плазму повинна міститися інформація про плазму, що використовувалася як вихідний матеріал/ сировина,
- 41. б) про якість та безпеку плазми: відповідність монографії Європейської фармакопеї або у разі її відсутності іншій
- 42. 8.1.2. У Мастер-файлі на плазму повинна міститися інформація про прийняту систему взаємодії між виробником одержаного з
- 43. Настанова СТ-Н МОЗ України 42-4.0:2016 «Лікарські засоби. Належна виробнича практика» Терміни та визначення понять: Основне досьє
- 44. Відповідальна особа (Responsible Person) В установах із взяття/випробування крові має бути призначена особа (відповідальна особа), яка
- 45. Відповідальна особа має відповідати таким мінімальним умовам щодо кваліфікації: а) він/вона повинні мати диплом, сертифікат чи
- 46. d) установи із взяття/випробування крові мають повідомляти компетентному органу про ім'я відповідальної особи, а також інших
- 47. Додаток GMP 14 (обов'язковий!) ВИРОБНИЦТВО ЛІКАРСЬКИХ ПРЕПАРАТІВ, ОДЕРЖУВАНИХ З ДОНОРСЬКОЇ КРОВІ АБО ПЛАЗМИ 1. Загальні положення
- 48. 2. Принципи 2.1 Лікарські засоби, одержувані з донорської крові або плазми (а також їх діючі речовини,
- 49. 2.2 Взагалі, діючі речовини, використовувані як вихідна сировина для лікарських препаратів, мають відповідати принципам та правилам
- 50. 2.5 Чинні вимоги поширюються на всі стадії після взяття та випробування крові (наприклад, обробка (включаючи розділення),
- 51. 2.6 Спеціальні вимоги щодо документації та інші заходи стосовно вихідної сировини для лікарських препаратів, одержуваних з
- 52. 3. Управління якістю 3.1 Управління якістю має охоплювати всі стадії від відбору донорів до постачання готової
- 53. 3.5 Підприємство з фракціонування/виробник готової продукції має укласти письмові контракти з установами із взяття/випробування крові, що
- 54. У підприємства з фракціонування/виробника лікарського препарату мають бути в наявності результати випробувань усіх одиниць, поставлених установою
- 55. 4. Простежуваність та заходи після взяття крові 4.1 Має бути система, що дає можливість простеження від
- 56. 4.4 У контрактах (зазначених у п. 3.5 цього додатка) між установами із взяття/випробування крові (у тому
- 57. 6. Виробництво Вихідна сировина 6.1 Вихідна сировина має відповідати вимогам всіх відповідних монографій Європейської Фармакопеї та
- 58. Сертифікація/видача дозволу на випуск плазми для фракціонування, використовуваної як вихідна сировина 6.7 Дозвіл на випуск плазми
- 59. 7. Контроль якості 7.1 Вимоги до випробування щодо вірусів або інших інфікуючих агентів слід встановлювати з
- 60. ТОВ «БІОФАРМА ПЛАЗМА» найближчого майбутнього
- 61. Керівник служби якості ТОВ «Біофарма Плазма» - Куркіна Оксана Вікторівна +38 067 236 74 07 Інженер
- 63. Скачать презентацию























































 QALY (quality-adjusted life years) - количество приобретенных в результате медицинского вмешательства лет качественной жизни
QALY (quality-adjusted life years) - количество приобретенных в результате медицинского вмешательства лет качественной жизни Дія алкоголю
Дія алкоголю Верхняя челюсть Maxilla
Верхняя челюсть Maxilla Снотворные, противосудорожные (противоэпилептические, противопаркинсонические), обезболивающие ЛС
Снотворные, противосудорожные (противоэпилептические, противопаркинсонические), обезболивающие ЛС Профилактика и лечение венозных тромбозов
Профилактика и лечение венозных тромбозов Нарушения внешнего дыхания
Нарушения внешнего дыхания Дети поколения Z и поколения Альфа
Дети поколения Z и поколения Альфа Дискогенные заболевания позвоночника собак. Распространенность дископатий среди плотоядных животных
Дискогенные заболевания позвоночника собак. Распространенность дископатий среди плотоядных животных Молекулярная онкология
Молекулярная онкология Участие медицинской сестры в реабилитационных мероприятиях у пациентов с артрозами
Участие медицинской сестры в реабилитационных мероприятиях у пациентов с артрозами Механизмы действия антибиотиков
Механизмы действия антибиотиков Анестезия при заболеваниях эндокринной системы
Анестезия при заболеваниях эндокринной системы Интерпретация лабораторных маркеров некроза миокарда, острофазовых показателей при заболеваниях миокарда и эндокарда
Интерпретация лабораторных маркеров некроза миокарда, острофазовых показателей при заболеваниях миокарда и эндокарда Острый живот в гинекологии
Острый живот в гинекологии Этилметилгидроксипиридина сукцинат
Этилметилгидроксипиридина сукцинат topuz2
topuz2 Анаэробная инфекция и столбняк
Анаэробная инфекция и столбняк Случаи применения биологического оружия в истории человечества
Случаи применения биологического оружия в истории человечества Препараты, используемые в кардиологии
Препараты, используемые в кардиологии Спаечная болезнь
Спаечная болезнь Тазалық-денсаулық кепілі
Тазалық-денсаулық кепілі Алгоритм работы при отработке заболевших Сovid-19
Алгоритм работы при отработке заболевших Сovid-19 Хронический гнойный эпитимпанит
Хронический гнойный эпитимпанит Симптомы болезни - боли в животе у ребенка (терапевтические)
Симптомы болезни - боли в животе у ребенка (терапевтические) Симптомы и синдромы пневмонии
Симптомы и синдромы пневмонии Топырақ тыңайтушы препараттарды шығару
Топырақ тыңайтушы препараттарды шығару Сколько весит портфель первоклассника?
Сколько весит портфель первоклассника? Представления молодежи г. Красноярска об идеальном брачном партнере
Представления молодежи г. Красноярска об идеальном брачном партнере