Содержание
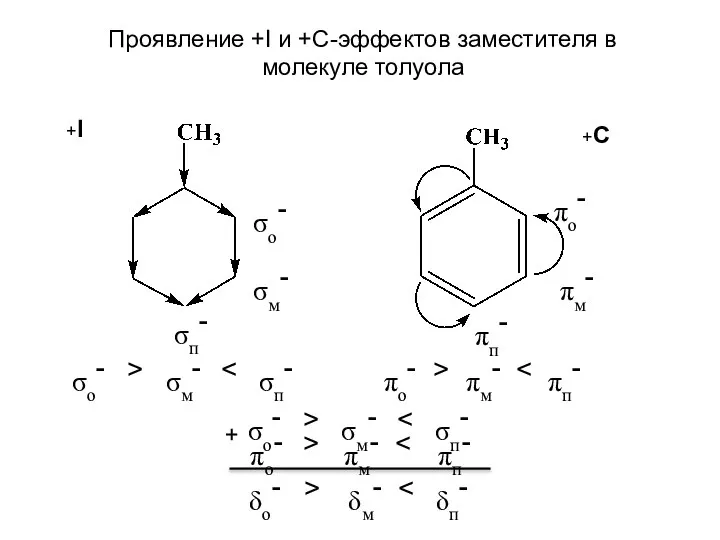
- 2. σo- σм- σп- > σo- σм- σп- πo- πo- πм- πм- πп- πп- > σo- σм-
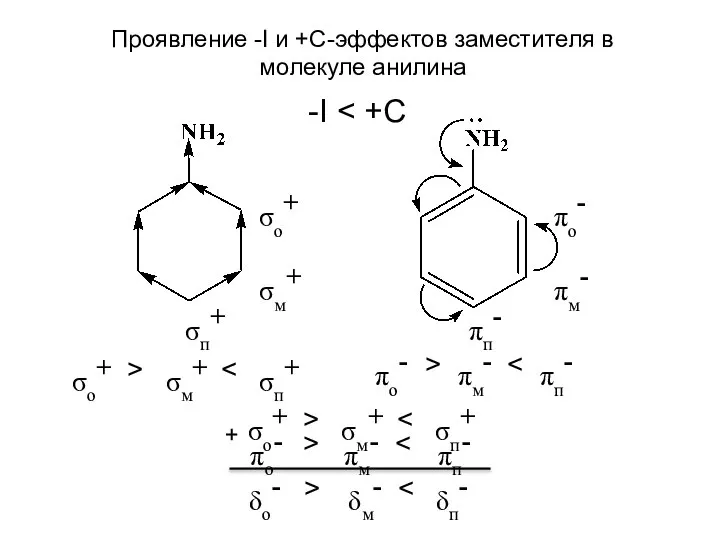
- 3. При проявлении заместителем двух эффектов противоположного знака учитывается их относительная величина. В анилине аминогруппа проявляет –I
- 4. σo+ σм+ σп+ > πo- πм- πп- > σo+ σм+ σп+ πo- πм- πп- σo+ σм+
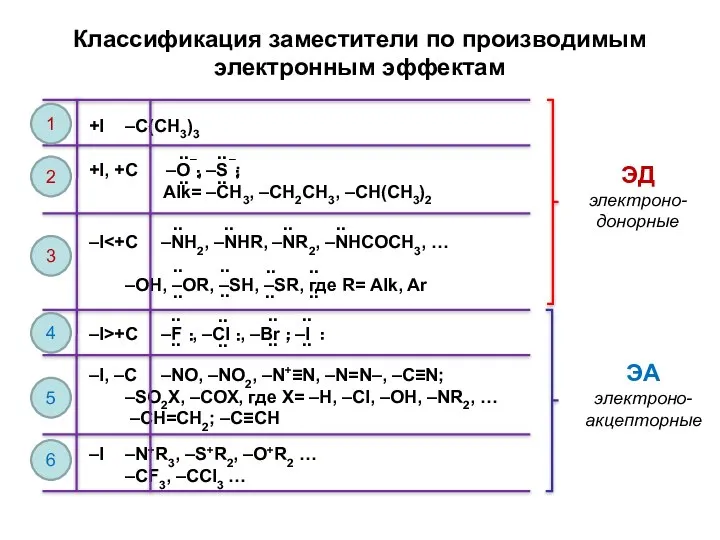
- 5. Классификация заместители по производимым электронным эффектам +I –C(CH3)3 +I, +C –O¯, –S¯; Alk= –CH3, –CH2CH3, –CH(CH3)2
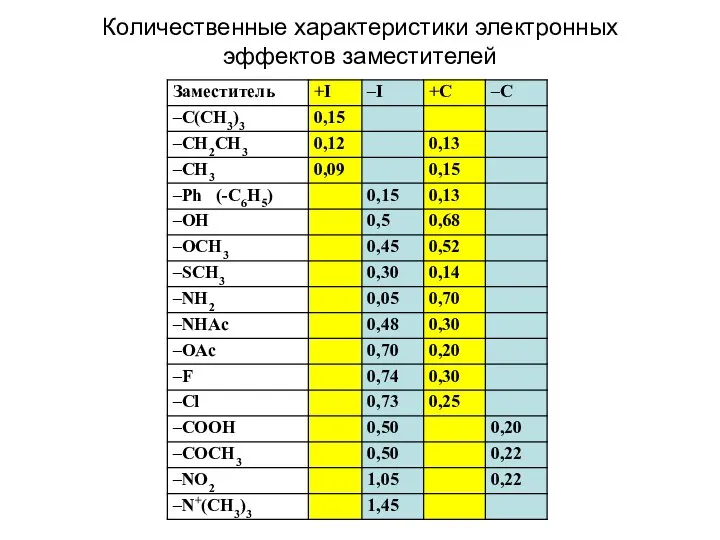
- 6. Количественные характеристики электронных эффектов заместителей
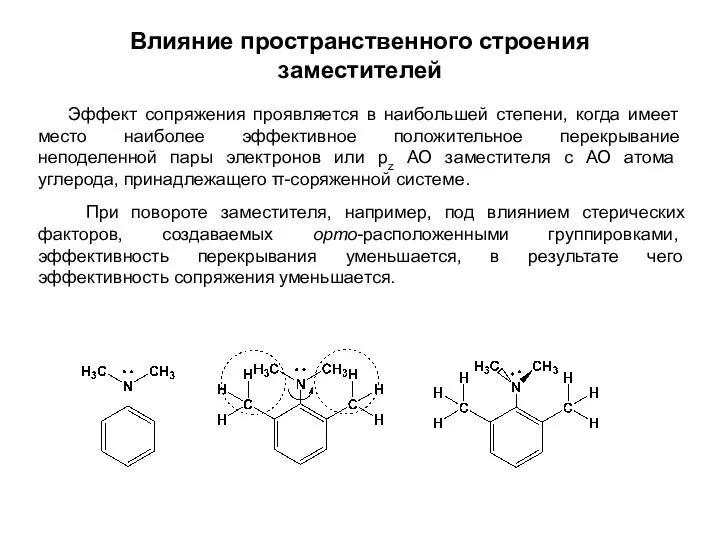
- 7. Влияние пространственного строения заместителей Эффект сопряжения проявляется в наибольшей степени, когда имеет место наиболее эффективное положительное
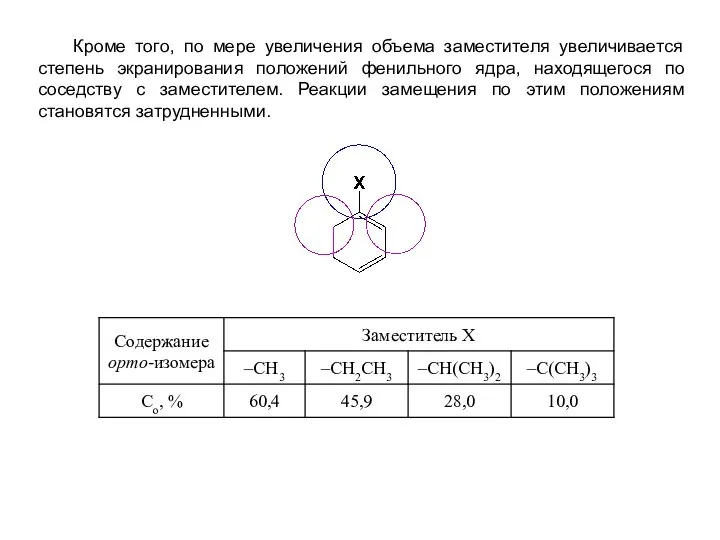
- 8. Кроме того, по мере увеличения объема заместителя увеличивается степень экранирования положений фенильного ядра, находящегося по соседству
- 9. Количественная оценка влияния заместителей В 1930 г Гамметом установлено, что для серии однотипных реакций: т.е. реакций,
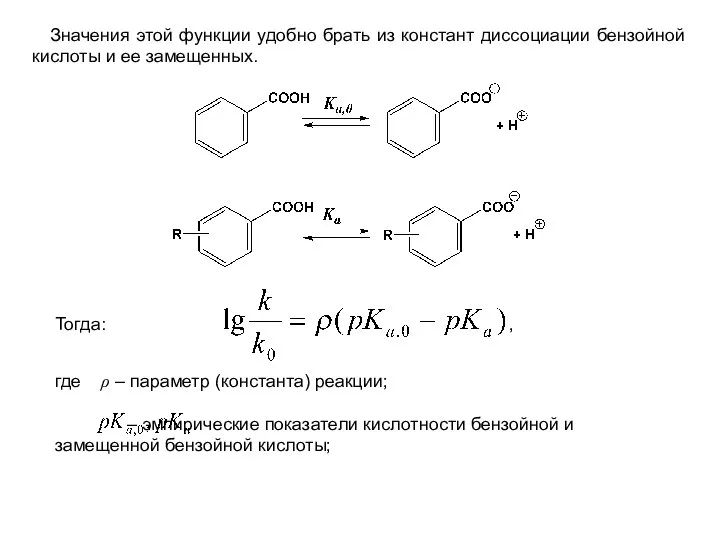
- 10. Значения этой функции удобно брать из констант диссоциации бензойной кислоты и ее замещенных. Тогда: где ρ
- 11. Обозначив - константа Гаммета, приведем последнее выражение к виду: Принимая во внимание, что электронное влияние заместителя
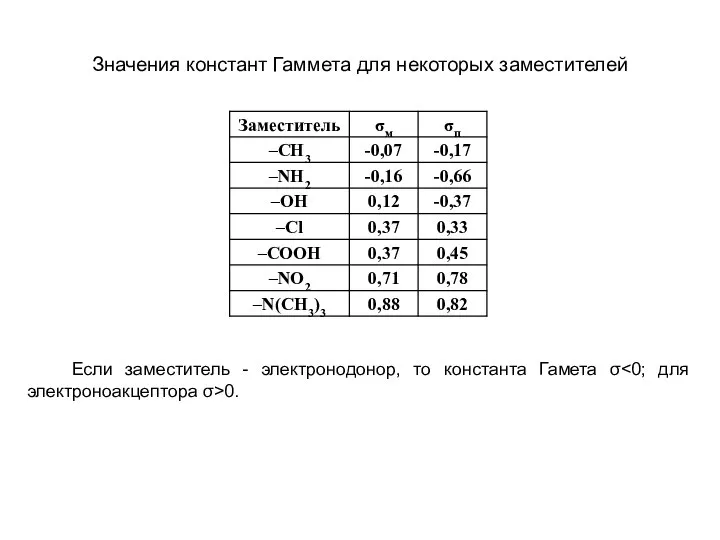
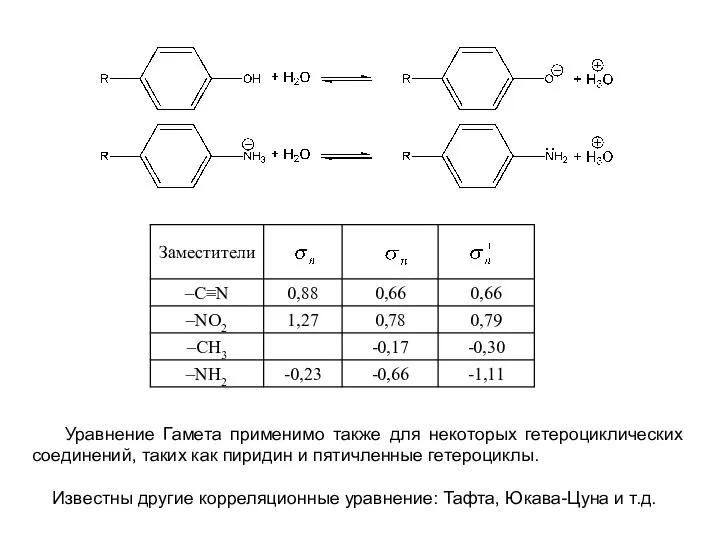
- 12. Значения констант Гаммета для некоторых заместителей Если заместитель - электронодонор, то константа Гамета σ 0.
- 13. Параметр реакции (ρ) характеризует чувствительность реакции к изменению электронных эффектов заместителя в конкретных условиях, зависит от
- 14. Абсолютное значение параметра реакции зависит от расстояния, от проводимости электронных эффектов, от активности реагента и условий
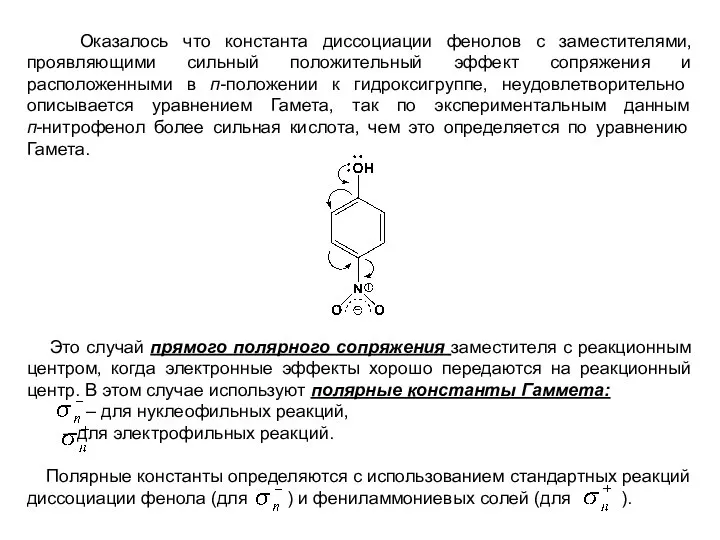
- 15. Оказалось что константа диссоциации фенолов с заместителями, проявляющими сильный положительный эффект сопряжения и расположенными в п-положении
- 16. Уравнение Гамета применимо также для некоторых гетероциклических соединений, таких как пиридин и пятичленные гетероциклы. Известны другие
- 17. Кислотно-основные свойства органических соединений В настоящее время для определения кислотности наиболее широко применяется 2 определения кислоты
- 18. Йоханнес-Николаус Брёнстед (Дания) (22.02.1879 — 17.12.1947). Автор протонной теории кислот и оснований, развивал теорию кислотно-основного катализа.
- 19. По Бренстеду кислоты – вещества, молекулы которых способны отдавать протон, а основания – соединения, способные принимать
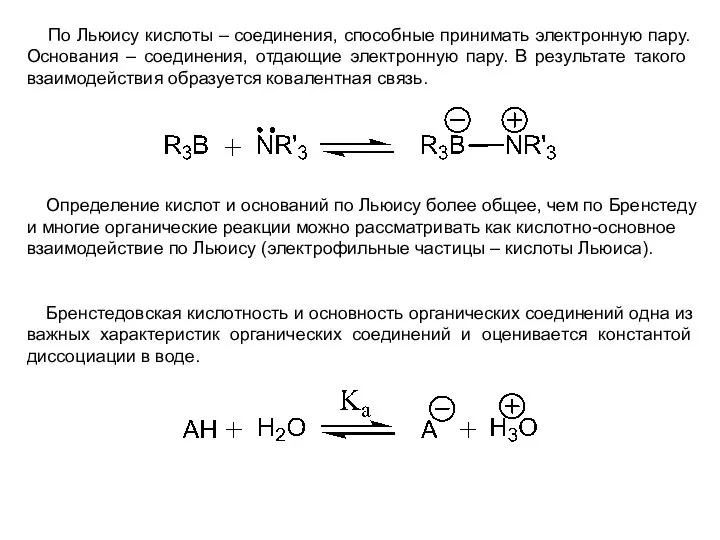
- 20. По Льюису кислоты – соединения, способные принимать электронную пару. Основания – соединения, отдающие электронную пару. В
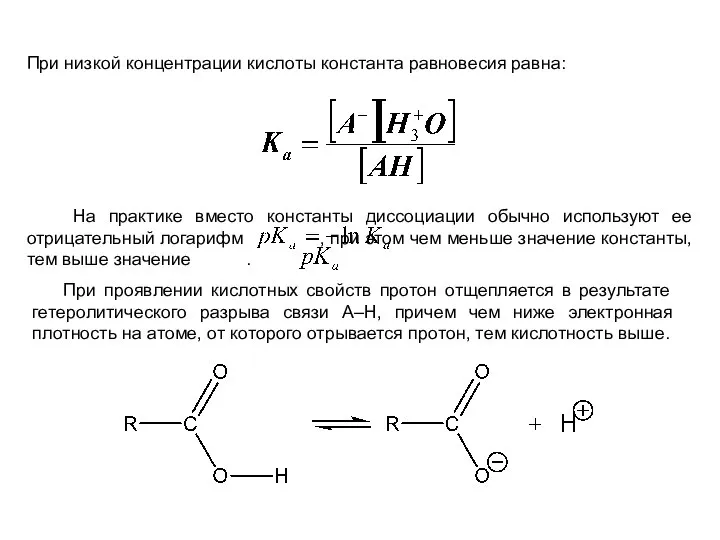
- 21. При низкой концентрации кислоты константа равновесия равна: На практике вместо константы диссоциации обычно используют ее отрицательный
- 22. С другой стороны, чем выше устойчивость образующегося аниона, тем выше кислотность. При этом устойчивость аниона зависит
- 23. ВН+ + Н2О ↔ В: + Н+3О С целью построения непрерывной шкалы кислотности и основаности силу
- 24. До настоящего времени не существует специальной шкалы кислотности по Льюису. Относительная кислотность определяется с использованием различных
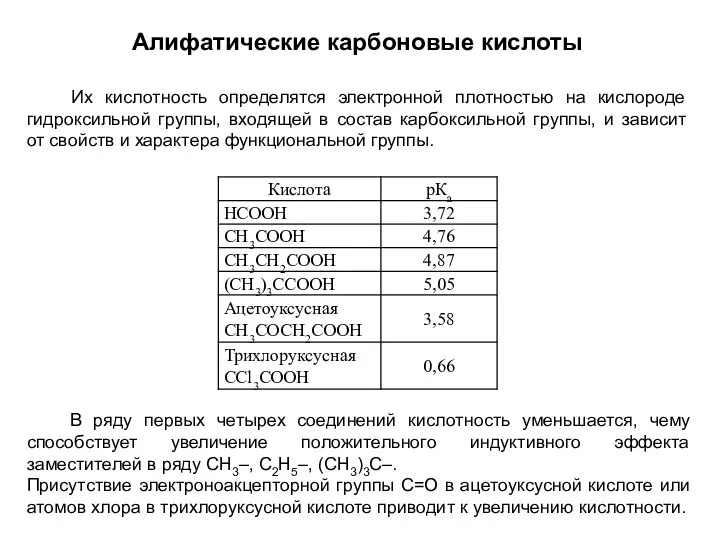
- 25. Алифатические карбоновые кислоты Их кислотность определятся электронной плотностью на кислороде гидроксильной группы, входящей в состав карбоксильной
- 26. Ароматические карбоновые кислоты Бензойная кислота – более слабая кислота, чем муравьиная, т.к. фенильное ядро – электронодонор
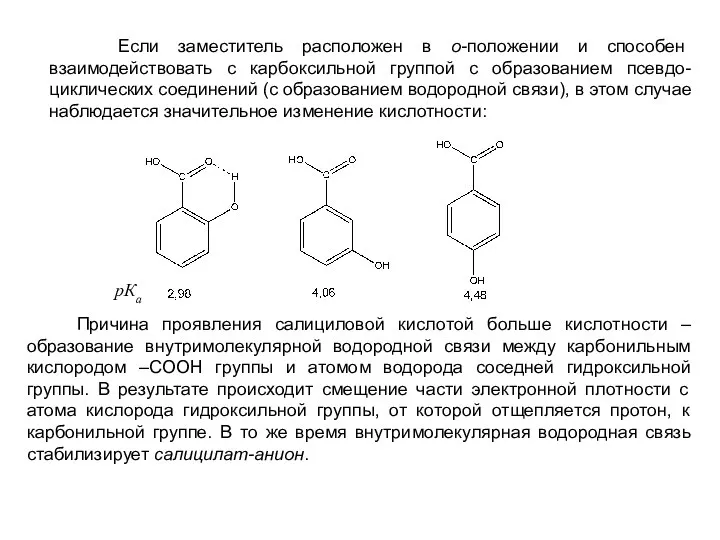
- 27. Если заместитель расположен в о-положении и способен взаимодействовать с карбоксильной группой с образованием псевдо-циклических соединений (с
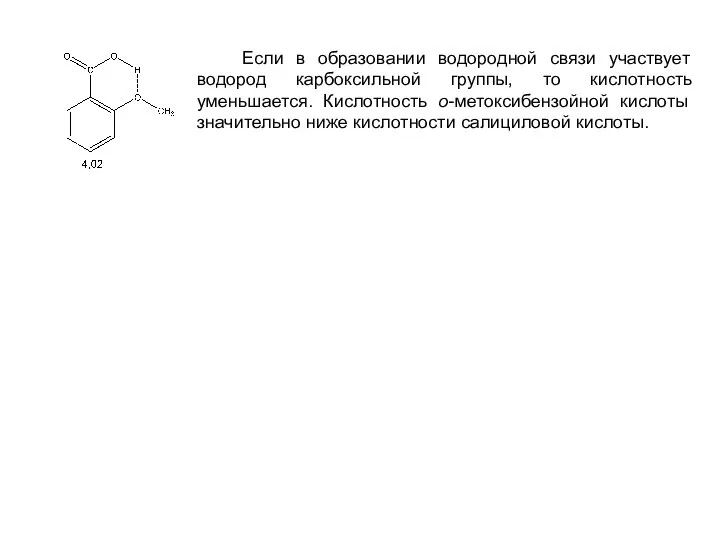
- 28. Если в образовании водородной связи участвует водород карбоксильной группы, то кислотность уменьшается. Кислотность о-метоксибензойной кислоты значительно
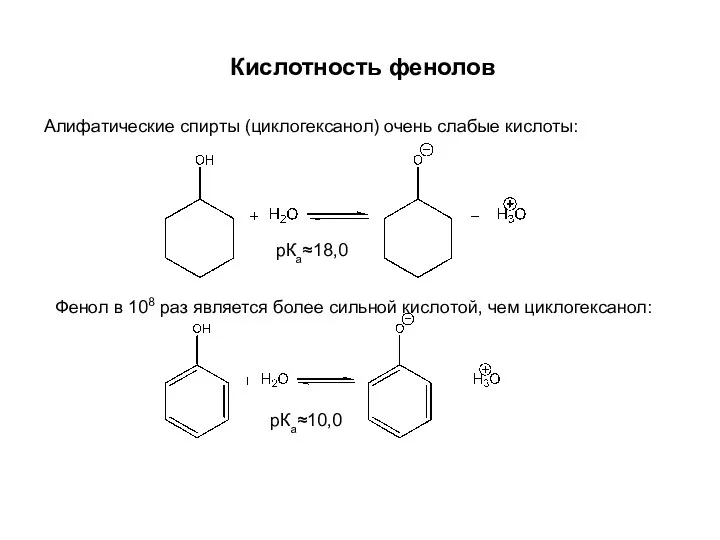
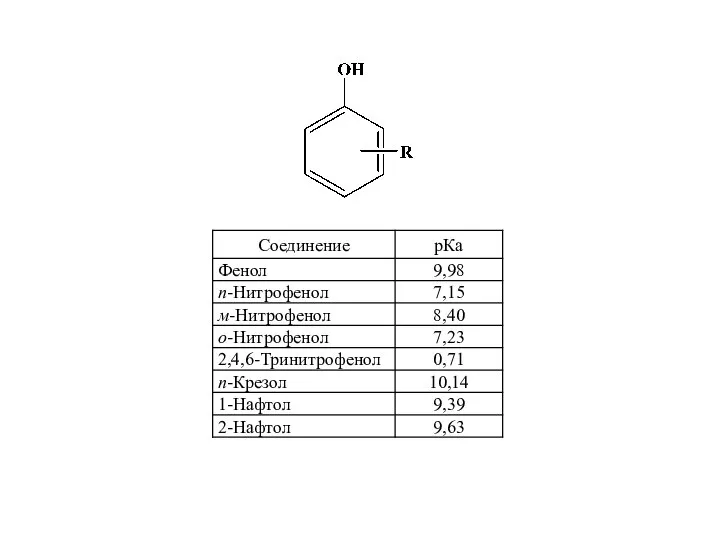
- 29. Кислотность фенолов Алифатические спирты (циклогексанол) очень слабые кислоты: рКа≈18,0 Фенол в 108 раз является более сильной
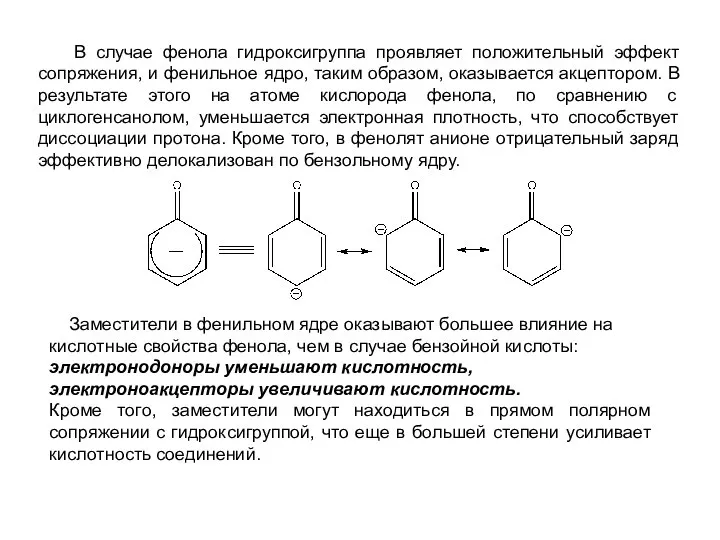
- 30. В случае фенола гидроксигруппа проявляет положительный эффект сопряжения, и фенильное ядро, таким образом, оказывается акцептором. В
- 32. Основность органических соединений Основные свойства органических соединений связаны с наличием атома, несущего свободную пару электронов, по
- 33. При переходе от первичных алифатических аминов к вторичным происходит увеличение основности, т.к. алкильные группы проявляют положительный
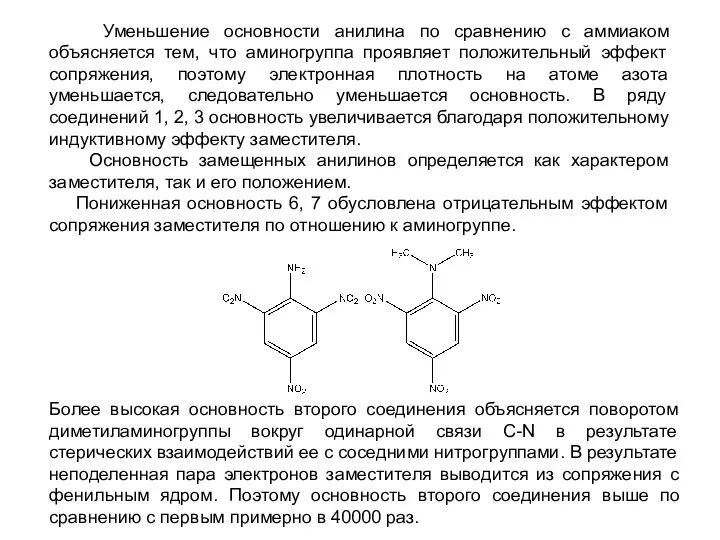
- 34. Уменьшение основности анилина по сравнению с аммиаком объясняется тем, что аминогруппа проявляет положительный эффект сопряжения, поэтому
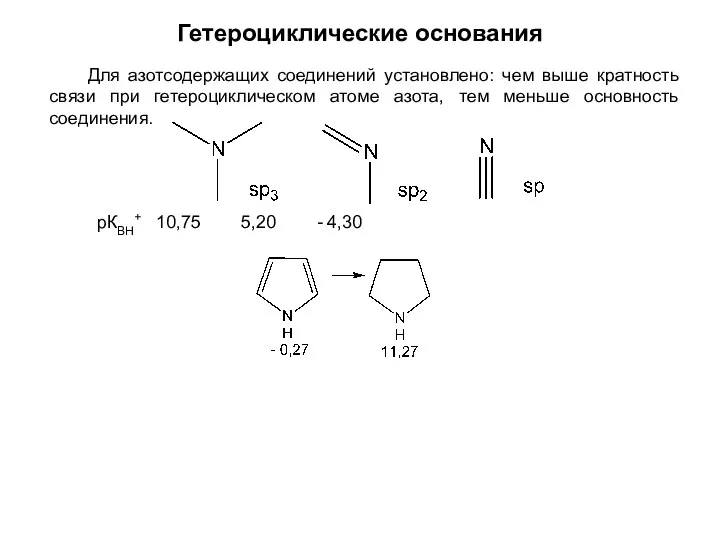
- 35. Гетероциклические основания Для азотсодержащих соединений установлено: чем выше кратность связи при гетероциклическом атоме азота, тем меньше
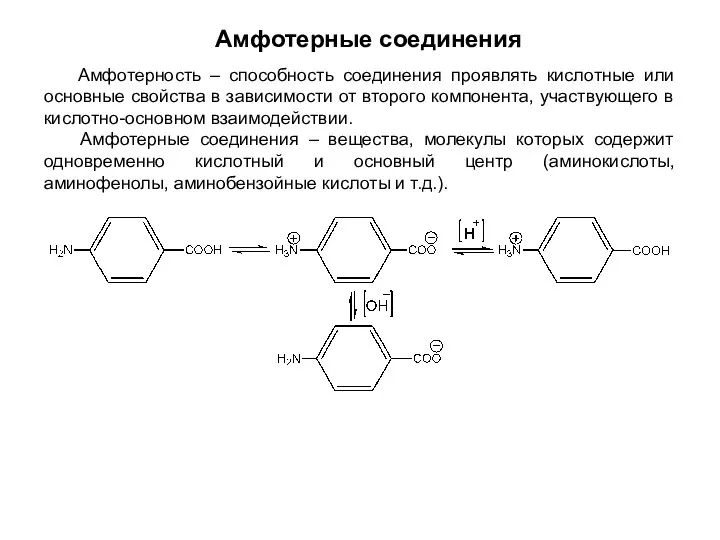
- 36. Амфотерные соединения Амфотерность – способность соединения проявлять кислотные или основные свойства в зависимости от второго компонента,
- 38. Скачать презентацию














 Архитектура Владимиро-Суздальского княжества
Архитектура Владимиро-Суздальского княжества Черенков Фёдор Фёдорович
Черенков Фёдор Фёдорович Электроника. Последовательностная логика
Электроника. Последовательностная логика Презентация Характеристика элементов вывозных таможенных пошлин. Ставки и порядок их применения
Презентация Характеристика элементов вывозных таможенных пошлин. Ставки и порядок их применения Новая конституция РФ (приложение)
Новая конституция РФ (приложение) Всероссийский физкультурно-спортивный комплекс «Готов к труду и обороне» (ГТО): актуальные вопросы внедрения
Всероссийский физкультурно-спортивный комплекс «Готов к труду и обороне» (ГТО): актуальные вопросы внедрения Основы защиты информации в телекоммуникационных системах
Основы защиты информации в телекоммуникационных системах  Методика развития гибкости у детей 8-9 лет, занимающихся греко-римской борьбой
Методика развития гибкости у детей 8-9 лет, занимающихся греко-римской борьбой Программа элективного курса «Основы фитодизайна»
Программа элективного курса «Основы фитодизайна» Виды юридической ответственности
Виды юридической ответственности Мировая политика и мировая экономика в условиях глобализации
Мировая политика и мировая экономика в условиях глобализации Регрессия — погружение в прошлые жизни
Регрессия — погружение в прошлые жизни Эл пособие ч 2
Эл пособие ч 2 Характеристики и виды организаций
Характеристики и виды организаций Теорема Виета (8 класс) - презентация по Алгебре_
Теорема Виета (8 класс) - презентация по Алгебре_ Современная тактика лечения ОРЗ у часто болеющих детей
Современная тактика лечения ОРЗ у часто болеющих детей  Концепция производственной демократии
Концепция производственной демократии  E-commerce web 2.0 для Полякова Елена проектировщик интерфейсов HumanoIT Group. - презентация
E-commerce web 2.0 для Полякова Елена проектировщик интерфейсов HumanoIT Group. - презентация Posters NPE
Posters NPE Заповеди блаженств
Заповеди блаженств 격조사 (падежные частицы). Корейские окончания. Урок 2-4
격조사 (падежные частицы). Корейские окончания. Урок 2-4 Асинхронные двигатели
Асинхронные двигатели Приостановление сроков исковой давности
Приостановление сроков исковой давности Система команд МП I80X86. Команди пересилання даних, зсуви та арифметичні команди
Система команд МП I80X86. Команди пересилання даних, зсуви та арифметичні команди Профессия автомеханик
Профессия автомеханик НЕВРОЛОГИЯ Клещевой энцефалит
НЕВРОЛОГИЯ Клещевой энцефалит C# и Entity FrameWork
C# и Entity FrameWork Component Enabler for .NET
Component Enabler for .NET