Содержание
- 2. Базисный набор | 1 〉 | 2 〉 … | k 〉 ... | n 〉
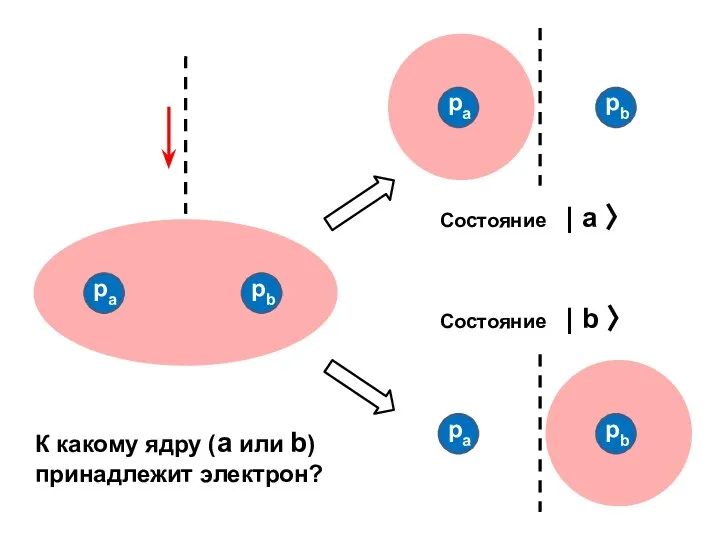
- 3. Молекулярный ион водорода [ Н–Н ]+ (два неподвижных протона + движущийся электрон)
- 4. К какому ядру (a или b) принадлежит электрон?
- 5. |Ca|2 = Рa — вероятность обнаружения электрона в окрестности ядра а |Cb|2 = Рb — вероятность
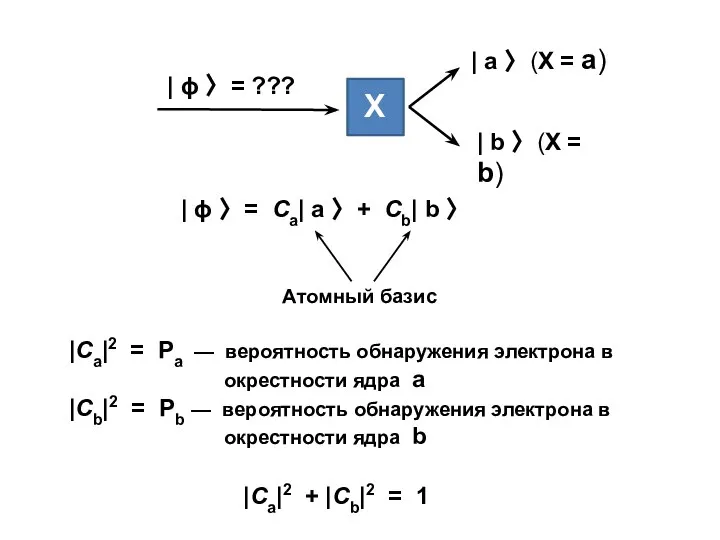
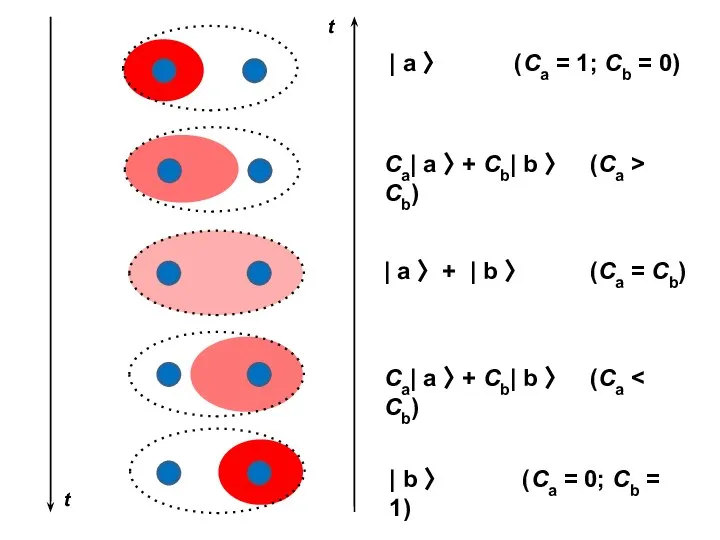
- 6. Произвольный вектор состояния, представленный в атомном базисе Собственные векторы оператора H
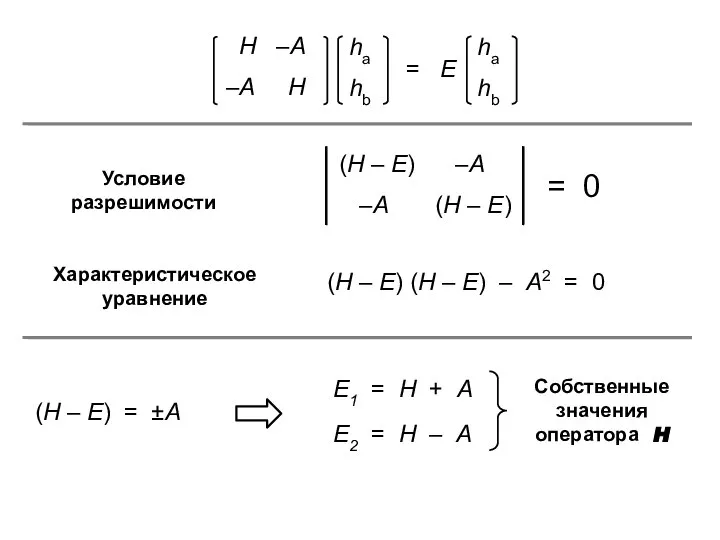
- 9. – hb = ha
- 10. hb = ha
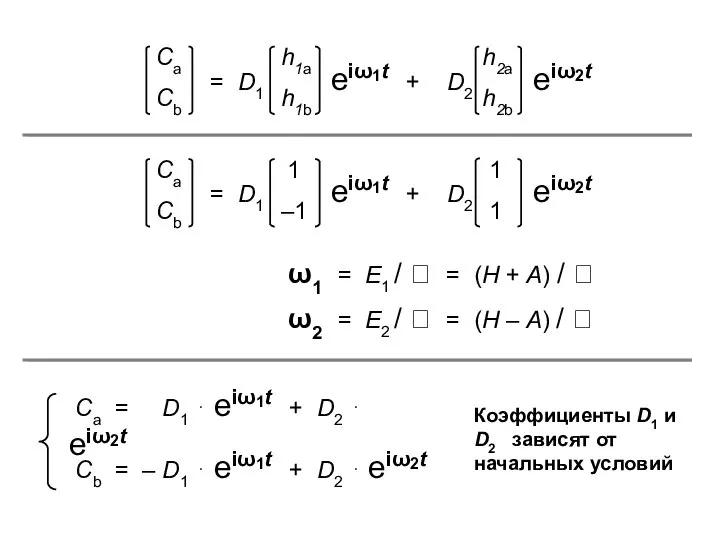
- 11. Сa = D1 ⋅ eiω1t + D2 ⋅ eiω2t Сb = – D1 ⋅ eiω1t +
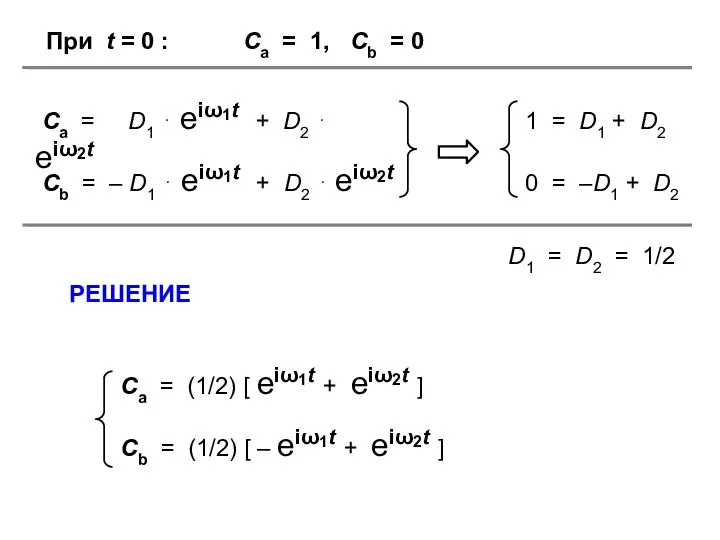
- 12. При t = 0 : Сa = 1, Сb = 0 D1 = D2 = 1/2
- 13. Pa = (1/4) [ eiω1t + eiω2t ] ⋅ [ e–iω1t + e–iω2t ] = Ра
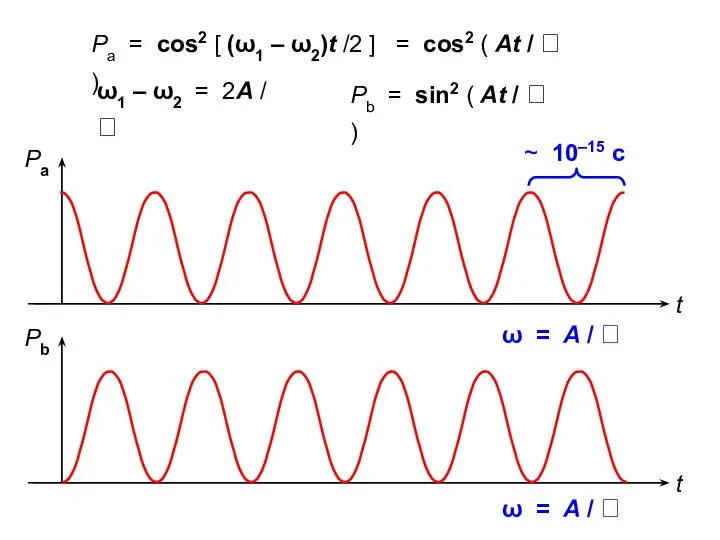
- 14. Pb = sin2 ( At / ) ω = A / ω = A
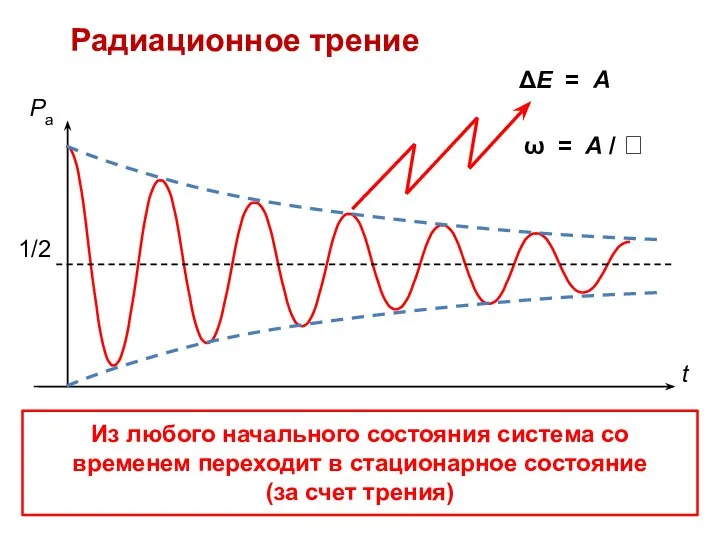
- 16. Радиационное трение Из любого начального состояния система со временем переходит в стационарное состояние (за счет трения)
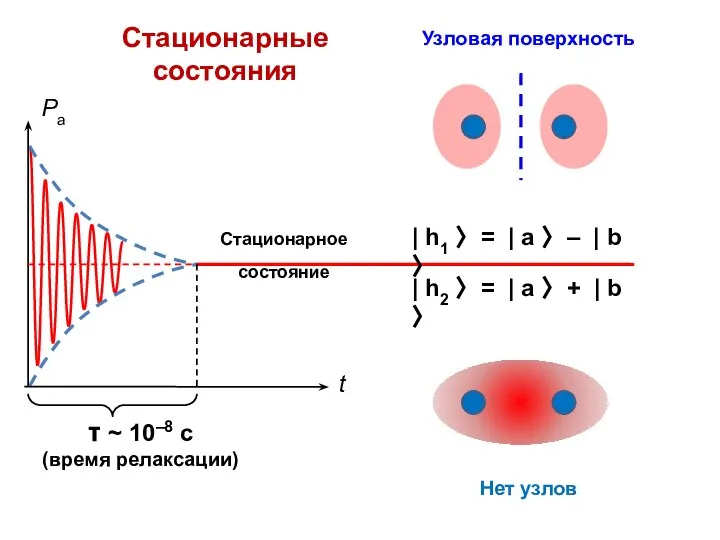
- 17. Узловая поверхность Стационарные состояния Нет узлов
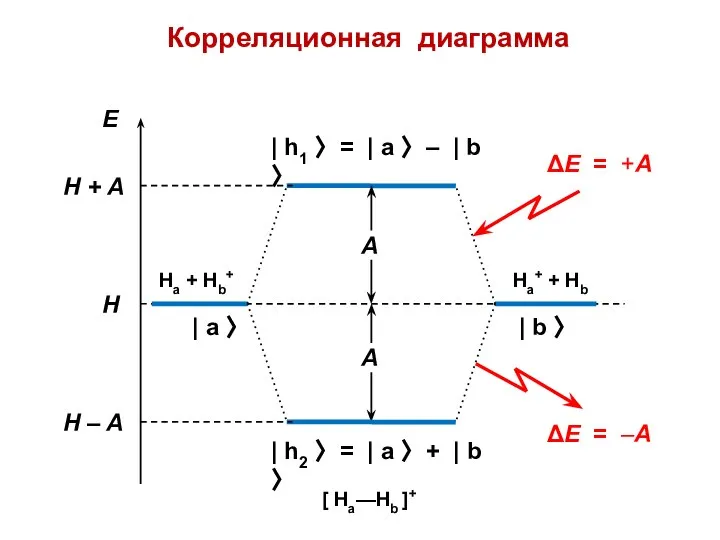
- 18. Корреляционная диаграмма Е H | h1 〉 = | a 〉 – | b 〉 |
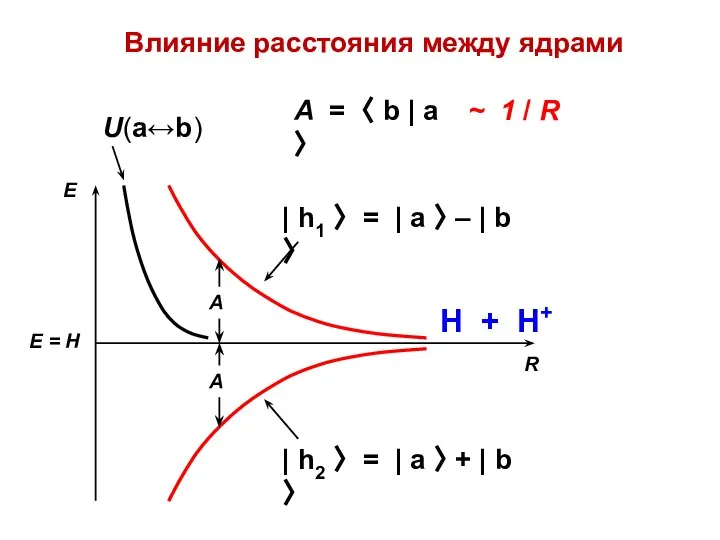
- 19. Влияние расстояния между ядрами А = 〈 b | a 〉 ~ 1 / R E
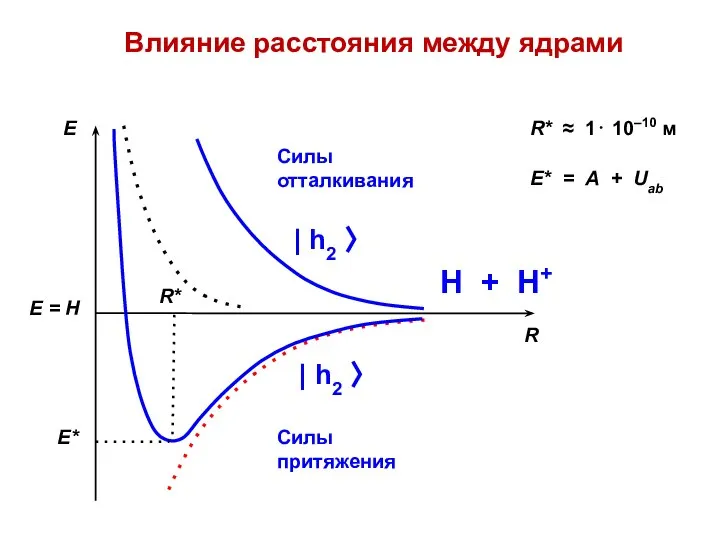
- 20. Влияние расстояния между ядрами Силы отталкивания Силы притяжения
- 21. КМ-резонанс — механизм образования химических связей При сближении атомов возникают колебания их электронных облаков, сопровождающиеся переходами
- 22. Из-за влияния межъядерного расстояния ( R ) на потенциальную энергию взаимодействия ядер ( Uab ) всякая
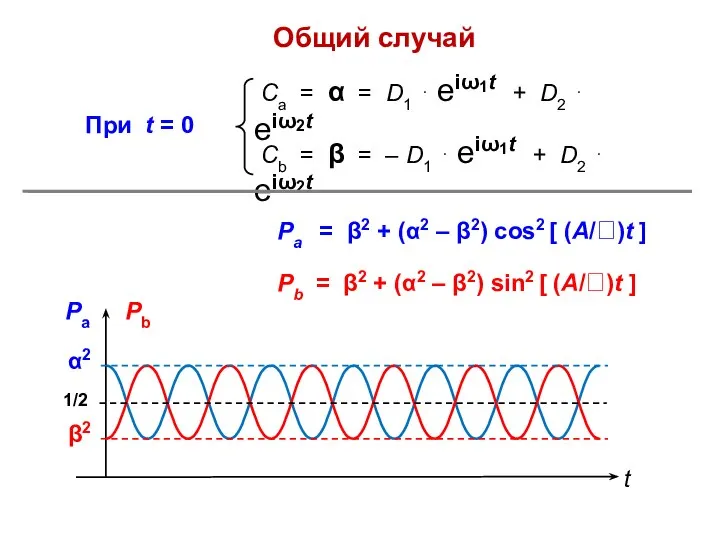
- 23. Общий случай Рa = β2 + (α2 – β2) cos2 [ (A/)t ] Рb = β2
- 24. Рa = β2 + (α2 – β2) cos2 [ (A/)t ] = β2 = 1/2 Рb
- 25. Несимметричные молекулы Собственные числа являются корнями характеристического уравнения: (Нaa – Е) ⋅ (Нbb – Е) –
- 27. Е1 ≅ (1/2)[(Haa + Hbb) + (Нaa – Нbb) + 4HabHba/2(Нaa – Нbb)] = = (1/2)[2Haa
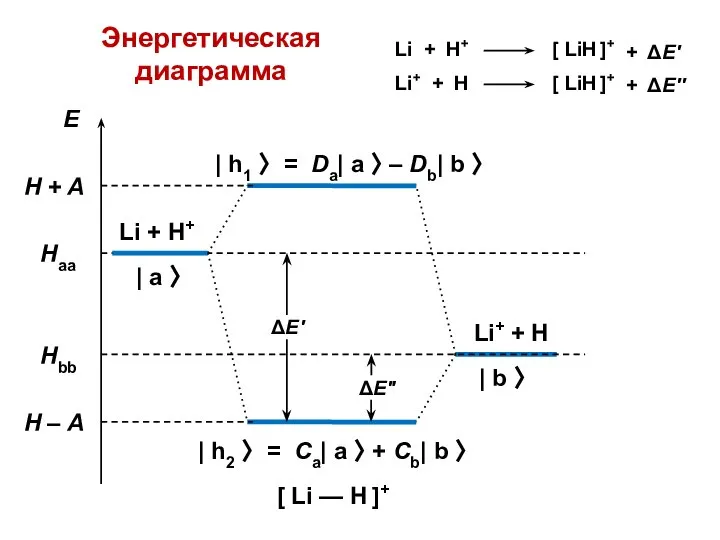
- 28. Энергетическая диаграмма
- 29. | h2 〉 = Ca| a 〉 + Cb| b 〉 [ Li — H ]+
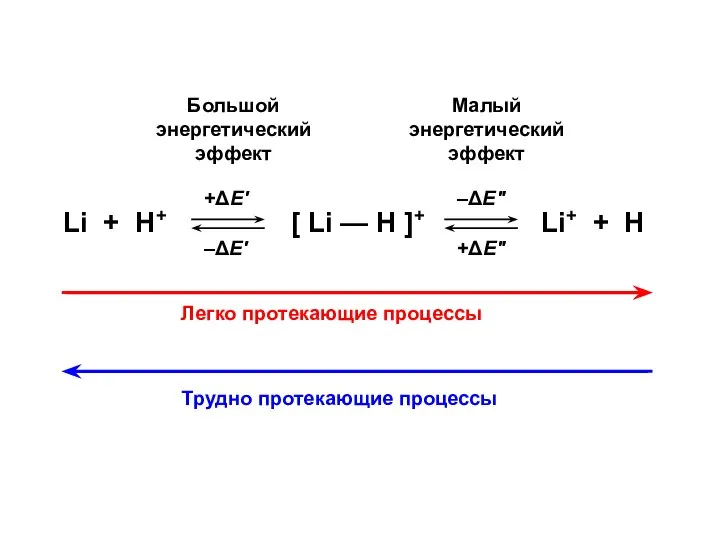
- 30. +ΔE' –ΔE' –ΔE" +ΔE" Большой энергетический эффект Малый энергетический эффект Легко протекающие процессы Трудно протекающие процессы
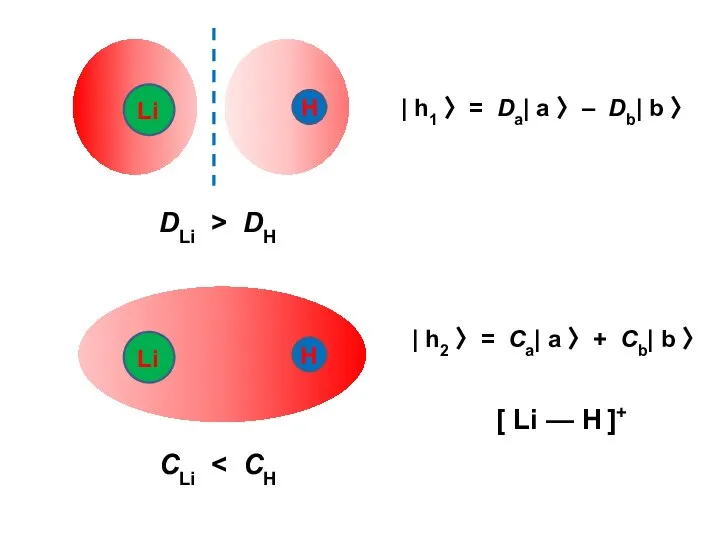
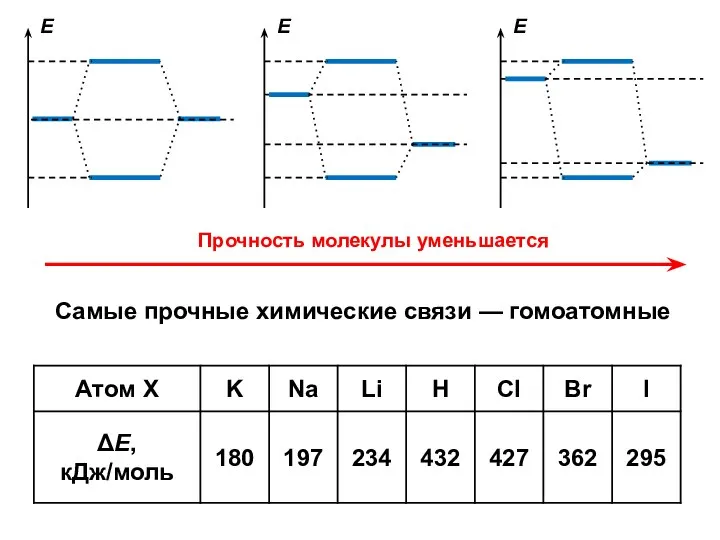
- 31. Прочность молекулы уменьшается Самые прочные химические связи — гомоатомные
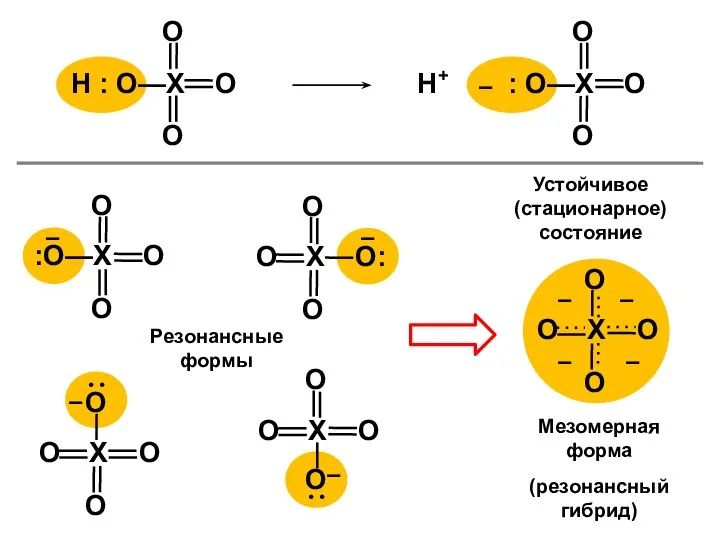
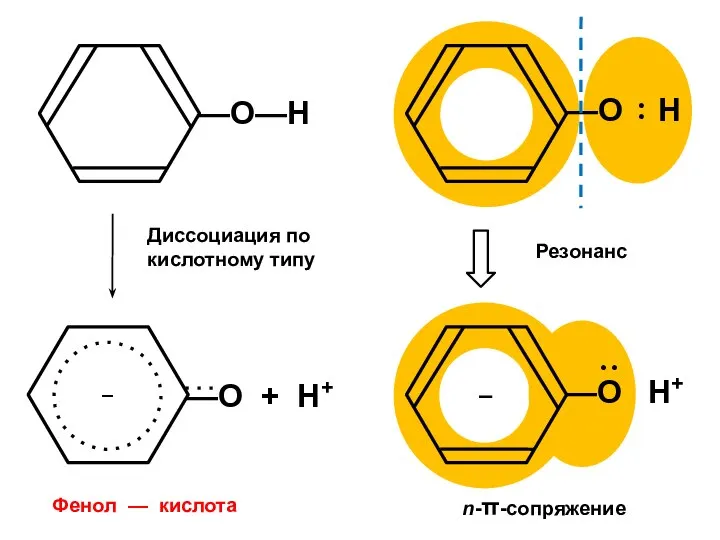
- 33. Н+ + –
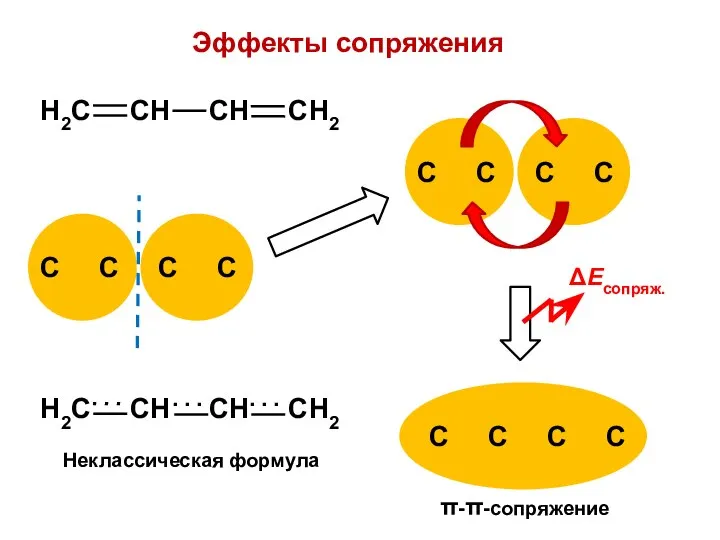
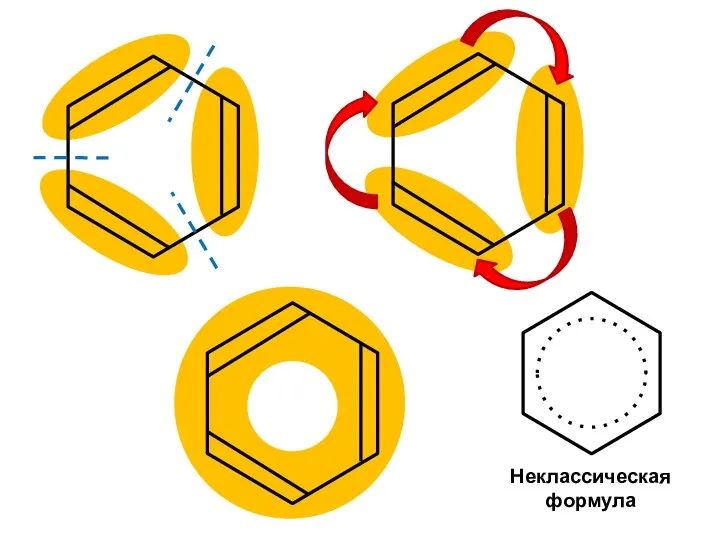
- 34. Эффекты сопряжения π-π-сопряжение
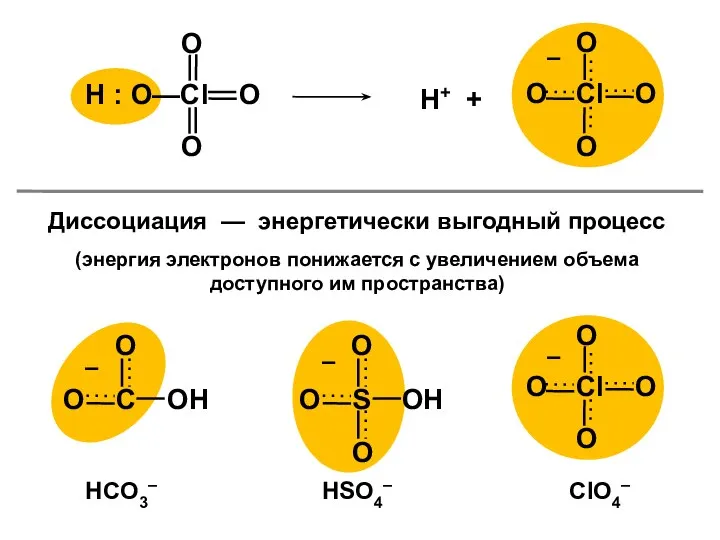
- 36. Диссоциация по кислотному типу n-π-сопряжение Фенол — кислота
- 38. Скачать презентацию

![Молекулярный ион водорода [ Н–Н ]+ (два неподвижных протона + движущийся электрон)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308416/slide-2.jpg)




![Pa = (1/4) [ eiω1t + eiω2t ] ⋅ [ e–iω1t](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308416/slide-12.jpg)


![Рa = β2 + (α2 – β2) cos2 [ (A/)t ]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1308416/slide-23.jpg)



 Усыновление в РФ Процесс. Органы и госслужащие, а также негосударственные организации, участвующие в процессе усыновления в СПб
Усыновление в РФ Процесс. Органы и госслужащие, а также негосударственные организации, участвующие в процессе усыновления в СПб Генератор сигналов на основе звуковой платы
Генератор сигналов на основе звуковой платы Программирование на языке Паскаль
Программирование на языке Паскаль ЦВП
ЦВП Велика Британия
Велика Британия Презентация "Новые чудеса света" - скачать презентации по МХК
Презентация "Новые чудеса света" - скачать презентации по МХК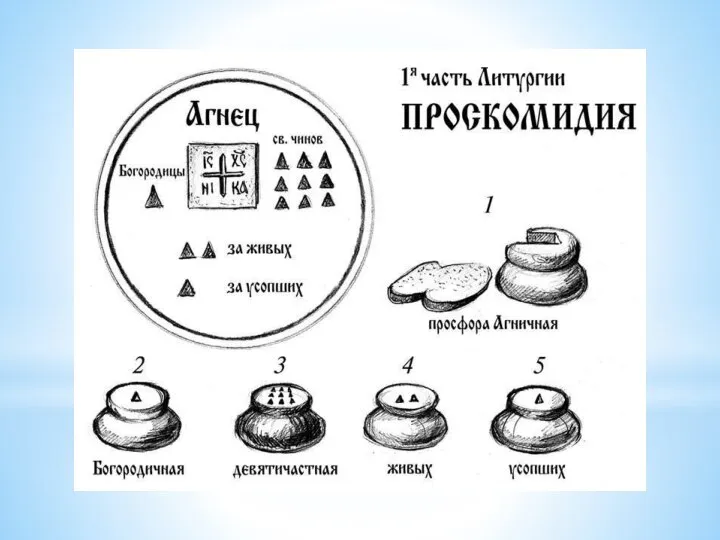 Проскомидия. Первая часть Литургии
Проскомидия. Первая часть Литургии Театр Востока
Театр Востока Презентация Корпоративные социальные инвестиции. Понятие, виды, индикаторы
Презентация Корпоративные социальные инвестиции. Понятие, виды, индикаторы Диалектика
Диалектика  Язык программирования Java
Язык программирования Java Роботизированная коробка передач
Роботизированная коробка передач Теоретико-правовые основы международной системы ПОД/ФТ (противодействие отмыванию доходов и финансированию терроризма)
Теоретико-правовые основы международной системы ПОД/ФТ (противодействие отмыванию доходов и финансированию терроризма) Анализ маркетинговой деятельности компании Красный куб подзаголовок
Анализ маркетинговой деятельности компании Красный куб подзаголовок Аманкелді Үдербайұлы Иманов (03.04.1873 18.5.1919)
Аманкелді Үдербайұлы Иманов (03.04.1873 18.5.1919) Художник и учёный Урок искусства 9 класс , Учитель Сомко Е.В.
Художник и учёный Урок искусства 9 класс , Учитель Сомко Е.В.  Кровельные и гидроизоляционные материалы
Кровельные и гидроизоляционные материалы Разработка вертикально-сверлильного станка
Разработка вертикально-сверлильного станка Легкая атлетика
Легкая атлетика Поисковое продвижение (SEO)
Поисковое продвижение (SEO) Ремонт штукатурки фасада с последующей окраской водными составами
Ремонт штукатурки фасада с последующей окраской водными составами Презентация_быстрые сервисы_и_ как правильно передать показания ПУ
Презентация_быстрые сервисы_и_ как правильно передать показания ПУ Особенности организации работы по физическому развитию детей дошкольного возраста в соответствии с ФГОС ДО
Особенности организации работы по физическому развитию детей дошкольного возраста в соответствии с ФГОС ДО Галактики, виды галактик
Галактики, виды галактик Сервлеты, компоненты приложений Java 2 Platform Enterprise Edition. (Лекция 17)
Сервлеты, компоненты приложений Java 2 Platform Enterprise Edition. (Лекция 17) Система змащення двигуна УТД - 20С1
Система змащення двигуна УТД - 20С1 Христос - наша праведность (оправдание) и наше освящение
Христос - наша праведность (оправдание) и наше освящение Культура как система знаков
Культура как система знаков