Содержание
- 2. Філософія хімічних досліджень та інженерії, що закликає до створення продуктів та процесів, які дозволять мінімізувати використання
- 3. Як хімічна філософія, зелена хімія має застосування до органічної хімії, неорганічної хімії, біохімії, аналітичної хімії та
- 4. Прикладом зеленої хімії можна назвати водневу енергетику, коли відновлювана енергія запасається у вигляді водню, отриманого із
- 5. В 1998 П. Т. Анастас і Дж. С. Уорнер у своїй книзі "Зелена хімія: теорія і
- 6. 1. Краще запобігти втратам, ніж переробляти і чистити залишки. 2. Методи синтезу треба вибирати таким чином,
- 7. 5. Допоміжні речовини при виробництві, такі, як розчинники або розділяють агенти, краще не використовувати зовсім, а
- 8. 9. Завжди слід віддавати перевагу каталітичним процесам (по можливості найбільш селективним). 10. Хімічний продукт повинен бути
- 9. 13. Якщо ви робите все так, як звикли, то і отримаєте те, що зазвичай отримуєте. Є.
- 10. Нові шляхи синтезу (часто це реакції з застосуванням каталізатора); Відновлювані вихідні реагенти (тобто отримані не з
- 11. В 2005 Р. Найорі (en: Ryoji Noyori) виділив три ключові напрямки розвитку Зеленої хімії: використання надкритичного
- 12. Найбільш поширений - використання каталізатора, який знижує енергетичний бар'єр реакції. Деякі з новітніх каталітичних процесів мають
- 13. Інший напрямок - використання локальних джерел енергії для активації молекул ( фотохімія, мікрохвильове випромінювання), що дозволяють
- 14. Велика надія покладається на використання сверхкритических рідин (в основному, вуглекислий газ і вода, меншою мірою -
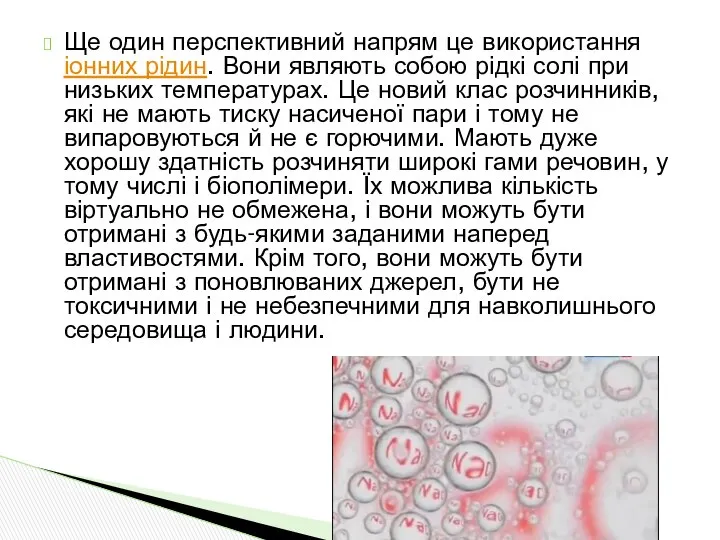
- 15. Ще один перспективний напрям це використання іонних рідин. Вони являють собою рідкі солі при низьких температурах.
- 16. Ще один шлях, що веде до цілей "зеленої хімії", - широке використання біомаси замість нафти, з
- 17. Працює кілька потужних заводів з отримання молочної кислоти з глюкози, отриманої з меляси і відходів целюлози.
- 19. Скачать презентацию















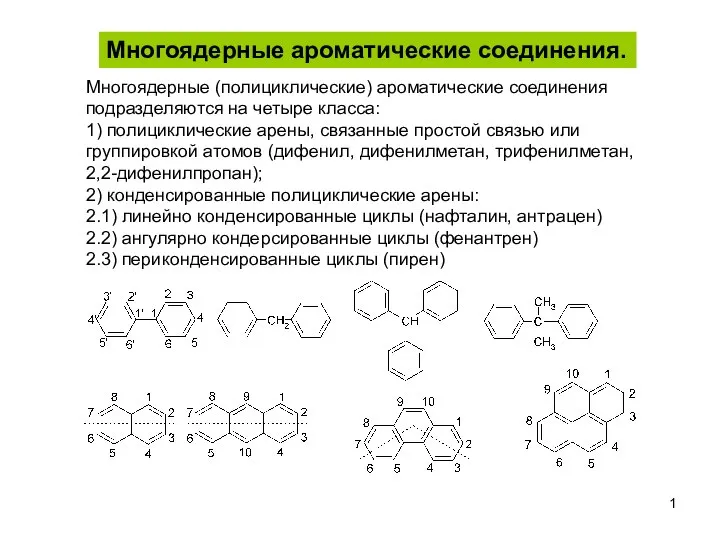 Многоядерные ароматические соединения
Многоядерные ароматические соединения Классификация углеводов
Классификация углеводов Жидкие системы
Жидкие системы Градуировка спектральных приборов
Градуировка спектральных приборов Химия в косметике
Химия в косметике Растворы высокомолекулярных соединений (ВМС)
Растворы высокомолекулярных соединений (ВМС) Презентация по Химии "Классы неорганических веществ" 8 класс
Презентация по Химии "Классы неорганических веществ" 8 класс Трифенилметановые красители
Трифенилметановые красители Гидролиз. Методы его получения и применения
Гидролиз. Методы его получения и применения Месторождения железистых кварцитов
Месторождения железистых кварцитов Опасные химикаты
Опасные химикаты 8 класс
8 класс  Электролиз.
Электролиз.  Фосфор как элемент мысли и жизни
Фосфор как элемент мысли и жизни Link reaction
Link reaction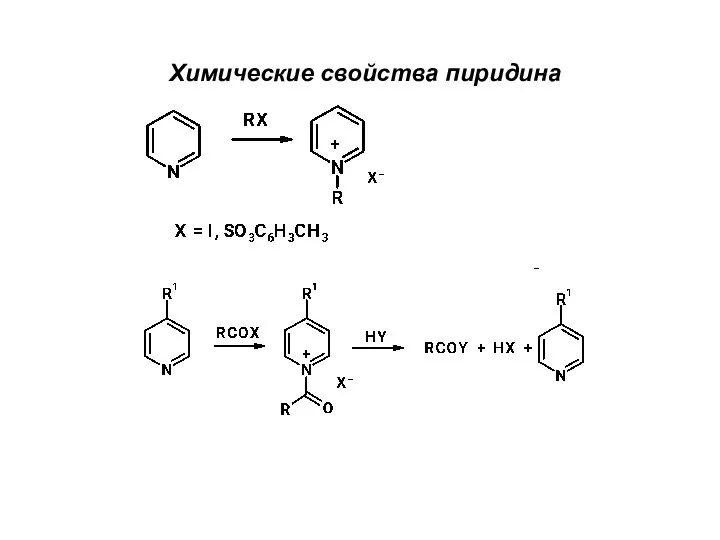 Химические свойства пиридина
Химические свойства пиридина Роль химических элементов в жизнедеятельности организма
Роль химических элементов в жизнедеятельности организма Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття
Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття Полярография и измерение рН
Полярография и измерение рН Арбузный снег. Предположения
Арбузный снег. Предположения Презентация по Химии "Алкены." - скачать смотреть бесплатно_
Презентация по Химии "Алкены." - скачать смотреть бесплатно_ Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Кількість речовини в хімії
Кількість речовини в хімії 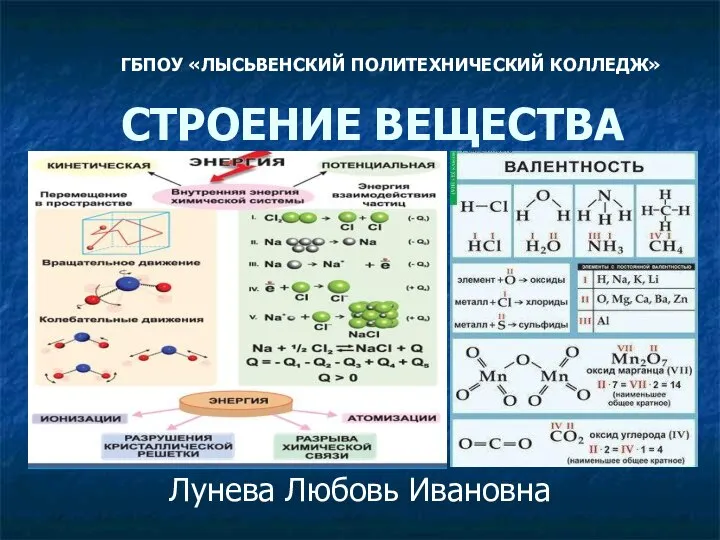 Строение вещества
Строение вещества Диктант: название алканов
Диктант: название алканов Трансформация соединений азота
Трансформация соединений азота Їх згубна дія на організм людини СПИРТИ
Їх згубна дія на організм людини СПИРТИ  Азот и фосфор
Азот и фосфор