Содержание
- 2. Определение Химия- наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения.
- 3. Основные понятия химии Вещество Молекулы и атомы Химический элемент Химическая формула Валентность Химическое уравнение Моль Оксид,
- 10. Строение атома Атом- мельчайшая химически неделимая электронейтральная частица вещества. В центре атома находится положительно заряженное ядро,
- 11. Строение атома Изотопы отличаются друг от друга числом нейтронов в ядре. Порядковый номер химического элемента показывает:
- 12. Периодический закон Д.И. Менделеева Свойства химических элементов и образуемых ими простых и сложных веществ находятся в
- 13. Строение периодической системы Периодическая система Менделеева- графическое отображение периодического закона. В ней 7 периодов, 10 рядов,
- 14. Явления
- 15. Химические явления (химические реакции)
- 16. Химическая формула Химическая формула – это условная запись состава вещества посредством химических знаков и индексов. СаСО3
- 17. Химическое уравнение Химическим уравнением называют условную запись химической реакции посредством химических знаков и формул 2Н2 +
- 18. Классификация химических реакций По числу и составу исходных и образующихся веществ
- 19. Индикаторы Индикаторы – вещества, которые под действием растворов кислот и щелочей изменяют свой цвет Лакмус, метиловый
- 20. Законы химии Закон сохранения массы веществ Закон постоянства состава веществ Закон Авогадро Периодический закон
- 21. Закон сохранения массы веществ Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ
- 22. Закон постоянства состава веществ Каждое химически чистое вещество независимо от места нахождения и способа получения имеет
- 23. Закон Авогадро Равные объемы любых газов (при одинаковых температуре и давлении) содержат равное число молекул.
- 24. Периодический закон Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости
- 25. Классы неорганических соединений
- 26. Классификация оксидов
- 27. Химические свойства основных оксидов
- 28. Химические свойства кислотных оксидов
- 29. Классификация оснований
- 30. Химические свойства щелочей 1. Щелочь + кислота = соль + вода NaOH + HCL = NaCL
- 31. Химические свойства нерастворимых оснований Нераст. осн. + кислота = соль + вода Cu(OH)2 + 2HCL =
- 32. Классификация кислот
- 33. Химические свойства кислот Изменяют цвет индикаторов С металлами С основными оксидами С основаниями С солями (
- 34. Классификация солей Средние (нормальные) – К2СО3 Кислые – КНСО3 Основные – Mg(OH)CL Двойные – К2NaPO4 Комплексные
- 35. Химические свойства солей Соль + кислота = другая соль+ другая кислота К2СО3 +2 НСL = 2
- 36. Генетическая связь между классами неорганических соединений Генетический ряд металлов 1.Металл- основный оксид- основание (щелочь)- соль Са-
- 37. Генетическая связь между классами неорганических соединений Генетический ряд неметаллов Неметалл- кислотный оксид- кислота- соль
- 38. Проверь свои знания Напиши формулы веществ: карбонат калия, оксид натрия, серная кислота, гидроксид кальция, хлорид магния,
- 40. Скачать презентацию





































 1_Bazovye_raschetnye_formuly
1_Bazovye_raschetnye_formuly Гетерофункциональные органические соединения
Гетерофункциональные органические соединения Свойства катализатора. Влияние массы катализатора на скорость реакции
Свойства катализатора. Влияние массы катализатора на скорость реакции Отбор проб товаров для анализа. Химико-аналитический контроль
Отбор проб товаров для анализа. Химико-аналитический контроль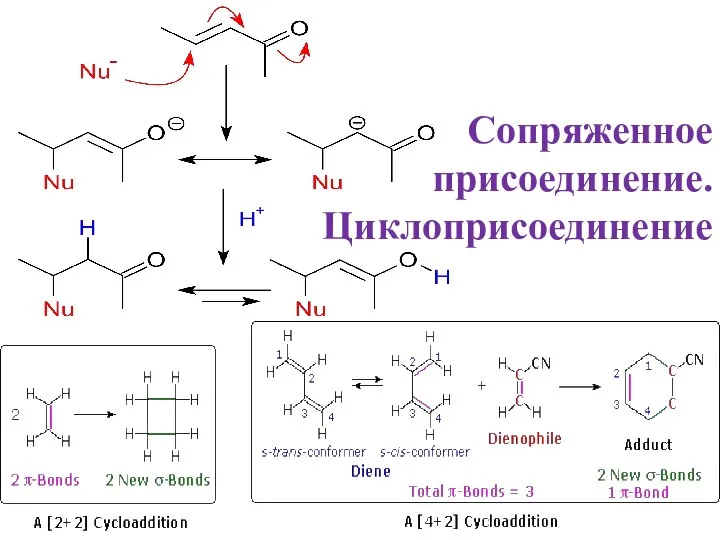 Сопряженное присоединение. Циклоприсоединениеie
Сопряженное присоединение. Циклоприсоединениеie Масс-спектрометрия (МС)
Масс-спектрометрия (МС) Классификации, номенклатура, строение и свойства органических соединений
Классификации, номенклатура, строение и свойства органических соединений Великие ученые XIX-XX веков
Великие ученые XIX-XX веков Презентация Электролиты
Презентация Электролиты Атоми і хімічні елементи. Молекули, їх рух. Дифузія
Атоми і хімічні елементи. Молекули, їх рух. Дифузія Производство шампуня. Технология
Производство шампуня. Технология 140 лет дому, который построил Д.И. Менделеев
140 лет дому, который построил Д.И. Менделеев 160198375
160198375 Презентация Лекарства дома
Презентация Лекарства дома Биохимия. Введение
Биохимия. Введение Углеводы (моносахариды, олигосахариды, полисахариды)
Углеводы (моносахариды, олигосахариды, полисахариды) Автомобильные бензины
Автомобильные бензины Силикатная промышленность
Силикатная промышленность Кислоты
Кислоты Виробництво біогазу Виконав: студент IV курсу групи БЛБ-43з Вила Віктор
Виробництво біогазу Виконав: студент IV курсу групи БЛБ-43з Вила Віктор  Хроматографические методы анализа
Хроматографические методы анализа Электролиз
Электролиз Оксиды. Химические свойства
Оксиды. Химические свойства Основные законы химии. Законы и формулировки
Основные законы химии. Законы и формулировки Метод крутого восхождения или метод Бокса-Уилсона. Симплексный метод оптимизации
Метод крутого восхождения или метод Бокса-Уилсона. Симплексный метод оптимизации Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Кислород. Свойства кислорода
Кислород. Свойства кислорода Валентность химических элементов (8 класс)
Валентность химических элементов (8 класс)