Содержание
- 2. Учебная цель: изучить способы получения, химические свойства и применение алкенов на примере непредельного углеводорода - этилена
- 3. Эпиграф к уроку «Границ научному познанию и предсказанию предвидеть невозможно» Д.И.Менделеев
- 4. Лист самоанализа учебной деятельности учащегося ___________ по теме «Получение, химические свойства и применение алкенов»
- 5. Ответьте, пожалуйста, на следующие вопросы: Какие углеводороды называются алкенами? Какова общая формула алкенов? Какова структурная формула
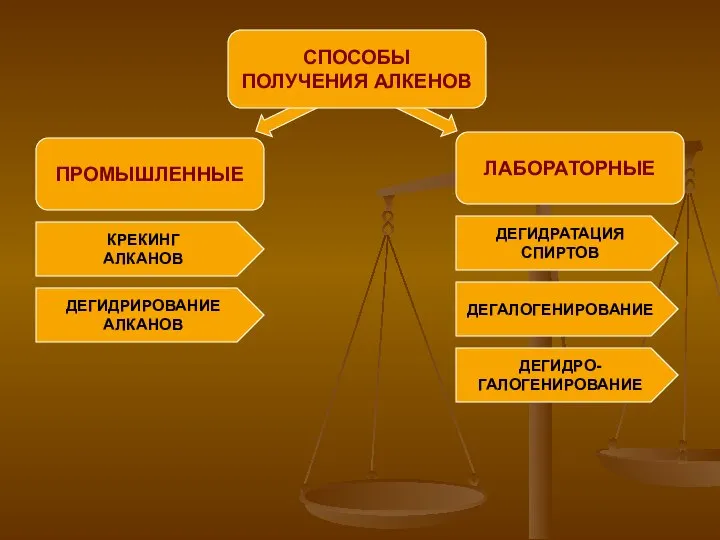
- 6. ПРОМЫШЛЕННЫЕ СПОСОБЫ ПОЛУЧЕНИЯ АЛКЕНОВ ЛАБОРАТОРНЫЕ КРЕКИНГ АЛКАНОВ ДЕГИДРИРОВАНИЕ АЛКАНОВ ДЕГИДРАТАЦИЯ СПИРТОВ ДЕГАЛОГЕНИРОВАНИЕ ДЕГИДРО- ГАЛОГЕНИРОВАНИЕ
- 7. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ КРЕКИНГ АЛКАНОВ АЛКАН → АЛКАН + АЛКЕН С БОЛЕЕ ДЛИННОЙ С МЕНЕЕ ДЛИНОЙ
- 8. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОД ПРИМЕР: Ni, t=500C Н3С - СН3
- 9. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРАТАЦИЯ СПИРТОВ СПИРТ → АЛКЕН + ВОДА ПРИМЕР: t≥140C, Н Н Н2SO4(конц.) Н-С
- 10. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГАЛОГЕНИРОВАНИЕ ПРИМЕР: t Н2С – СН2 + Zn → Н2С = СН2 +
- 11. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕ ПРИМЕР: спиртовой H H раствор Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O Н Cl
- 12. СХЕМЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ
- 13. РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ Это процесс соединения одинаковых молекул в более крупные. ПРИМЕР: n CH2=CH2 (-CH2-CH2-)n этилен полиэтилен
- 14. РЕАКЦИИ ОКИСЛЕНИЯ ГОРЕНИЕ АЛКЕНОВ ПРИМЕР: 2С2Н6 + 7О2 4СО2 + 6Н2О
- 15. РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНАГАНАТА КАЛИЯ (реакция Е.Е.Вагнера) Н2С=СН2 + [O] +
- 16. Применение этилена
- 19. Скачать презентацию














 Окислительно-восстановительное равновесие
Окислительно-восстановительное равновесие Материаловедение. Адсорбционные материалы. Металлоорганические каркасы
Материаловедение. Адсорбционные материалы. Металлоорганические каркасы Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Біохімічний рівень організації
Біохімічний рівень організації Акимовская ООШ №1 приветствует учителей ХИМИИ района Выступление учителя химии Галак Р.С.
Акимовская ООШ №1 приветствует учителей ХИМИИ района Выступление учителя химии Галак Р.С. Новые требования, предъявляемые к лабораторно-минералогическим исследованиям
Новые требования, предъявляемые к лабораторно-минералогическим исследованиям 1. История и актуальность темы. 2. Получение стекломассы 3. Стеклянные изделия 4. Применение и виды стекла: Энергосберегающ
1. История и актуальность темы. 2. Получение стекломассы 3. Стеклянные изделия 4. Применение и виды стекла: Энергосберегающ Производные морфинана (фенантренизохинолина)
Производные морфинана (фенантренизохинолина) Стан, роль і місце органічної хімії в сучасній хімічній освіті.
Стан, роль і місце органічної хімії в сучасній хімічній освіті.  Химия и производство
Химия и производство Катализ. Лекция 1
Катализ. Лекция 1 Влияние на скорость ферментативной реакции
Влияние на скорость ферментативной реакции Поливинилхлорид (ПВХ, PVC)
Поливинилхлорид (ПВХ, PVC) Липиды. Общая характеристика и классификация. (Модуль 4.8)
Липиды. Общая характеристика и классификация. (Модуль 4.8) Производство бензина
Производство бензина Подготовка учащихся к практическим турам олимпиад по химии
Подготовка учащихся к практическим турам олимпиад по химии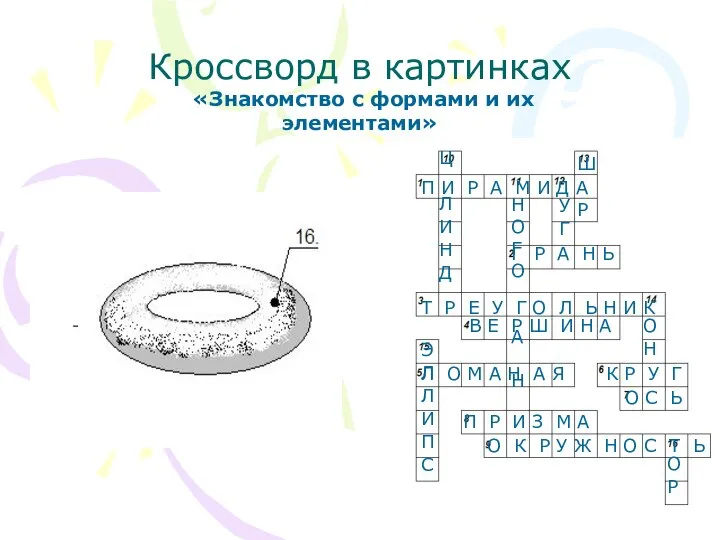 Кроссворд в картинках. Знакомство с формами и их элементами
Кроссворд в картинках. Знакомство с формами и их элементами Презентация по Химии "Синтетические моющие средства" - скачать смотреть
Презентация по Химии "Синтетические моющие средства" - скачать смотреть  Общая химическая технология
Общая химическая технология Анализ качества питьевой воды
Анализ качества питьевой воды  Реакции замещения и реакции обмена
Реакции замещения и реакции обмена Хлоридна кислота
Хлоридна кислота Физические свойства
Физические свойства Соединения железа
Соединения железа Химическая связь и ее виды
Химическая связь и ее виды История одного металла. Медь и её сплавы.
История одного металла. Медь и её сплавы.  Ֆլավանոիդներ պարունակող դեղաբույսեր եվ հումք
Ֆլավանոիդներ պարունակող դեղաբույսեր եվ հումք Классификация дисперсных систем. Коллигативные свойства растворов. Растворимость газов в воде. Термодинамика
Классификация дисперсных систем. Коллигативные свойства растворов. Растворимость газов в воде. Термодинамика