Содержание
- 2. Fе(ОН)3 → Fе2O3 + Н2O, Fе(ОН)3 + HCl → FеСl3 + Н2О, Li + O2 →
- 3. Fе(ОН)3 → Fе2O3 + Н2O, Fе(ОН)3 + HCl → FеСl3 + Н2О, Li + O2 →
- 4. Fе(ОН)3 → Fе2O3 + Н2O, Fе(ОН)3 + HCl → FеСl3 + Н2О, Li + O2 →
- 5. Zn + 2HCl → ZnCl2 + H2↑ Теперь заменим Zn на Fe и Cu: Fe +
- 6. Возьмем вместо раствора кислоты, раствор солей и металлы: CuSO4 + Fe → Cu↓ + FeSO4 2AgNO3
- 7. Тот металл, который располагается в ряду левее – вытесняет из соединений металл, который располагается правее. Для
- 8. Fе(ОН)3 → Fе2O3 + Н2O, Fе(ОН)3 + HCl → FеСl3 + Н2О, Li + O2 →
- 9. Fе(ОН)3 → Fе2O3 + Н2O, Fе(ОН)3 + HCl → FеСl3 + Н2О, Li + O2 →
- 10. Реакции, в результате которых два сложных вещества обмениваются своими составными частями. Реакции обмена –
- 11. Продуктами реакции взаимодействия щелочи и кислоты являются соль и вода – реакция нейтрализации. Общая схема реакции:
- 12. При взаимодействии щелочи с солями образуются новая соль и новое основание. Me(KO) + MeOH → Me(KO)
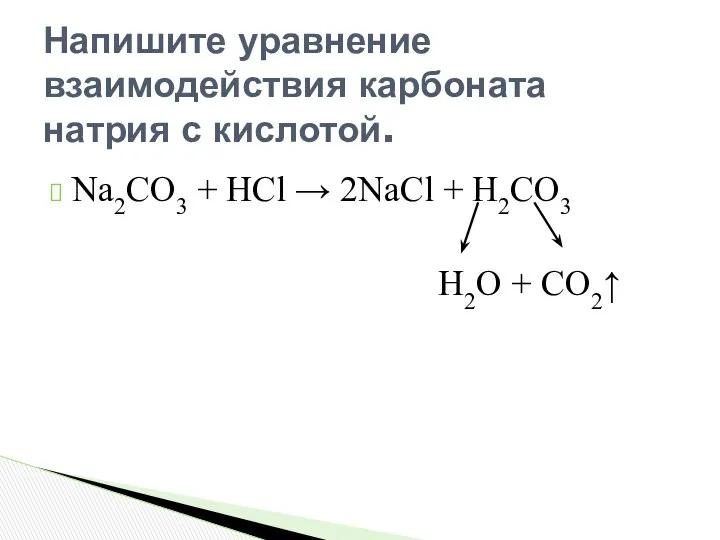
- 13. Na2CO3 + HCl → Напишите уравнение взаимодействия карбоната натрия с кислотой. 2NaCl + ?
- 14. Na2CO3 + HCl → 2NaCl + Н2СО3 Н2О + СО2↑ Напишите уравнение взаимодействия карбоната натрия с
- 15. Реакции обмена, протекающие в растворах, идут до конца только в том случае, если в результате их
- 17. Скачать презентацию













 Химический брейн-ринг
Химический брейн-ринг Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева
Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева Характеристика и технология производства основных катализаторов нефтепереработки
Характеристика и технология производства основных катализаторов нефтепереработки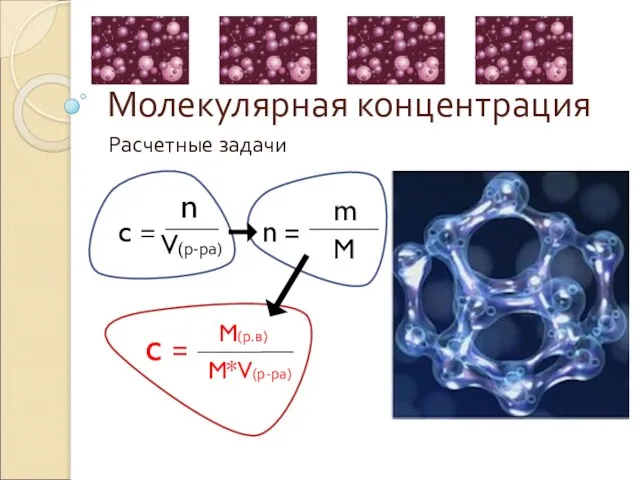 Молекулярная концентрация Расчетные задачи
Молекулярная концентрация Расчетные задачи Презентация по Химии "Мир кристаллов медного купороса" - скачать смотреть
Презентация по Химии "Мир кристаллов медного купороса" - скачать смотреть  Основные химические понятия
Основные химические понятия Закон действующих масс и его использование в расчетах. (Лекциии 4-6)
Закон действующих масс и его использование в расчетах. (Лекциии 4-6) XIII конференция ИХТРЭМС «Научно-практические проблемы в области химии и химических технологий»
XIII конференция ИХТРЭМС «Научно-практические проблемы в области химии и химических технологий» Презентация по Химии "Основные классы неогранических соединений" - скачать смотреть
Презентация по Химии "Основные классы неогранических соединений" - скачать смотреть  Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Классификация элементов. Электрохимическая цепь
Классификация элементов. Электрохимическая цепь История получения алюминия и его применение
История получения алюминия и его применение Поняття ПРО СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ НА ПРИКЛАДІ АСПІРИНУ
Поняття ПРО СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ НА ПРИКЛАДІ АСПІРИНУ Введение в органическую химию. 10 класс
Введение в органическую химию. 10 класс Green chemistry application to intermolecular forces
Green chemistry application to intermolecular forces Основы химической термодинамики
Основы химической термодинамики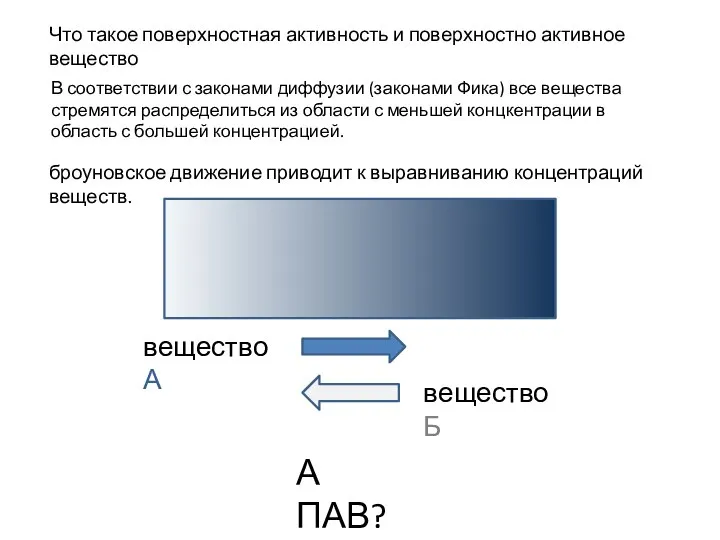 Поверхностная активность и поверхностно активное вещество
Поверхностная активность и поверхностно активное вещество Титан. История открытия титана
Титан. История открытия титана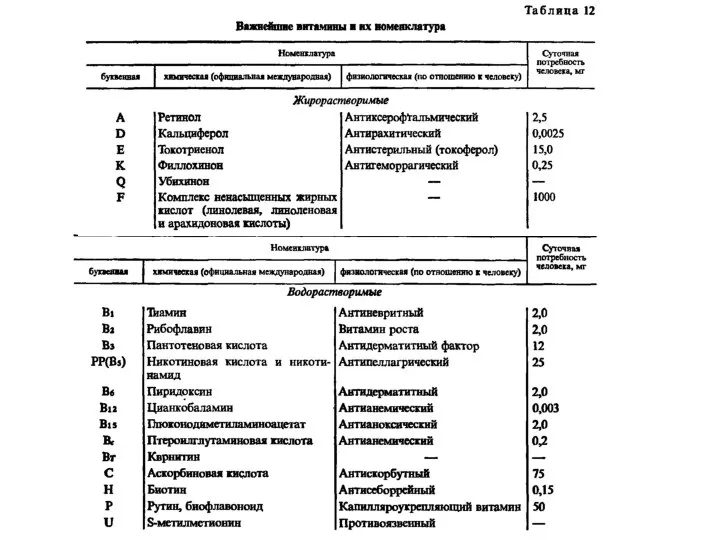 Важнейшие витамины и их номенклатура
Важнейшие витамины и их номенклатура Галогены. Химические свойства. Применение
Галогены. Химические свойства. Применение Железоуглеродистый сплав чугун
Железоуглеродистый сплав чугун Презентация для класса Способы получения натрия
Презентация для класса Способы получения натрия  Презентация по Химии "Белки" - скачать смотреть бесплатно_
Презентация по Химии "Белки" - скачать смотреть бесплатно_ Понятие синтетических лекарственных препаратов
Понятие синтетических лекарственных препаратов  Фосфор в природе
Фосфор в природе Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних
Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних Презентация по Химии "Теория строения химических соединений А.М. Бутлерова" - скачать смотреть
Презентация по Химии "Теория строения химических соединений А.М. Бутлерова" - скачать смотреть  Электролиз Цель: изучить сущность процесса электролиза Задачи: раскрыть принцип работы электролизёра суть катодных и анодных
Электролиз Цель: изучить сущность процесса электролиза Задачи: раскрыть принцип работы электролизёра суть катодных и анодных