Содержание
- 2. Химические процессы могут сопровождаться различными явлениями — поглощением и выделением теплоты, света, звука и т.д. В
- 3. Алессандро Вольта опытным путём установил ряд напряжений металлов: Zn, Pb, Sn, Fe, Cu, Ag, Au. Сила
- 4. В 1853 г. русский учёный, один из основоположников физической химии Николай Николаевич Бекетов (1827-1911) сделал в
- 5. Теоретическую основу ряда активности (и рядa напряжений) заложил немецкий физикохимик Вальтер Нернст (1864-1941).
- 6. Величина , характеризующая способность каждого металла переходить в раствор в виде ионов, а также восстанавливаться из
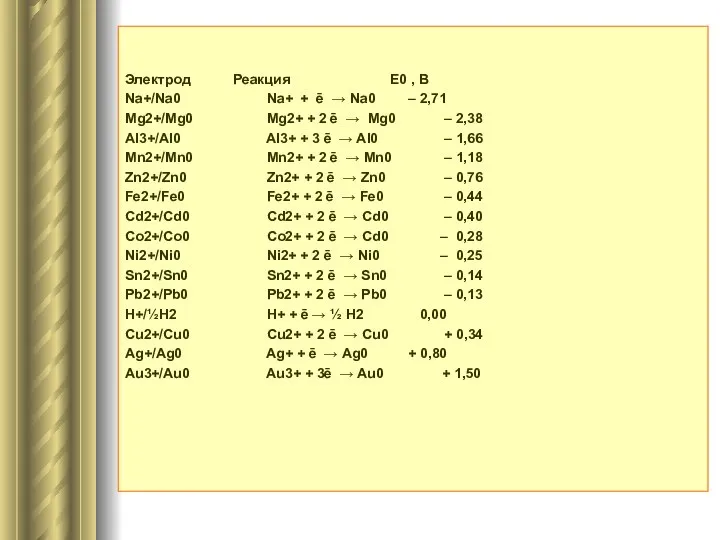
- 7. Электрод Реакция Е0 , В Na+/Na0 Na+ + ē → Na0 – 2,71 Mg2+/Mg0 Mg2+ +
- 8. Величина электродного потенциала зависит от природы металла, концентрации ионов в растворе, температуры и определяется уравнением Нернста:
- 9. Стандартный потенциал окислительно-восстановительной пары, в которой окисленной формой является выбранный нами окислитель, называется потенциалом окислителя φоОк,
- 10. Ряд стандартных электродных потенциалов характеризует восстановительную способность металлов в окислительно-восстановительных реакциях, протекающих в водной среде при
- 15. Скачать презентацию











 Неметаллы. Смотр знаний. Для учащихся 9 классов
Неметаллы. Смотр знаний. Для учащихся 9 классов Сложные эфиры. Жиры
Сложные эфиры. Жиры Аттестационная работа. Методика по химии 9 класс Исследовательская деятельность в решении экспериментальных задач
Аттестационная работа. Методика по химии 9 класс Исследовательская деятельность в решении экспериментальных задач Насыщенные углеводороды. (Тема 1.1)
Насыщенные углеводороды. (Тема 1.1) Презентация по Химии "Оксид алюмінію" - скачать смотреть бесплатно
Презентация по Химии "Оксид алюмінію" - скачать смотреть бесплатно Занимательные опыты по химии
Занимательные опыты по химии Бүйрек зәр түзе отырып, қаннан шығатын бөлінділерді сүзетін
Бүйрек зәр түзе отырып, қаннан шығатын бөлінділерді сүзетін Займання та горіння твердих горючих матеріалів (лекція 11)
Займання та горіння твердих горючих матеріалів (лекція 11) Кислоты. Повторение
Кислоты. Повторение Эволюция понятия “валентность”
Эволюция понятия “валентность” Презентация Принципы гормональной и нейромедиаторной регуляции
Презентация Принципы гормональной и нейромедиаторной регуляции 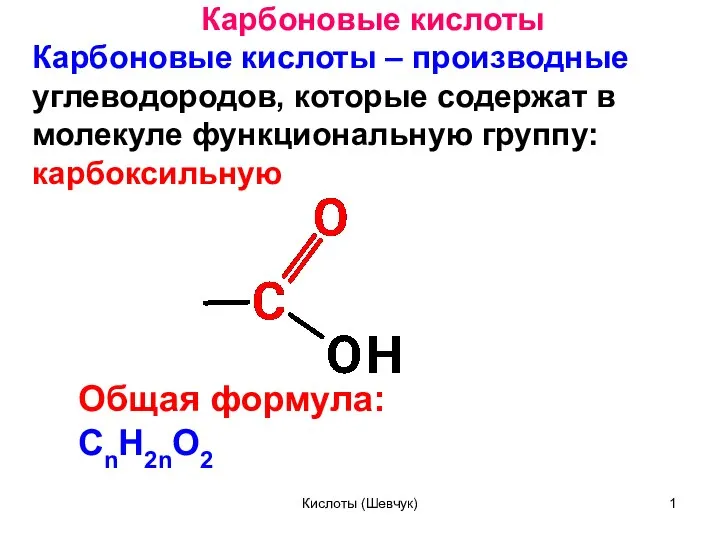 Карбоновые кислоты
Карбоновые кислоты Комплексные соединения
Комплексные соединения Значение минеральных веществ и витаминов в питании человека
Значение минеральных веществ и витаминов в питании человека Эндогенная серия. Скарновая группа
Эндогенная серия. Скарновая группа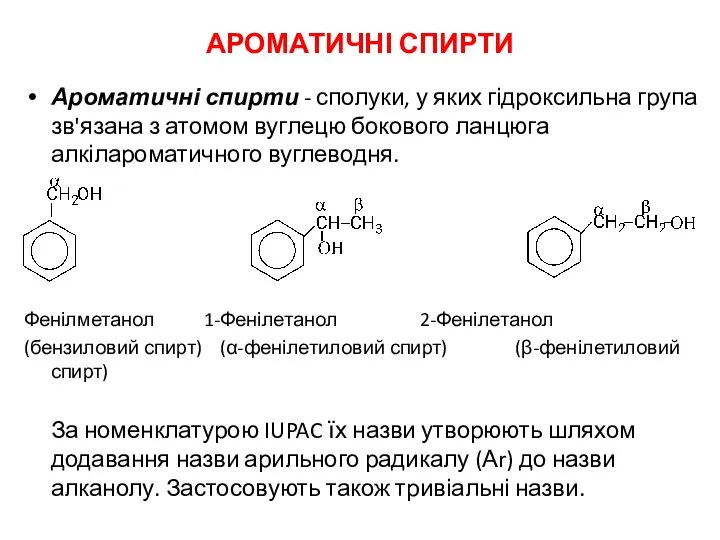 Ароматичні спирти
Ароматичні спирти Основы кристаллографии
Основы кристаллографии Происхождение рибосомы, белкового синтеза и генетического кода
Происхождение рибосомы, белкового синтеза и генетического кода Электролиз. Электролиз хлорида натрия
Электролиз. Электролиз хлорида натрия Термодинамика. Законы термодинамики
Термодинамика. Законы термодинамики Кристалы и их свойства
Кристалы и их свойства Амедео Авогадро
Амедео Авогадро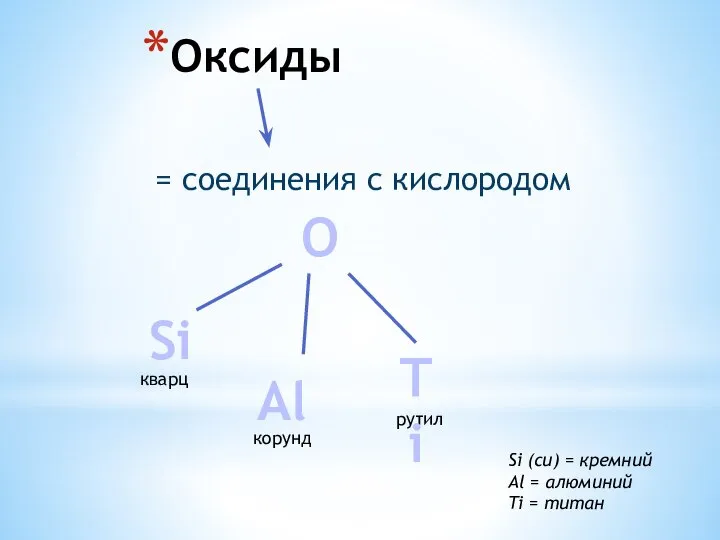 Оксиды. Кварц (SiO2). Корунд (Al2O3)
Оксиды. Кварц (SiO2). Корунд (Al2O3) Основания, их классификация и свойства в свете ТЭД
Основания, их классификация и свойства в свете ТЭД Кварцевые пески
Кварцевые пески Химические волокна (7 класс)
Химические волокна (7 класс) Галогены. Галогеноводородные кислоты и их соли
Галогены. Галогеноводородные кислоты и их соли Кристаллохимические радиусы
Кристаллохимические радиусы