Содержание
- 2. Биоорганическая химия изучает строение и свойства соединений, участвующих в процессах жизнедеятельности, во взаимосвязи с их биологическими
- 3. В основе теории органической химии, сформулированной А.М. Бутлеровым, лежит положение о зависимости свойств соединений от их
- 4. Рассмотрим электронное строение атомов тех элементов, которые чаще всего встречаются в структуре органических молекул: углерода, водорода,
- 6. Водород – элемент первого периода, следовательно, его внешний электронный уровень представлен только s-орбиталью (она имеет сферическую
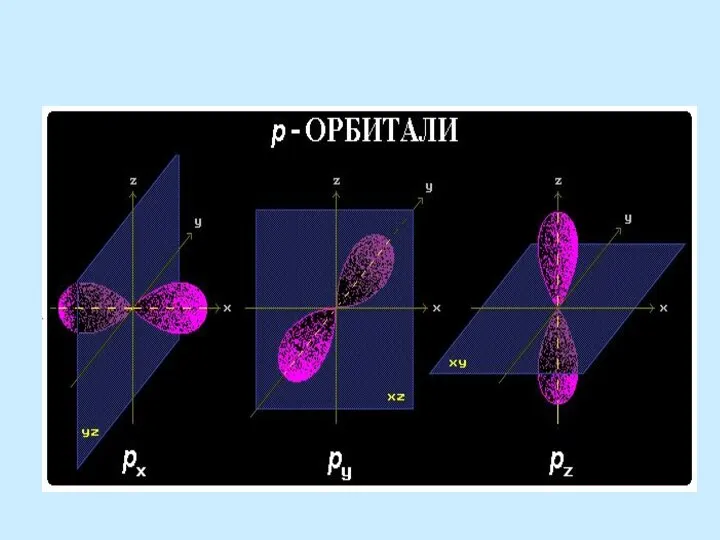
- 8. Углерод, азот и кислород – элементы второго периода, их внешний электронный уровень представлен одной s- и
- 12. Электронная конфигурация углерода в основном состоянии 1s22s22p2, т.е. углерод должен быть двухвалентным. Получая энергию, углерод переходит
- 13. В органической химии широко используются представления о гибридных орбиталях. Сущность гибридизации заключается в том, что из
- 14. Атомы углерода и азота могут находиться в одном из трёх состояний гибридизации - sp3, sp2, sp.
- 15. sp3-гибридизация
- 16. Гибридные орбитали равноценны, имеют форму неправильных объёмных восьмёрок и расположены в пространстве под углом 109о28’, т.е.
- 17. У атома углерода на каждой гибридной орбитали присутствует по одному электрону четыре электрона распределены по четырем
- 18. Электронная конфигурация sp3-гибридизованного атома азота отличается тем, что на одной из гибридных орбиталей у него присутствуют
- 19. Эту пару электронов называют неподелённой электронной парой, т.к. обычно она не участвует в образовании связей. неподелённая
- 20. У sp3-гибридизованного атома кислорода на двух гибридных орбиталях находится по два электрона (электронная формула кислорода 1s22s22p4):
- 21. У кислорода есть две неподелённых электронных пары. неподелённые электронные пары 104,5о Валентный угол sp3-гибридного атома кислорода
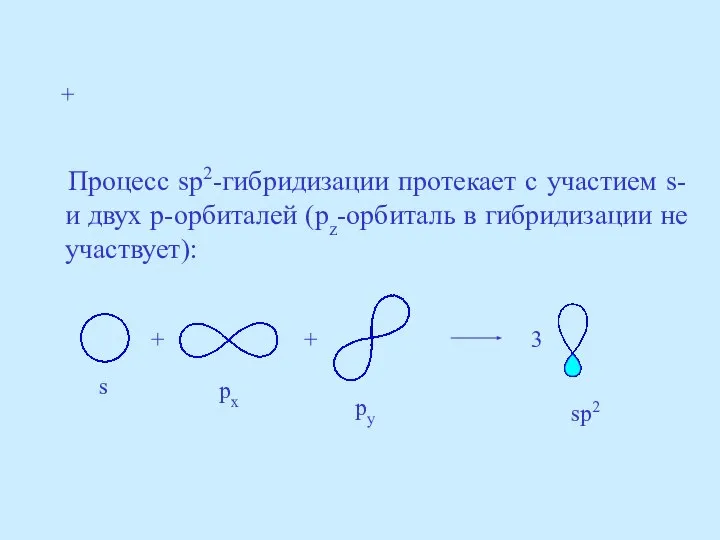
- 22. Процесс sp2-гибридизации протекает с участием s- и двух p-орбиталей (pz-орбиталь в гибридизации не участвует): + +
- 23. sp2-гибридизация Три гибридных орбитали располагаются в одной плоскости под углом 120о. Они направлены как бы к
- 24. Электронная конфигурация sp2-гибридизованного атома углерода На каждой из атомных орбиталей находится по одному электрону
- 25. Электронная конфигурация sp2-гибридизованного атома азота Неподеленная электронная пара может находиться на негибридной pz-орбитали Неподеленная электронная пара
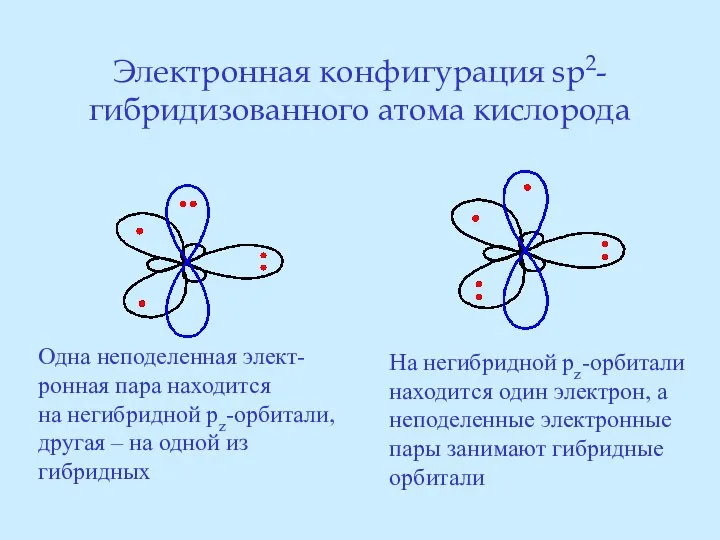
- 26. Электронная конфигурация sp2-гибридизованного атома кислорода Одна неподеленная элект- ронная пара находится на негибридной pz-орбитали, другая –
- 27. Процесс sp-гибридизации протекает с участием s- и px-орбитали (py и pz-орбитали в гибридизации не участвуют): +
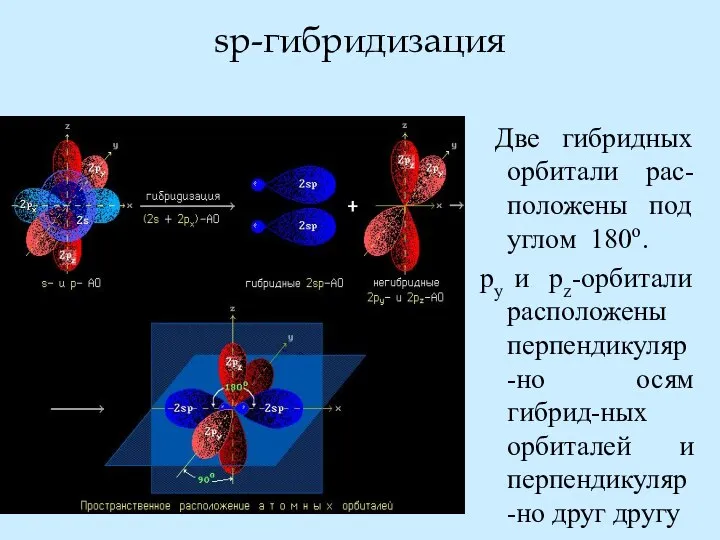
- 28. sp-гибридизация Две гибридных орбитали рас-положены под углом 180о. py и pz-орбитали расположены перпендикуляр-но осям гибрид-ных орбиталей
- 29. Электронная конфигурация sp-гибридизованного атома углерода На каждой орбитали находится по одному электрону
- 30. Электронная конфигурация sp-гибридизованного атома азота Неподеленная электронная пара всегда находится на одной из гибридных орбиталей
- 31. Почему важно научиться определять тип гибридизации атомов в молекуле Это необходимо для понимания распределения электронной плотности
- 32. Как определить тип гибридизации атомов в молекуле Для углерода тип гибридизации определяется по количеству σ-связей. σ-Связи
- 33. Как определить тип гибридизации атомов в молекуле CH2 CH CH3 1 2 3 пропен Первый атом
- 34. Как определить тип гибридизации атомов в молекуле CH C CH3 1 2 3 пропин Первый атом
- 35. Как определить тип гибридизации атомов в молекуле Тип гибридизации атомов азота и кислорода определяется по соседнему
- 36. Если мы установили, что атом азота или кислорода находятся в sp2-гибридизации, необходимо определить его электронную конфигурацию
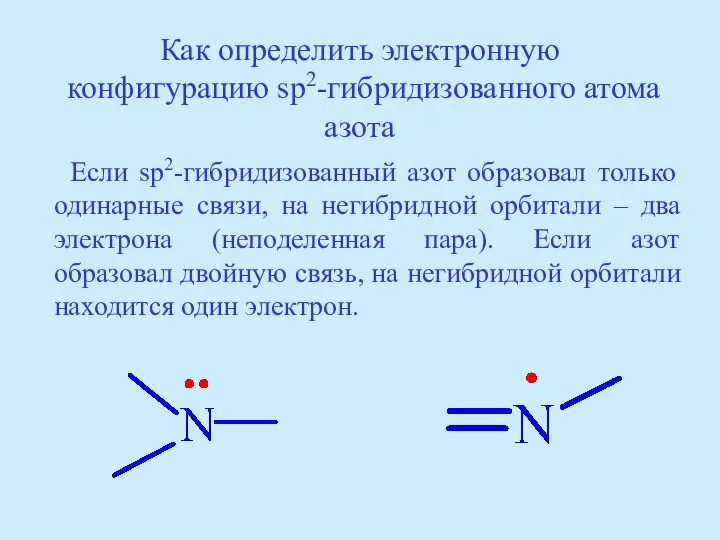
- 37. Как определить электронную конфигурацию sp2-гибридизованного атома азота Если sp2-гибридизованный азот образовал только одинарные связи, на негибридной
- 38. Как определить электронную конфигурацию sp2-гибридизованного атома кислорода Если sp2-гибридизованный кислород образовал только одинарные связи, на негибридной
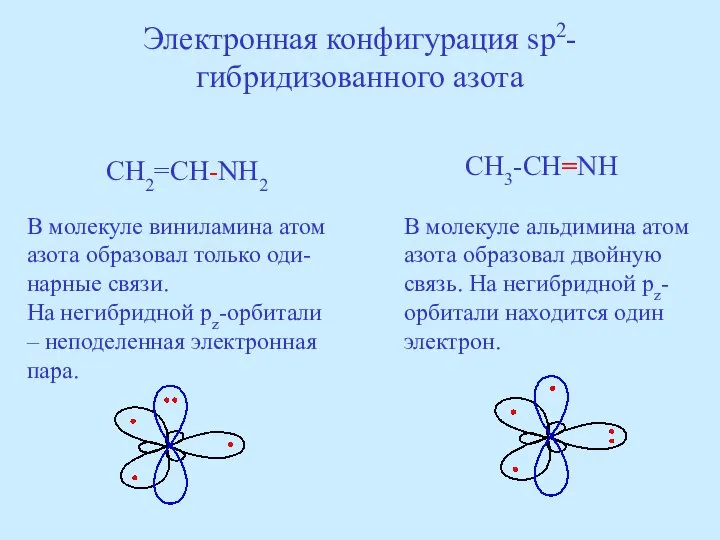
- 39. Электронная конфигурация sp2-гибридизованного азота CH2=CH-NH2 CH3-CH=NH В молекуле виниламина атом азота образовал только оди-нарные связи. На
- 40. Электронная конфигурация sp2-гибридизованного кислорода CH2=CH-O-CH3 CH3-C-CH3 O В молекуле метилвинилового эфира атом кислорода образовал только одинарные
- 41. Химические связи в органических молекулах Химические связи – это силы, посредством которых атомы удерживаются в молекулах.
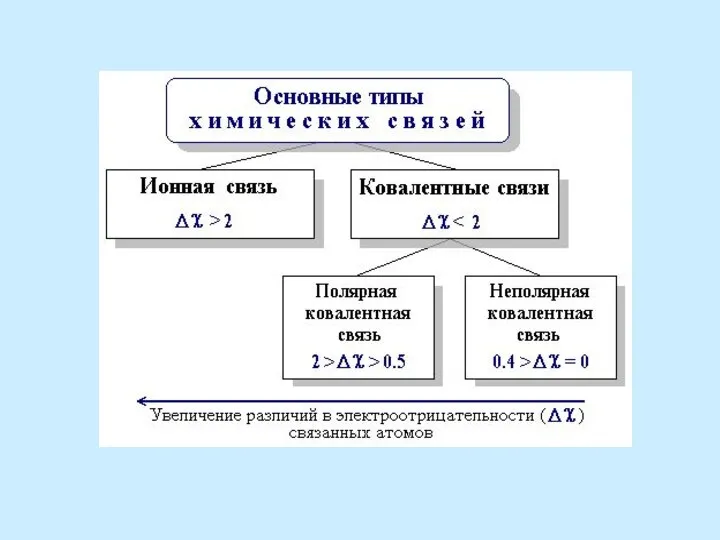
- 42. При образовании связей атомы завершают внешний энергетический уровень. Основными типами связи являются ионная (электровалентная) и ковалентная.
- 44. Схемы образования ионной и ковалентной связей + + ионная связь ковалентная связь
- 45. Образование ионной связи + - ионы Между противоположно заряженными ионами возникают силы притяжения.
- 46. Кристаллическая решетка NaCl
- 47. Образование ковалентной связи общая электронная пара Оба атома хлора завершили внеш- ний электронный уровень
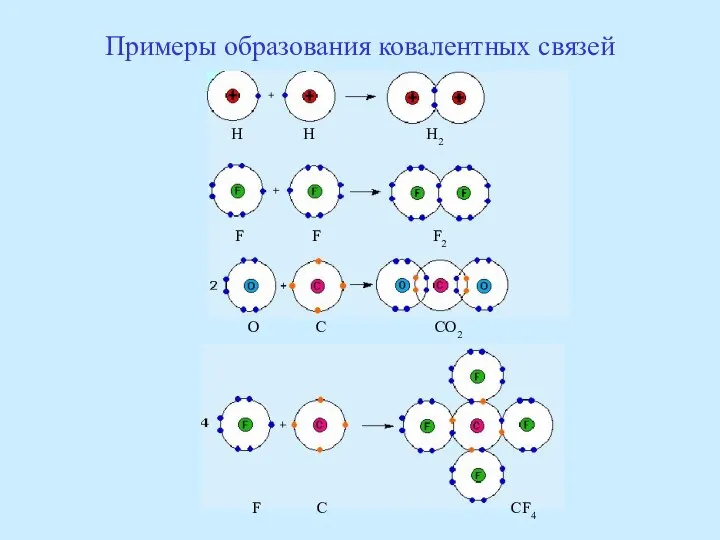
- 48. Примеры образования ковалентных связей H H H2 F F F2 O C CO2 F C CF4
- 50. Ковалентная связь может образоваться и по донорно-акцепторному механизму: один из атомов предоставляет пару электронов, а другой
- 51. Существует два типа ковалентных связей – σ- и π-. σ-Связью называется ковалентная связь, образованная при перекрывании
- 52. s- s- p- p- гибридная
- 53. π-Связь образуется при боковом перекрывании негибридных p-орбиталей с максимумом перекрывания по обе стороны от оси, соединяющей
- 55. Встречающиеся в органических соединениях кратные связи являются сочетанием σ- и π-связей: двойная - одна σ- и
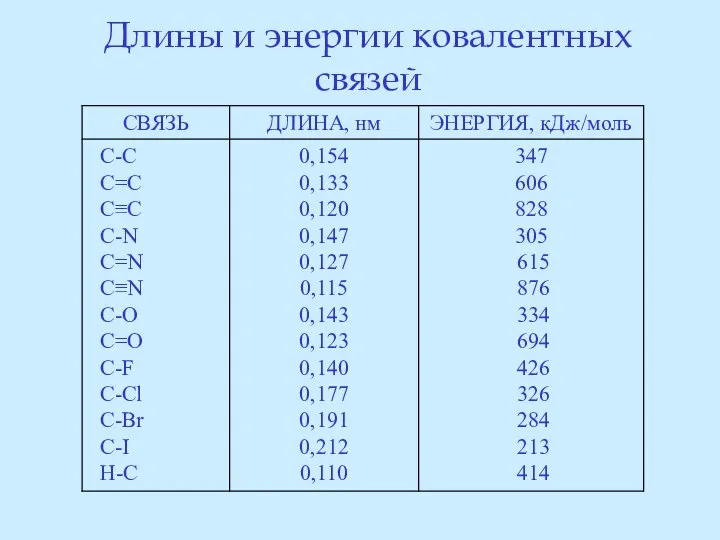
- 56. Свойства ковалентной связи выражаются следующими характеристиками: длина энергия полярность поляризуемость
- 57. Длина связи – это расстояние между центрами связанных атомов. Длина связи является её важной характеристикой, т.к.
- 58. Чтобы сравнить длины различных связей, нужно сравнить атомные радиусы атомов, а это можно сделать, используя Периодическую
- 59. H H Сравним длины связей H-H, H-Cl и Cl-Cl. Водород – элемент 1-го периода, хлор –
- 60. Двойная связь короче одинарной, тройная – короче двойной. Это связано с тем, что между ядрами атомов,
- 61. Энергия связи – это энергия (в расчёте на 1 моль), которая выделилась в результате образования связи.
- 62. Чем короче связь, тем она прочнее (например, H-H связь прочнее Cl-Cl связи). σ-Связь прочнее π-связи, т.к.
- 63. Длины и энергии ковалентных связей
- 64. Полярность связи – это неравномерное распределение электронной плотности связи между двумя атомами из-за различия в их
- 65. Чем больше разница в электроотрицательности атомов, тем полярнее связь, т.е. тем более общая электронная пара смещена
- 66. Поляризуемость – лёгкость, с которой смещаются электроны связи под действием внешних воздействий (электрическое поле, реагирующая частица,
- 67. + + - связь неполярна связь полярна Под действием внешнего электрического поля произошла поляризация связи
- 69. Скачать презентацию

























































 Ферменты и гормоны Урок химии в 10 (11) классе Автор: учитель химии Ким Н.В. МОУ СОШ №6 г. Нягани ХМАО-Югры Тюменской области
Ферменты и гормоны Урок химии в 10 (11) классе Автор: учитель химии Ким Н.В. МОУ СОШ №6 г. Нягани ХМАО-Югры Тюменской области Квалификация химических реактивов, принятая в РФ
Квалификация химических реактивов, принятая в РФ Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша)
Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша) Получение, собирание и распознавание водорода
Получение, собирание и распознавание водорода Розчини
Розчини Зелёные камни
Зелёные камни Гормоны. Виды и классификация гормонов
Гормоны. Виды и классификация гормонов Анодные реакции коррозионного процесса
Анодные реакции коррозионного процесса Электрохимические процессы
Электрохимические процессы Теобромин
Теобромин Карбо́новые кисло́ты
Карбо́новые кисло́ты Строение атома
Строение атома Смесители. Пропеллерная мешалка
Смесители. Пропеллерная мешалка Презентация по Химии "Применение электролиза" - скачать смотреть
Презентация по Химии "Применение электролиза" - скачать смотреть  Перевариваемые полисахариды злаковых, бобовых, овощей, ягод и фруктов. Крахмал (амилоза, амилопектин), фруктаны (инулин)
Перевариваемые полисахариды злаковых, бобовых, овощей, ягод и фруктов. Крахмал (амилоза, амилопектин), фруктаны (инулин) Р-элементы IV группы: C, Si, Ge, Sn, Pb
Р-элементы IV группы: C, Si, Ge, Sn, Pb Задача №9. Глицерин. Команда Карбораны
Задача №9. Глицерин. Команда Карбораны ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств
ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств Презентация по Химии "Насичені одноатомні спирти" - скачать смотреть бесплатно
Презентация по Химии "Насичені одноатомні спирти" - скачать смотреть бесплатно К 180-летию со дня рождения Д.И. Менделеева
К 180-летию со дня рождения Д.И. Менделеева Пегматитовые месторождения
Пегматитовые месторождения Chemical bonding and Molecular Structure
Chemical bonding and Molecular Structure Обобщающий урок –игра Звездный час по теме Подгруппа кислорода
Обобщающий урок –игра Звездный час по теме Подгруппа кислорода Распределение примесей в процессе выращивания мультикристаллического кремния
Распределение примесей в процессе выращивания мультикристаллического кремния Комплексные соединения
Комплексные соединения Типы химических реакций на примере свойств воды
Типы химических реакций на примере свойств воды  Алкилирование изобутана олефинами
Алкилирование изобутана олефинами Гигиенические нормативы. Химические факторы окружающей среды
Гигиенические нормативы. Химические факторы окружающей среды