Содержание
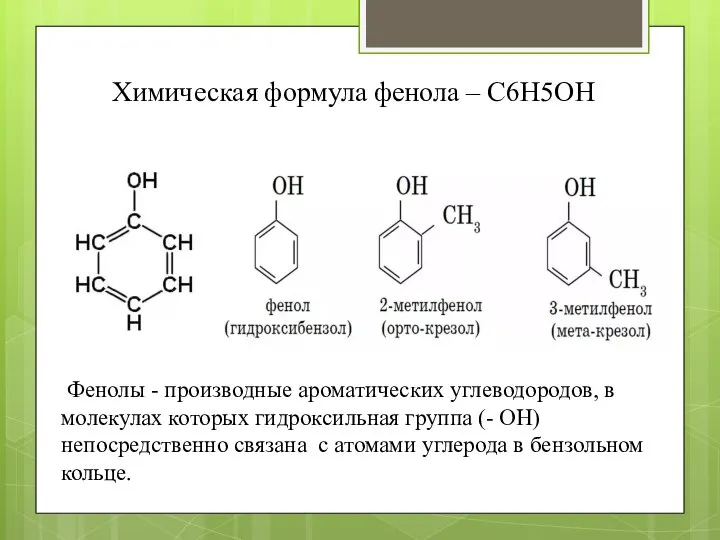
- 2. Химическая формула фенола – С6H5ОН Фенолы - производные ароматических углеводородов, в молекулах которых гидроксильная группа (-
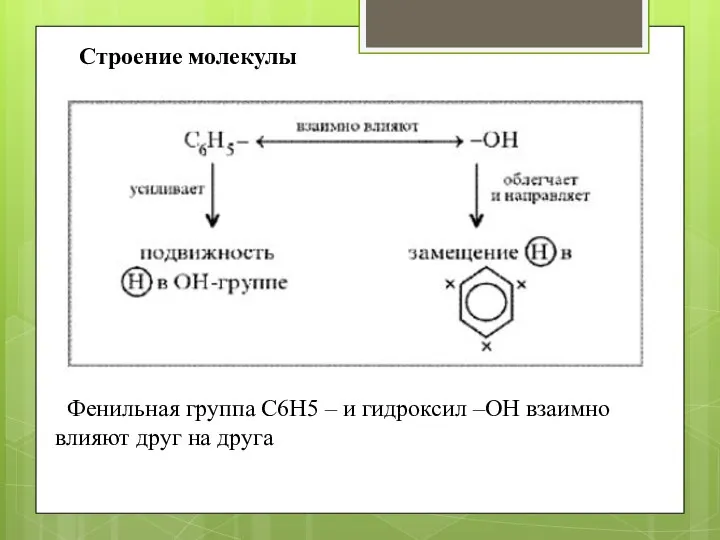
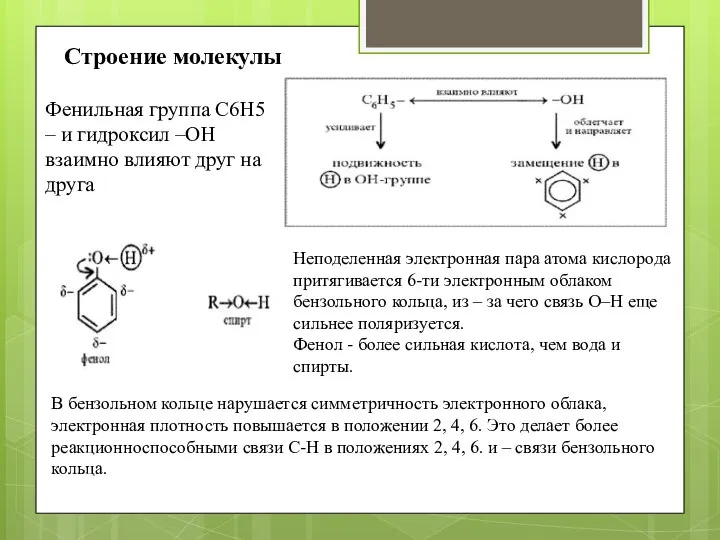
- 3. Строение молекулы Фенильная группа C6H5 – и гидроксил –ОН взаимно влияют друг на друга
- 4. Не поделённая электронная пара атома кислорода притягивается 6-ти электронным облаком бензольного кольца, из – за чего
- 5. Химические свойства фенола I. Свойства гидроксильной группы Кислотные свойства – выражены ярче, чем у предельных спиртов
- 6. II. Свойства бензольного кольца 1). Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях
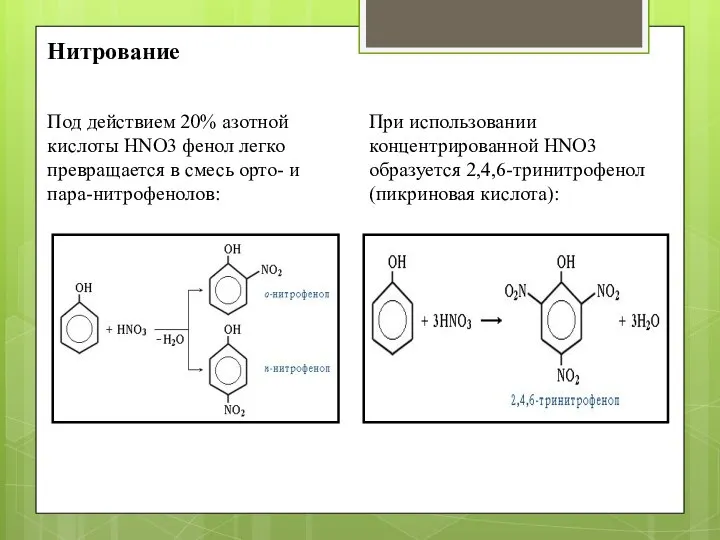
- 7. Нитрование Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов: При
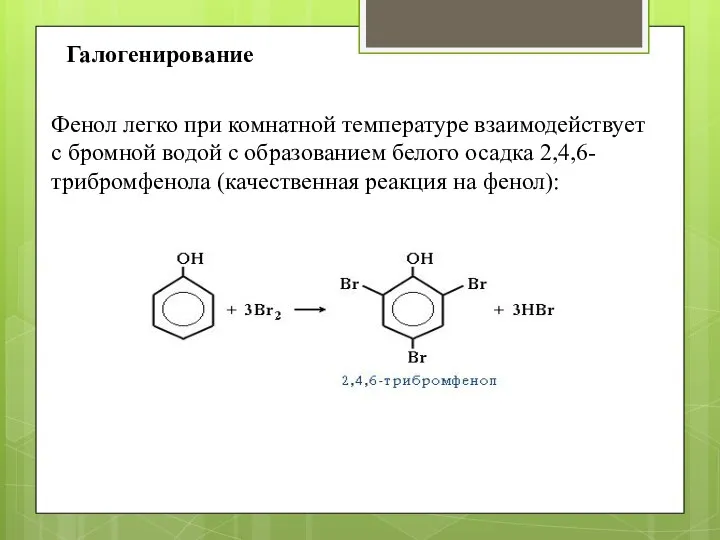
- 8. Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция
- 9. Конденсация с альдегидами 2). Гидрирование фенола C6H5-OH + 3H2 Ni, 170ºC → C6H11 – OH -
- 10. Физические свойства Большинство одноатомных фенолов при нормальных условиях представляют собой бесцветные кристаллические вещества с невысокой температурой
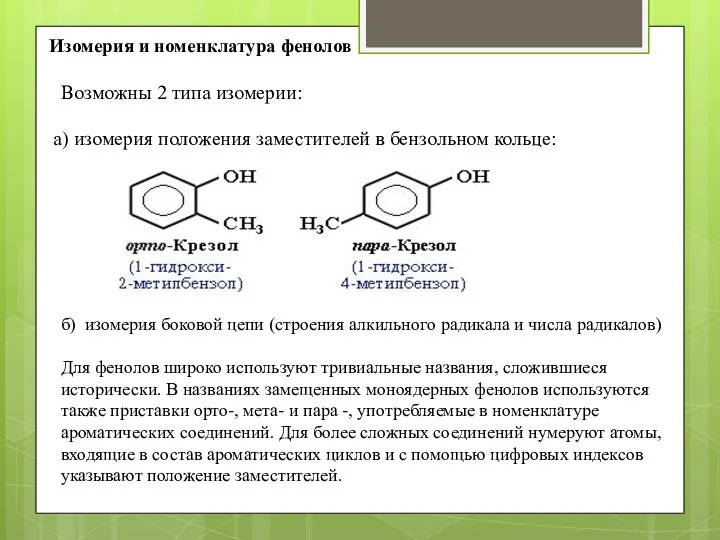
- 11. Изомерия и номенклатура фенолов Возможны 2 типа изомерии: а) изомерия положения заместителей в бензольном кольце: б)
- 12. Токсические свойства Фенол ядовит. Вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые
- 13. Применение фенолов Производство синтетических смол, пластмасс, полиамидов; 2. Лекарственных препаратов; 3. Красителей; 4. Поверхностно-активных веществ; 5.
- 14. Строение молекулы Фенильная группа C6H5 – и гидроксил –ОН взаимно влияют друг на друга Неподеленная электронная
- 16. Скачать презентацию







 Химия и косметика Подготовила: Аникина Алина 10 «А»
Химия и косметика Подготовила: Аникина Алина 10 «А»  Обобщение и систематизация знаний по теме Химическая связь и строение атома
Обобщение и систематизация знаний по теме Химическая связь и строение атома Ионообменная хроматография
Ионообменная хроматография Нуклеиновые кислоты Презентация по химии
Нуклеиновые кислоты Презентация по химии Использование химии в медицине
Использование химии в медицине Наиболее активные металлы: элементы I и II групп ПС
Наиболее активные металлы: элементы I и II групп ПС Хлористый водород
Хлористый водород Буферные системы в организме
Буферные системы в организме Основные положения технологии натрия как теплоносителя реакторов на быстрых нейтронах. Требования к качеству реакторного натрия
Основные положения технологии натрия как теплоносителя реакторов на быстрых нейтронах. Требования к качеству реакторного натрия Сульфат меди
Сульфат меди Химическое равновесие
Химическое равновесие Безазотистые вторичные метаболиты минорных групп в фармации. Биохимия, функциональное значение в царстве растений
Безазотистые вторичные метаболиты минорных групп в фармации. Биохимия, функциональное значение в царстве растений Биохимияға кіріспе. Белоктардың қызметтері. Белоктардың жіктелуі. Күрделі белоктар: хромопротеиндер, гликопротеиндер
Биохимияға кіріспе. Белоктардың қызметтері. Белоктардың жіктелуі. Күрделі белоктар: хромопротеиндер, гликопротеиндер Аминокислоты. Классификация
Аминокислоты. Классификация Массовая доля
Массовая доля Теоретические основы биоорганической химии
Теоретические основы биоорганической химии Спирты одноатомные предельные
Спирты одноатомные предельные Углеводы
Углеводы  ГБОУ СОШ № 661 Санкт-Петербург учитель химии Ефремова С.А.
ГБОУ СОШ № 661 Санкт-Петербург учитель химии Ефремова С.А.  Бетоны и железобетон (лекция 3)
Бетоны и железобетон (лекция 3) Состав, свойства и перегонка нефти. Нефтепродукты
Состав, свойства и перегонка нефти. Нефтепродукты Ситуационная задача по биохимии
Ситуационная задача по биохимии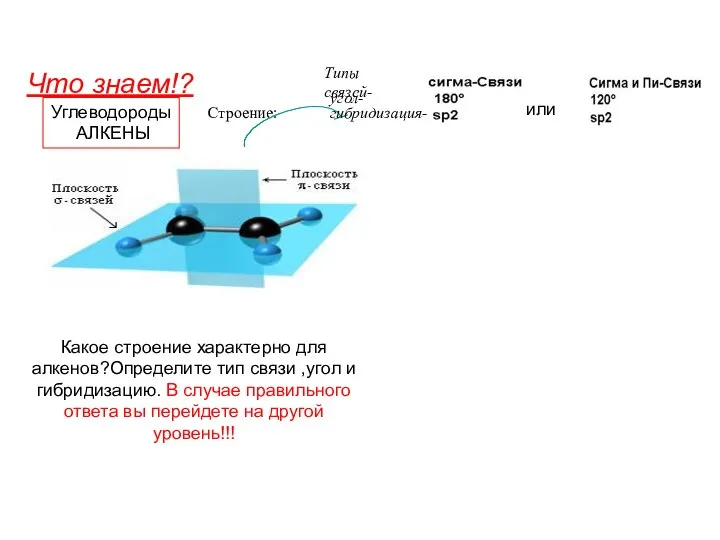 Углеводороды. Алкены
Углеводороды. Алкены L’introduction a la biochimie. La structure et les proprietes des proteines
L’introduction a la biochimie. La structure et les proprietes des proteines Непредельные углеводороды АЛКЕНЫ Алферова Мария Владимировна учитель химии ГБОУ лицей №486 Выборгского района г. Санкт-Петербу
Непредельные углеводороды АЛКЕНЫ Алферова Мария Владимировна учитель химии ГБОУ лицей №486 Выборгского района г. Санкт-Петербу Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар
Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар Окисно-відновні реакції, їхнє значення. Складання найпростіших окисно-відновних реакцій, добір коефіцієнтів
Окисно-відновні реакції, їхнє значення. Складання найпростіших окисно-відновних реакцій, добір коефіцієнтів Кристалічні та аморфні тіла. Рідкі кристали та їх властивості
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості