Содержание
- 2. Відмінність біологічних каталізаторів (ферментів) від мінеральних Надзвичайно висока ефективність дії (в дуже малих кількостях підсилюють швидкості
- 3. Будова ферментів 1) прості білки (однокомпонентні) 2) складні білки (двокомпонентні): простий білок + простетична група (апофермент)
- 4. Молекулярна маса РИБОНУКЛЕАЗА ……………....………………..……………………..13700 ТРИПСИН ………………………………………………………………23800 ГЕКСОКІНАЗА ……………………...………………….……………..45000 АЛЬДОЛАЗА ………………………………………………...………..142000 УРЕАЗА ………………………………………………………………..480000 ПІРУВАТДЕГІДРОГЕНАЗА ………..……….………………...……4500000
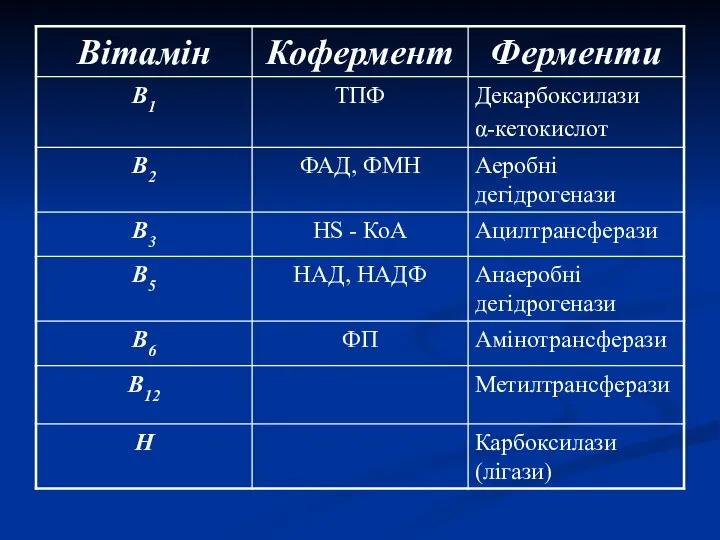
- 5. Коферменти 1. Водорозчинні вітаміни – у вигляді фосфорних ефірів (ТДФ та ФП) або в складі нуклеотидів
- 7. Центри ферментів це особливі ділянки ферментів, які формуються на рівні третинної і четвертинної структури та забезпечують
- 8. В структурі ферментів розрізняють наступні центри: 1. Активний центр, в ньому виділяють 2 ділянки, які теж
- 9. 2. Регуляторний (алостеричний) центр – це ділянка ферменту, приєднання до якого різних речовин (модифікаторів) призводить до
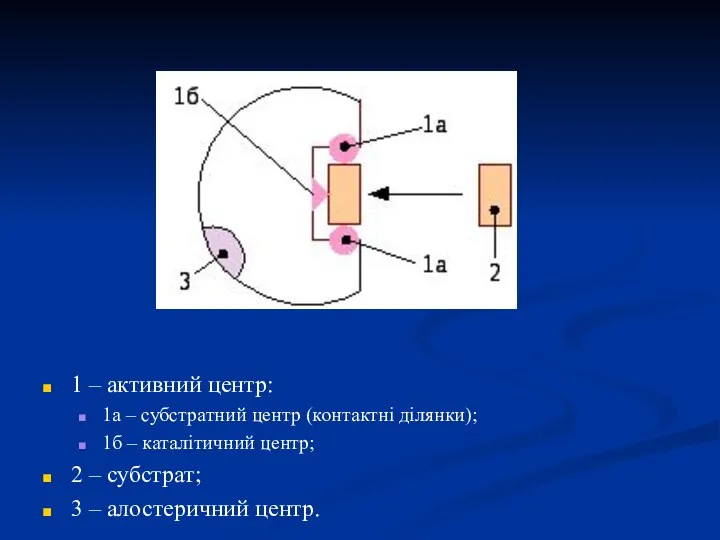
- 10. 1 – активний центр: 1а – субстратний центр (контактні ділянки); 1б – каталітичний центр; 2 –
- 11. Будова активного центру ферменту
- 12. Амінокислоти, що найчастіше входять до структури центрів Серин – ОН Треонін – ОН Тирозин – ОН
- 13. Загальні властивості ферментів 1. Термолабільність – це зміна активності ферментів при різних температурах: оптимальну активність вони
- 14. Залежність швидкості ферментативної реакції (V) від температури
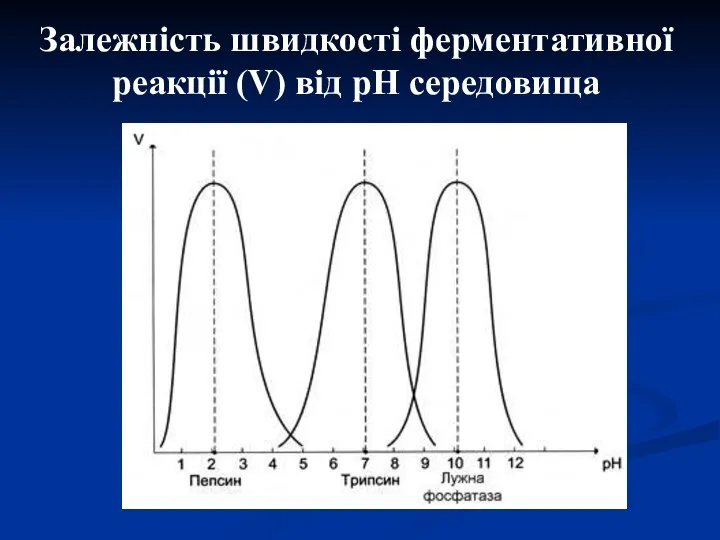
- 15. 2. Чутливість до рН середовища Більшість ферментів організму мають оптимум рН, наближений до нейтрального, хоча для
- 16. Залежність швидкості ферментативної реакції (V) від рН середовища
- 17. 3. Специфічність дії – це вибірковість дії ферментів як по відношенню до субстрату реакції, так і
- 18. 4. Зберігають активність в ізольованому вигляді, тому багато ферментів використовують як лікарські препарати. 5. Чутливість до
- 19. Механізм дії ферментів. Енергетичні зміни ПРИ ХІМІЧНИХ РЕАКЦІЯХ. Будь-які хімічні реакції перебігають згідно двох основних законів
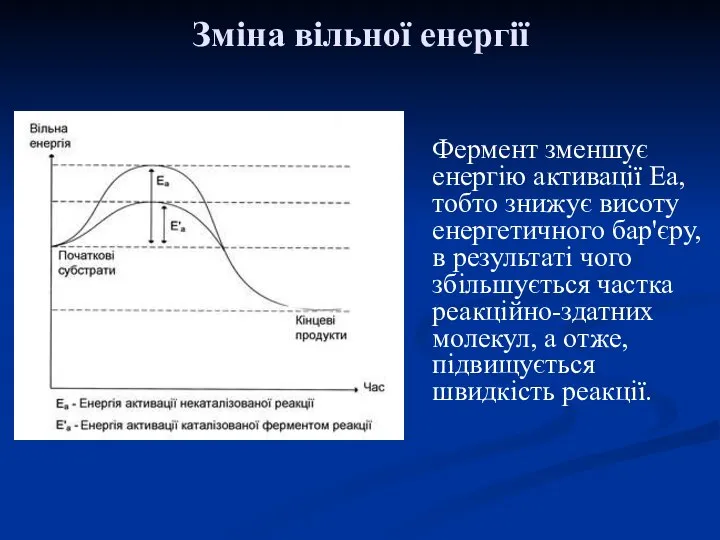
- 20. Фермент зменшує енергію активації Еа, тобто знижує висоту енергетичного бар'єру, в результаті чого збільшується частка реакційно-здатних
- 21. Зниження енергетичного бар'єру відбувається за рахунок: 1. Підвищення ймовірності зіткнення субстратів. 2. Чіткої орієнтації взаємодій молекул
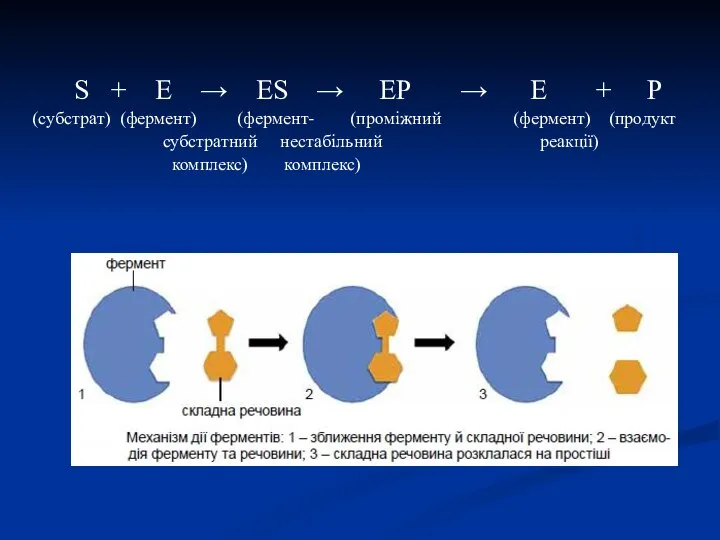
- 22. Механізм ферментативного каталізу (теорія нестійких фермент-субстратних комплексів) В механізмі ферментативного каталізу вирішальне значення має утворення нестійких
- 23. S + E → ES → EP → E + P (cубстрат) (фермент) (фермент- (проміжний (фермент)
- 24. Ефект деформації Активний центр ферменту також сприяє дестабілізації міжатомних зв'язків в молекулі субстрату, що полегшує перебіг
- 25. Етапи ферментативного каталізу I - етап зближення та орієнтації субстрату відносно активного центру ферменту; II -
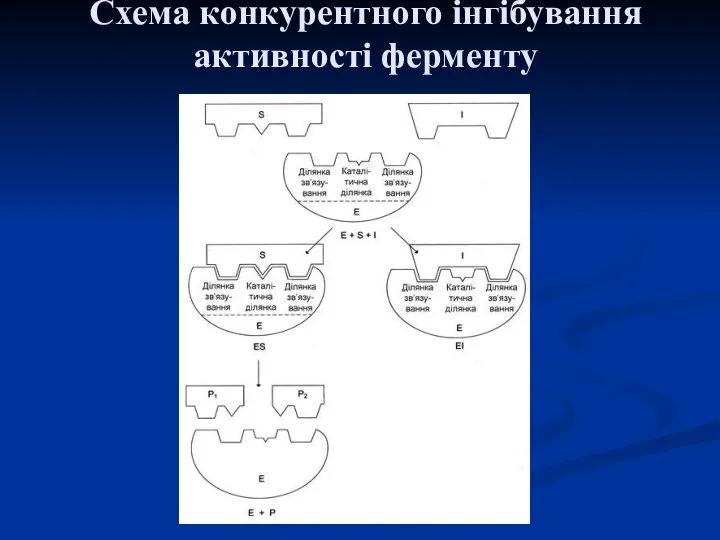
- 26. Конкурентна і неконкурентна дія інгібіторів Конкурентна дія інгібітора буває в тому випадку, коли його хімічна будова
- 27. Схема конкурентного інгібування активності ферменту
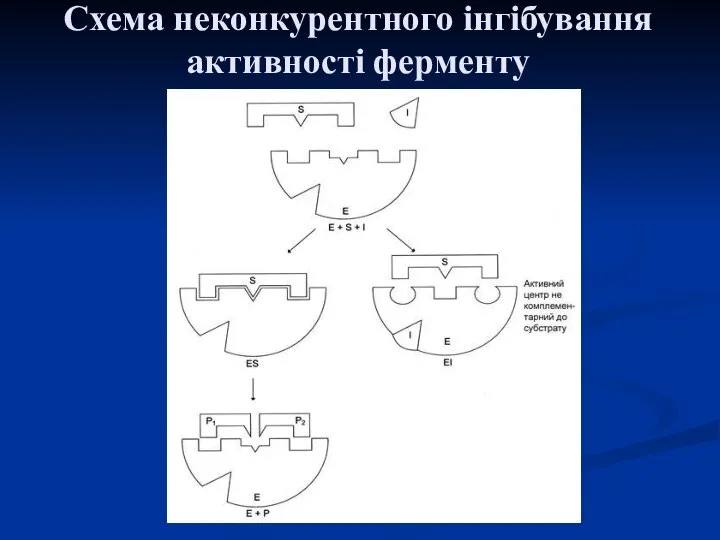
- 28. За неконкурентного інгібування інгібітор приєднується до алостеричного центру, в результаті чого змінюється конформація активного центру та
- 29. Схема неконкурентного інгібування активності ферменту
- 30. Ферментні ансамблі або мультиферменти – комплекс ферментів, які каталізують послідовні реакції при перетворенні однієї речовини.
- 31. ІЗОФЕРМЕНТИ Це множинні молекулярні форми, що мають єдину субстратну специфічність (фактично це один і той самий
- 32. Множинні ізоформи ЛДГ А – будова різних ізоформ ЛДГ (субодиниці типу Н і типу М); Б
- 33. Активність ферментів визначають опосередковано: за кількістю продукту, що утворився (Р), за кількістю спожитого субстрату (S). Міжнародна
- 34. Для оцінки кількості молекул ферменту серед інших білків досліджуваної тканини визначають питому активність (пит. ак.) ферменту,
- 35. Каталітична ефективність Кількість молекул субстрату, які перетворюються в продукт однією молекулою ферменту за 1 с, називають
- 36. Номенклатура ферментів Тривіальна (пепсин, трипсин, хімотрипсин); Назва субстрату (латинська або інша) + закінчення –аза: амілаза (amilum
- 37. Наукова назва: за допомогою цифр: - перша цифра – це номер класу; - друга цифра –
- 38. КЛАСИФІКАЦІЯ ФЕРМЕНТІВ Всі ферменти за механізмом дії розділені на 6 основних класів: Оксидоредуктази 4. Ліази Трансферази
- 39. Оксидоредуктази Ферменти цього класу каталізують окисно-відновні реакції, які лежать в основі забезпечення тканин необхідною енергією. Оксидоредуктази
- 40. Дегідрогенази: а) піридинзалежні (анаеробні), б) флавінзалежні (аеробні). Цитохроми: а) сімейство а (а1, а2, a3,…); б) сімейство
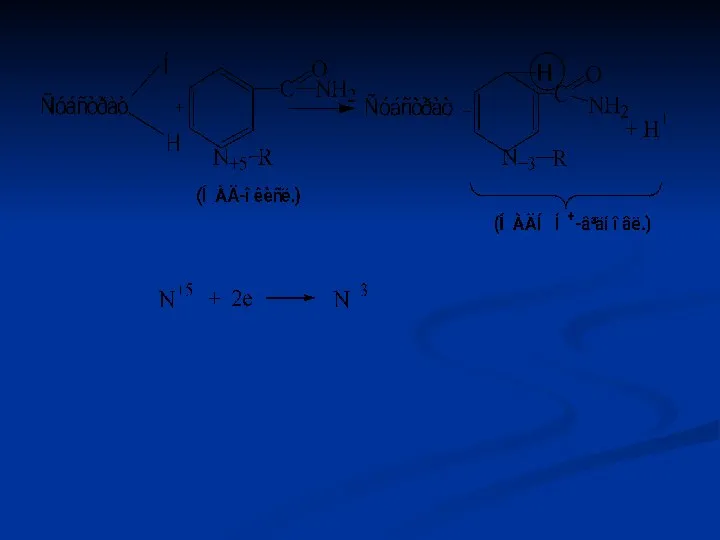
- 41. Піридинзалежні дегідрогенази (двохкомпонентні) Специфічний білок (апофермент) + кофермент НАД або НАДФ. Механізм дії:
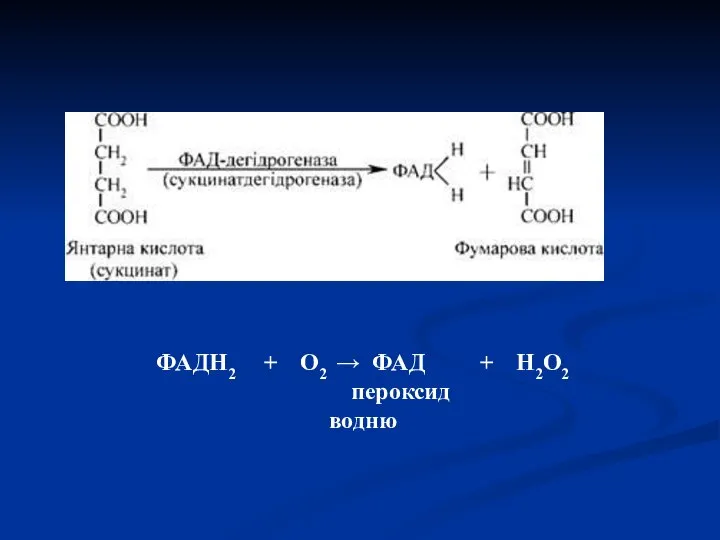
- 44. Флавінзалежні дегідрогенази (двохкомпонентні) Специфічний білок (апофермент) + кофермент ФМН або ФАД. Механізм дії:
- 45. ФАДН2 + О2 → ФАД + Н2О2 пероксид водню
- 47. Цитохроми За хімічною природою відносяться до хромопротеїнів (гемовмісних). Їх простетичною групою (коферментом) є гем, атом заліза
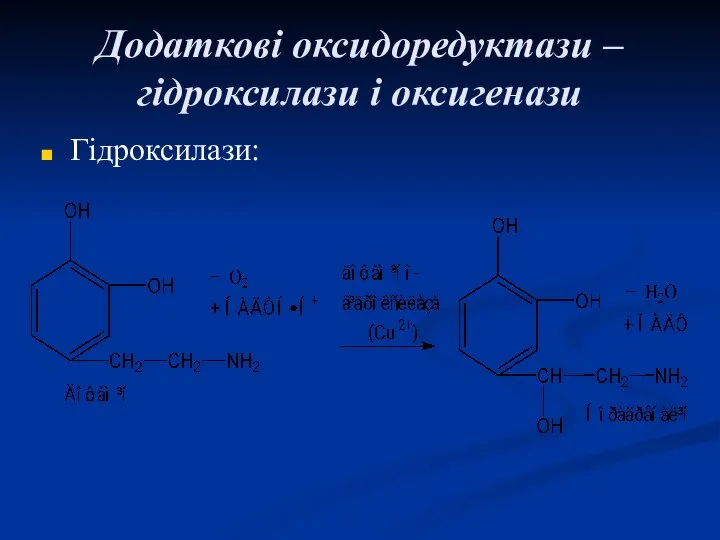
- 48. Додаткові оксидоредуктази – гідроксилази і оксигенази Гідроксилази:
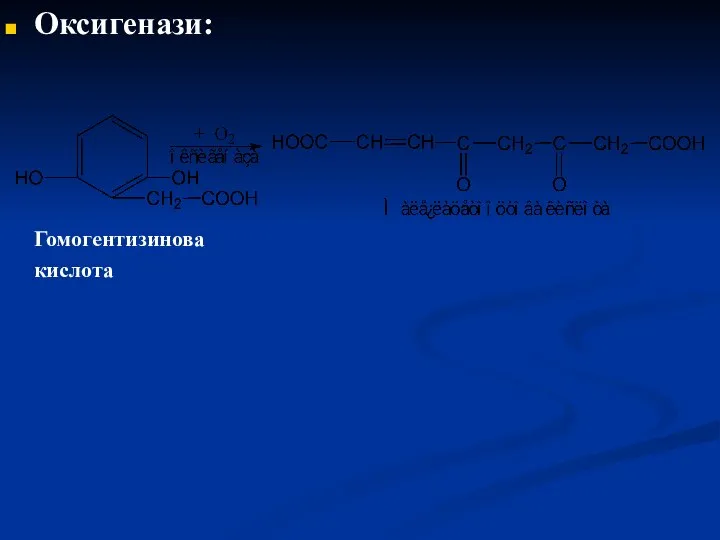
- 49. Оксигенази: Гомогентизинова кислота
- 50. Допоміжні оксидоредуктази Каталаза: Пероксидаза:
- 51. Трансферази Амінотрансферази (апофермент + ФП), Ацилтрансферази (апофермент + НS-КоА), Метилтрансферази (апофермент + В12), Формілтрансферази (апофермент +
- 52. Амінотрансферази (двохкомпонентні) Склад: специфічний білок + фосфопіридоксаль (ФП), тобто фосфорильований вітамін В6. α
- 53. Ацилтрансферази (двохкомпонентні) Склад: специфічний білок (апофермент) + НS-коензимА (містить вітамін В3)
- 54. Метилтрансферази (двохкомпонентні) Склад: специфічний білок (апофермент) + вітамін В12 та Вс
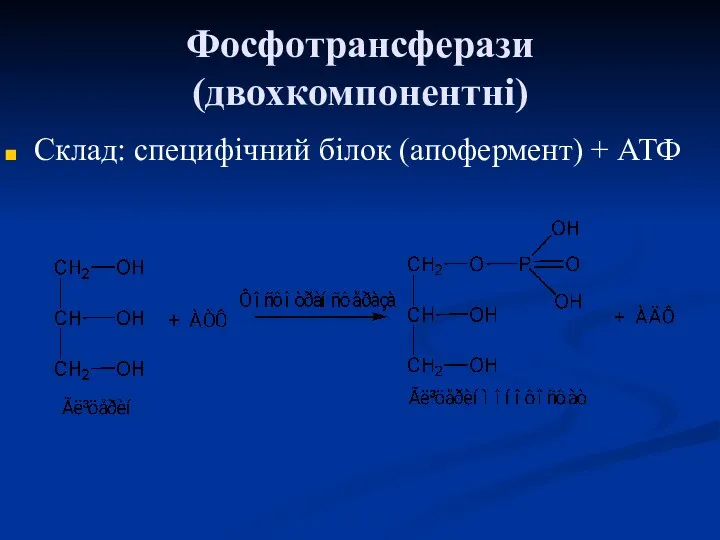
- 55. Фосфотрансферази (двохкомпонентні) Склад: специфічний білок (апофермент) + АТФ
- 56. Гідролази (однокомпонентні) Каталізують розрив хімічних зв'язків в молекулах складних речовин шляхом приєднання води. Найбільш часто гідролази
- 57. Підкласи пептидази, глікозидази, естерази, тіолази, амідази та ін.
- 58. Пептидази Прискорюють гідроліз пептидних зв'язків в молекулах білків і поліпептидів:
- 59. Ендопептидази Ендопептидази гідролізують пептидні зв'язки в середині поліпептидного ланцюга та розщеплюють її на декілька більш коротких
- 60. Екзопептидази При дії цих ферментів від поліпептидного ланцюга відщеплюються окремі амінокислоти, тобто екзопептидази гідролізують кінцеві пептидні
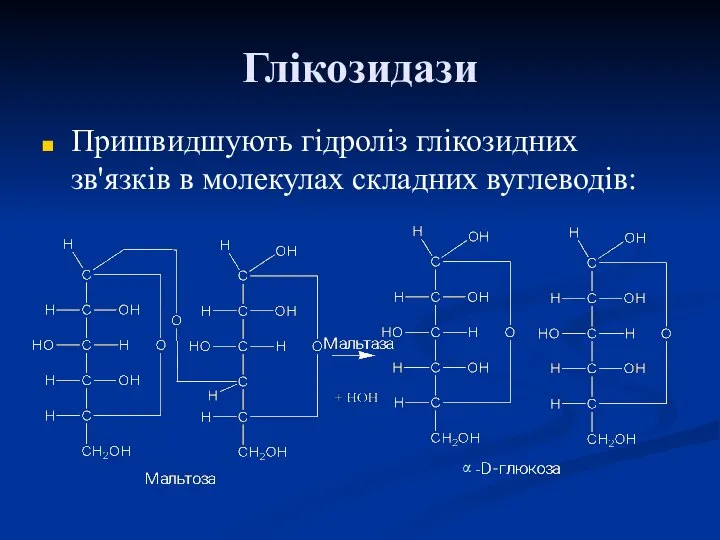
- 62. Глікозидази Пришвидшують гідроліз глікозидних зв'язків в молекулах складних вуглеводів: α
- 64. Естерази Прискорюють гідроліз різних складних ефірів. Залежно від кислоти, що бере участь в утворенні складно-ефірного зв'язку,
- 65. Фосфоестерази
- 66. Ліази Це ферменти, які можуть обернено приєднувати або відщепляти атомні групи по подвійним зв'язкам. По своїй
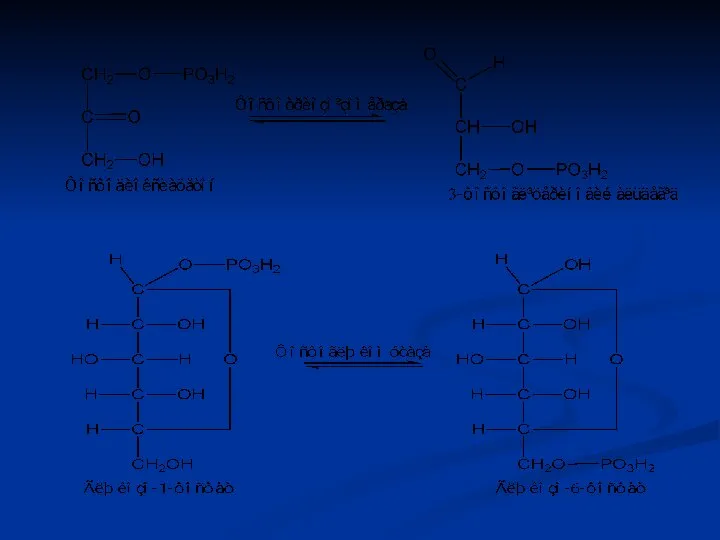
- 69. Ізомерази Ферменти цього класу каталізують реакції ізомерних перебудов невеликих молекул, а також реакції перенесення окремих груп
- 71. Лігази (синтетази) Каталізують синтез органічних речовин з двох більш простих молекул. При цьому обов'язково використовується енергія
- 73. Скачать презентацию
























































 Ферменты и гормоны Урок химии в 10 (11) классе Автор: учитель химии Ким Н.В. МОУ СОШ №6 г. Нягани ХМАО-Югры Тюменской области
Ферменты и гормоны Урок химии в 10 (11) классе Автор: учитель химии Ким Н.В. МОУ СОШ №6 г. Нягани ХМАО-Югры Тюменской области Квалификация химических реактивов, принятая в РФ
Квалификация химических реактивов, принятая в РФ Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша)
Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша) Получение, собирание и распознавание водорода
Получение, собирание и распознавание водорода Розчини
Розчини Зелёные камни
Зелёные камни Гормоны. Виды и классификация гормонов
Гормоны. Виды и классификация гормонов Анодные реакции коррозионного процесса
Анодные реакции коррозионного процесса Электрохимические процессы
Электрохимические процессы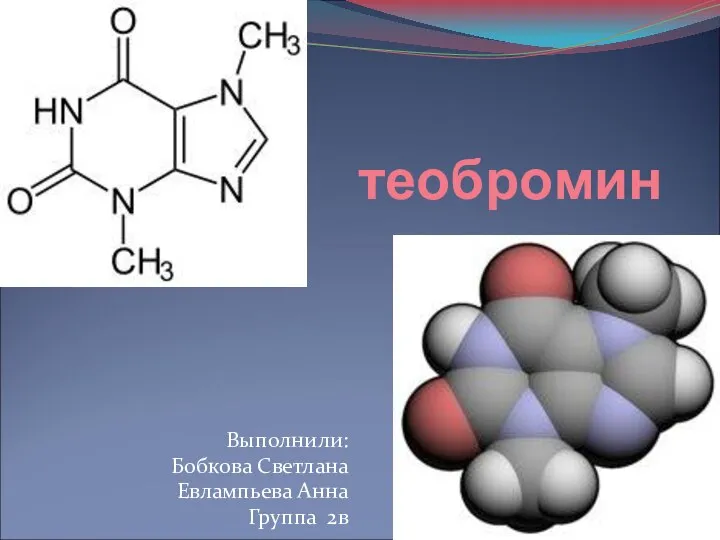 Теобромин
Теобромин Карбо́новые кисло́ты
Карбо́новые кисло́ты Строение атома
Строение атома Смесители. Пропеллерная мешалка
Смесители. Пропеллерная мешалка Презентация по Химии "Применение электролиза" - скачать смотреть
Презентация по Химии "Применение электролиза" - скачать смотреть  Перевариваемые полисахариды злаковых, бобовых, овощей, ягод и фруктов. Крахмал (амилоза, амилопектин), фруктаны (инулин)
Перевариваемые полисахариды злаковых, бобовых, овощей, ягод и фруктов. Крахмал (амилоза, амилопектин), фруктаны (инулин) Р-элементы IV группы: C, Si, Ge, Sn, Pb
Р-элементы IV группы: C, Si, Ge, Sn, Pb Задача №9. Глицерин. Команда Карбораны
Задача №9. Глицерин. Команда Карбораны ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств
ОКИСЛИТЕЛЬНО – ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Элективный специальный курс углублённого изучения темы для учащихся 11 классов естеств Презентация по Химии "Насичені одноатомні спирти" - скачать смотреть бесплатно
Презентация по Химии "Насичені одноатомні спирти" - скачать смотреть бесплатно К 180-летию со дня рождения Д.И. Менделеева
К 180-летию со дня рождения Д.И. Менделеева Пегматитовые месторождения
Пегматитовые месторождения Chemical bonding and Molecular Structure
Chemical bonding and Molecular Structure Обобщающий урок –игра Звездный час по теме Подгруппа кислорода
Обобщающий урок –игра Звездный час по теме Подгруппа кислорода Распределение примесей в процессе выращивания мультикристаллического кремния
Распределение примесей в процессе выращивания мультикристаллического кремния Комплексные соединения
Комплексные соединения Типы химических реакций на примере свойств воды
Типы химических реакций на примере свойств воды  Алкилирование изобутана олефинами
Алкилирование изобутана олефинами Гигиенические нормативы. Химические факторы окружающей среды
Гигиенические нормативы. Химические факторы окружающей среды