Содержание
- 2. 1 СВОЙСТВО: ВЗАИМОДЕЙСТВИЕ СО ЩЕЛОЧНЫМИ МЕТАЛЛАМИ Этиленгликоль при этом образует однозамещённый гликолят 2HO—CH2—CH2—OH + 2Na →
- 3. 2 СВОЙСТВО: ВЗАИМОДЕЙСТВИЕ С РАСТВОРАМИ ЩЕЛОЧЕЙ CH2-OH CH2-O-Na │ │ CH -OH + NaOH → CH
- 4. 4 СВОЙСТВО: ОБРАЗОВАНИЕ СЛОЖНЫХ ЭФИРОВ ПРИ ВЗАИМОДЕЙСТВИИ С КИСЛОТАМИ CH2-OH О CH2-OH О │ + ║
- 5. НИТРОГЛИЦЕРИН, ИЛИ ТРИНИТРАТ ГЛИЦЕРИНА, ИЛИ ТРИНИТРОГЛИЦЕРИД (НИТРОГЛИЦЕРИН) CH2- O - H + Н - О -
- 6. 5 СВОЙСТВО: РЕАКЦИИ ДЕГИДРАТАЦИИ А) внутримолекулярная дегидратация О ║ СН2 – СН – ОН → [Н2С
- 7. МЕЖМОЛЕКУЛЯРНАЯ ДЕГИДРАТАЦИЯ СН2 – СН2 – О – Н + Н – О – СН2 –
- 8. 6 СВОЙСТВО: ВЗАИМОДЕЙСТВИЕ С ГАЛОГЕНОВОДОРОДАМИ СН2 – О – Н СН2 – Br СН2 – Br
- 9. ДОМАШНЕЕ ЗАДАНИЕ Записать уравнение реакции горения: 1 вариант – этиленгликоля; 2 вариант – глицерина Записать уравнение
- 11. Скачать презентацию








 Термодинамическое равновесие
Термодинамическое равновесие Оксид металлов
Оксид металлов Легированные конструкционные стали. Инструментальные легированные стали
Легированные конструкционные стали. Инструментальные легированные стали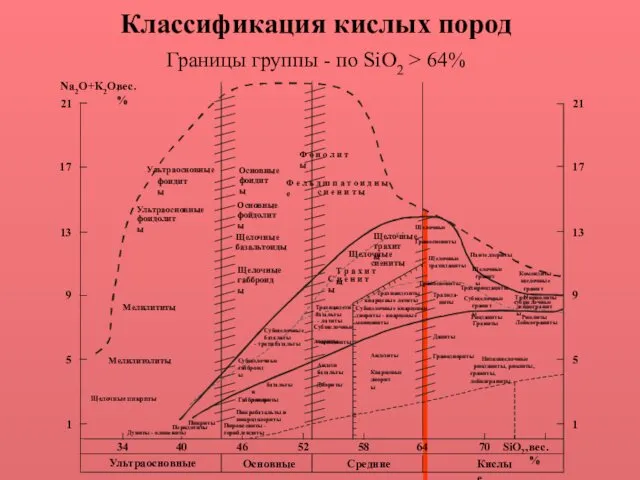 Классификация кислых пород
Классификация кислых пород Хімія та побут
Хімія та побут Биогенные элементы. Классификация. Топография биогенных элементов в организме человека
Биогенные элементы. Классификация. Топография биогенных элементов в организме человека Методы разделения и очистки биомолекул. Ультрацентрифугирование (седиментация)
Методы разделения и очистки биомолекул. Ультрацентрифугирование (седиментация) Презентация по Химии "Способы получения металлов" - скачать смотреть
Презентация по Химии "Способы получения металлов" - скачать смотреть  Аміак
Аміак  Анионно-координационная полимеризация
Анионно-координационная полимеризация Металл серебро
Металл серебро Растворы неэлектролитов и электролитов
Растворы неэлектролитов и электролитов Organic molecules
Organic molecules Атоми і хімічні елементи. Молекули, їх рух. Дифузія
Атоми і хімічні елементи. Молекули, їх рух. Дифузія Технология производства простых полиэфиров
Технология производства простых полиэфиров Литье под давлением реактопластов
Литье под давлением реактопластов Химия функциональных материалов. Адсорбционные материалы. Цеолиты
Химия функциональных материалов. Адсорбционные материалы. Цеолиты Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно
Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно Физиологические эффекты активных форм кислорода
Физиологические эффекты активных форм кислорода Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра
Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Электродные потенциалы. Гальванические элементы. ЭДС
Электродные потенциалы. Гальванические элементы. ЭДС Межмолекулярные силы (силы Ван дер Ваальса)
Межмолекулярные силы (силы Ван дер Ваальса) Углеводы. Глюкоза. ЗНАНИЯ, НЕПРОВЕРЕННЫЕ ОПЫТОМ, МАТЕРЬЮ ВСЯКОЙ ДОСТОВЕРНОСТИ, БЕСПЛОДНЫ И ПОЛНЫ ОШИБОК ЛЕОНАРДО ДА ВИНЧИ
Углеводы. Глюкоза. ЗНАНИЯ, НЕПРОВЕРЕННЫЕ ОПЫТОМ, МАТЕРЬЮ ВСЯКОЙ ДОСТОВЕРНОСТИ, БЕСПЛОДНЫ И ПОЛНЫ ОШИБОК ЛЕОНАРДО ДА ВИНЧИ  Метаморфизм
Метаморфизм Катаболизм фенилаланина, тирозина
Катаболизм фенилаланина, тирозина Живая и мертвая вода
Живая и мертвая вода Главная подгруппа V группы..Азот
Главная подгруппа V группы..Азот