Содержание
- 2. План лекции. Скорость химической реакции. Закон действия масс. Правило Вант-Гоффа. Катализаторы. Биокатализаторы. Химическое равновесие с точки
- 3. 1. Скорость химической реакции. Закон действия масс. Скорость химической реакции (V)- это изменение концентрации реагирующих веществ
- 4. 2. Правило Вант – Гоффа. Зависимость скорости реакции от температуры. Закон Вант-Гоффа: При повышении температуры на
- 5. 3. Катализаторы. Биокатализаторы. Катализаторы – это вещества, которые изменяют скорость реакции, но сами в реакции не
- 6. 4. Химическое равновесие с точки зрения кинетики Обратимыми называются реакции, протекающие в двух противоположных направлениях. Самым
- 7. 5. Химическое равновесие с точки зрения термодинамики. На протекание химической реакции влияют 2 фактора: энтальпийный (ΔH)
- 8. 6. Смещение химического равновесия На состояние химического равновесия влияет температура(t), давление(p) и концентрация веществ (C). Предсказать
- 9. Ле Шателье
- 10. Карл Фердинанд Браун Изобретатель кинескопа (катодно-лучевой трубки). В немецкоговорящих странах кинескоп до сих пор называют трубкой
- 11. Принцип Брауна Если на систему, находящуюся в химическом равновесии оказано воздействие извне, то она оказывает противодействие.
- 13. Скачать презентацию










 Анализ красителей и консервантов, входящих в состав безалкогольных газированных и негазированных напитков
Анализ красителей и консервантов, входящих в состав безалкогольных газированных и негазированных напитков Презентация по Химии "Предмет химии" - скачать смотреть
Презентация по Химии "Предмет химии" - скачать смотреть  Степень окисления. Составление формул бинарных соединений
Степень окисления. Составление формул бинарных соединений Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних
Циклічна обернено-похідна хронопотенціометрія пірокатехіну та його похідних Галогенидные и полигалогенидные комплексы постпереходных элементов
Галогенидные и полигалогенидные комплексы постпереходных элементов Электродные процессы, их биологическая роль и применение в медицине
Электродные процессы, их биологическая роль и применение в медицине Взаимодействие солей аммония со щелочами
Взаимодействие солей аммония со щелочами Алканы. Получение и применение алканов
Алканы. Получение и применение алканов Алкины
Алкины Химическая связь
Химическая связь Презентация по Химии "Штучні волокна" - скачать смотреть бесплатно
Презентация по Химии "Штучні волокна" - скачать смотреть бесплатно Пептиды. Белки
Пептиды. Белки Эмульсии и эмульгаторы
Эмульсии и эмульгаторы Сполуки фосфору
Сполуки фосфору Навчальний проект «Дослідження зміни концентрації CO2 у класній кімнаті під час занять»
Навчальний проект «Дослідження зміни концентрації CO2 у класній кімнаті під час занять» Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение
Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение Витамины и авитаминоз - презентация_
Витамины и авитаминоз - презентация_ Железо. Строение атома, физические и химические свойства простого вещества
Железо. Строение атома, физические и химические свойства простого вещества Электродные материалы для электрохимических систем
Электродные материалы для электрохимических систем Комплексті қосылыстар
Комплексті қосылыстар Абсолютное первенство по химии
Абсолютное первенство по химии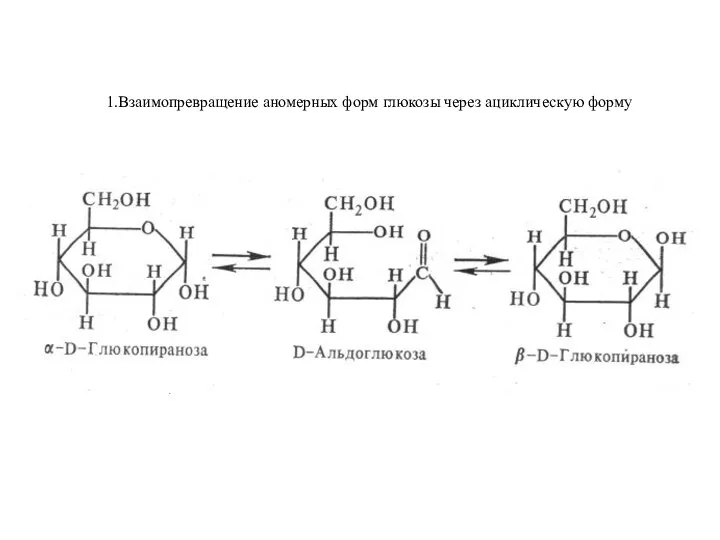 Взаимопревращение аномерных форм глюкозы через ациклическую форму
Взаимопревращение аномерных форм глюкозы через ациклическую форму Биологически важные ароматические и гетероциклические соединения
Биологически важные ароматические и гетероциклические соединения Химическая связь
Химическая связь Полимерные материалы и изделия
Полимерные материалы и изделия Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов. (Лекция 8)
Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов. (Лекция 8) Хром и его соединения
Хром и его соединения Липиды. Классификация
Липиды. Классификация