Содержание
- 2. Электролитическая теория первая научная ионная теория кислот и оснований (Оствальд, Аррениус, 1890 год). Согласно этой теории,
- 3. Амфотерность А. Ганч в 1917-1927 годах ввел понятие об амфотерности - способности некоторых соединений проявлять как
- 4. Теории кислот и оснований протолитическая (И. Бренстед и Т. Лоури) и электронная (Г. Льюис) теории кислот
- 5. В протолитической теории Вода принята за своеобразный стандарт для оценки кислотно-основных свойств веществ - стандарт нейтральной
- 6. Почему вода? Вода - одно из самых распространенных на Земле соединений. Ее кислотно-основные свойства определяют естественный
- 7. Количественная мера кислотности и основности Кислотность соединений количественно оценивается долей ионизированной формы вещества в растворе (воде)
- 8. Принцип ЖМКО Пирсона (1963) Кислоты и основания Льюиса делятся на жёсткие и мягкие, причём мягкие кислоты
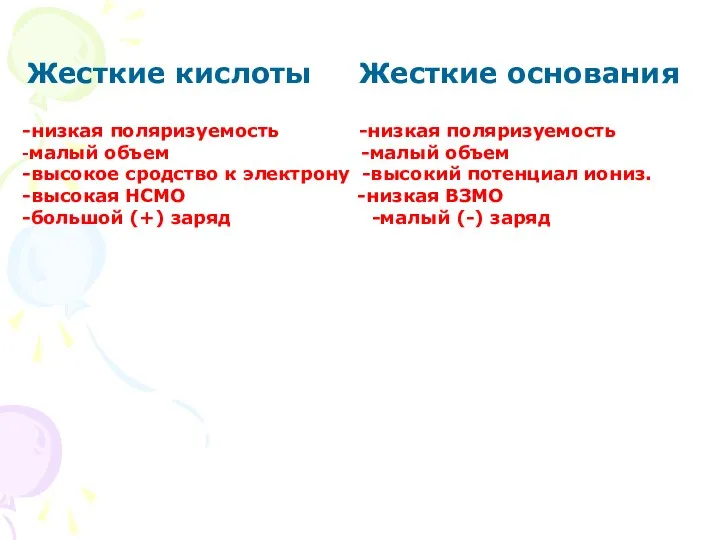
- 9. Жесткие кислоты Жесткие основания -низкая поляризуемость -низкая поляризуемость -малый объем -малый объем -высокое сродство к электрону
- 10. Мягкие кислоты Мягкие основания -высокая поляризуемость -высокая поляризуемость -большой объем -большой объем -низкая НСМО -высокая ВЗМО
- 11. Классификация кислот и оснований в рамках принципа ЖМКО
- 12. Помимо условного деления на три типа, можно также проследить зависимость жёсткости или мягкости в рядах отдельных
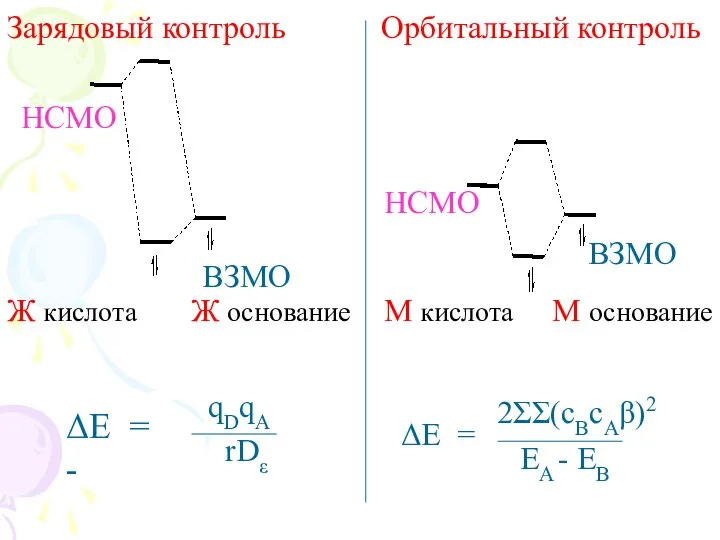
- 13. Ж. кис.+ Ж. осн. = Зарядовый контроль Высоколежащая НСМО к-ты + низколежащая ВЗМО осн-я. Определяющая роль
- 14. Зарядовый контроль Орбитальный контроль ВЗМО НСМО НСМО ВЗМО ΔE = - qDqA rDε ΔE = 2ΣΣ(cBcAβ)2
- 15. Применение в органической химии В органической химии принцип ЖМКО широко применяется для предсказания или объяснения протекания
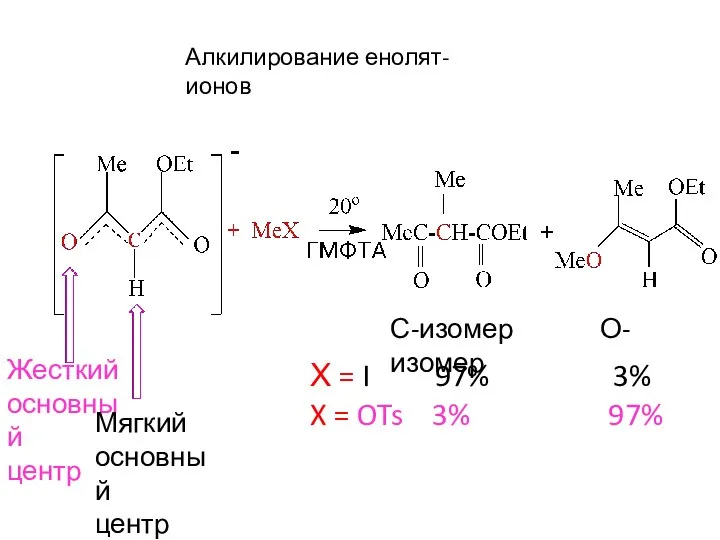
- 16. Принцип Пирсона также полезен для предсказания реакционной способности соединений с двумя реакционными центрами, например, енолят-ионов или
- 17. Алкилирование енолят-ионов С-изомер О-изомер Х = I 97% 3% X = OTs 3% 97% Жесткий основный
- 18. Амбидентные субстраты и реагенты -0.31 +0.09 -0.79 S - C = N MО ЖО Пример: S=C=N-
- 19. Амбидентность нитрит – иона O- – N = O ЖО МО С8H17Br + AgNO2 → C8H17O-N=O
- 20. Амбидентность енолят-аниона (С2H5)3OF (фторид триэтилоксония) – очень жесткий реагент – алкилирует енолят –анион по атому О
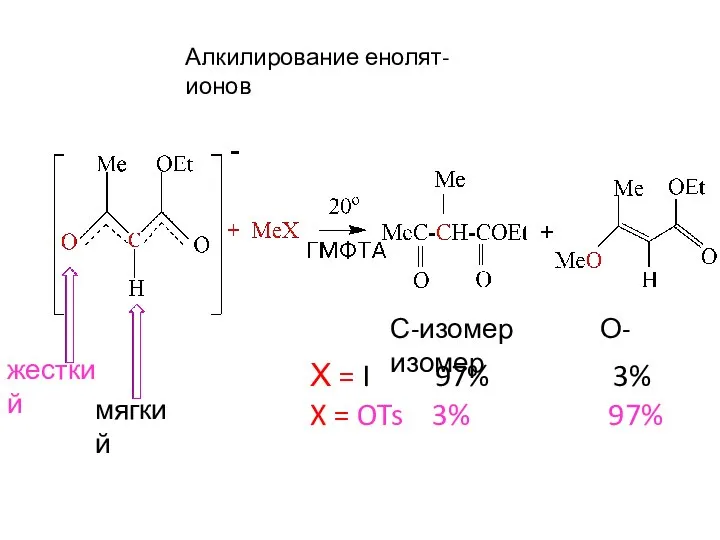
- 21. Алкилирование енолят-ионов С-изомер О-изомер Х = I 97% 3% X = OTs 3% 97% жесткий мягкий
- 23. Скачать презентацию
















 Строение, получение и применение полимеров
Строение, получение и применение полимеров Презентация Нефть и способы ее переработки
Презентация Нефть и способы ее переработки Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные
Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные Аттестаионная работа. Сахар. Изучаем и исследуем
Аттестаионная работа. Сахар. Изучаем и исследуем Химический состав клетки. Неорганические вещества клетки
Химический состав клетки. Неорганические вещества клетки Презентация по Химии "Химическое загрязнение среды промышленностью." - скачать смотреть бесплатно
Презентация по Химии "Химическое загрязнение среды промышленностью." - скачать смотреть бесплатно Презентация по Химии "Косметичні засоби" - скачать смотреть бесплатно
Презентация по Химии "Косметичні засоби" - скачать смотреть бесплатно Влияние шампуня на состояние волос человека
Влияние шампуня на состояние волос человека Презентация по Химии "Комплексные соединения" - скачать смотреть
Презентация по Химии "Комплексные соединения" - скачать смотреть  Аналитическая химия и химический анализ. (Лекция 1)
Аналитическая химия и химический анализ. (Лекция 1) Углеводы. Моносахариды. Лекция 5
Углеводы. Моносахариды. Лекция 5 Гетерогенные и лигандообменные равновесия и процессы
Гетерогенные и лигандообменные равновесия и процессы Детонаційна стійкість бензину
Детонаційна стійкість бензину Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола
Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола Энергетика химических процессов. Энтропия и энергия Гиббса
Энергетика химических процессов. Энтропия и энергия Гиббса Химитариум. Погрузись в мир занимательной химии
Химитариум. Погрузись в мир занимательной химии Роль минеральных веществ в организме человека
Роль минеральных веществ в организме человека Поверхностные явлении и дисперсные системы (коллоидная химия)
Поверхностные явлении и дисперсные системы (коллоидная химия) Производство топлив и масел
Производство топлив и масел Полимеры, пластмассы и товары на их основе
Полимеры, пластмассы и товары на их основе Альдегиды и кетоны
Альдегиды и кетоны Физико-химическая и механическая миграция
Физико-химическая и механическая миграция Свойства снега и льда (окружающий мир, 3 класс)
Свойства снега и льда (окружающий мир, 3 класс) Роль воды в жизни и хозяйстве
Роль воды в жизни и хозяйстве Магнитті қатты материалдар және оны техникада қолдану әдістері
Магнитті қатты материалдар және оны техникада қолдану әдістері Презентация Угольная кислота
Презентация Угольная кислота Кальцій і Магній
Кальцій і Магній  Фотометрический анализ III курс, д/о Преподаватель Ельчищева Юлия Борисовна
Фотометрический анализ III курс, д/о Преподаватель Ельчищева Юлия Борисовна