Содержание
- 2. Дихромат калия K2Cr2O7 Дихромат калия K2Cr2O7 Оксид никеля (II) NiO Оксид магния MgO Магний Золото Медь
- 3. Химическая связь - взаимодействие между атомами, приводящее к образованию устойчивой системы - молекулы, иона, кристалла Л.
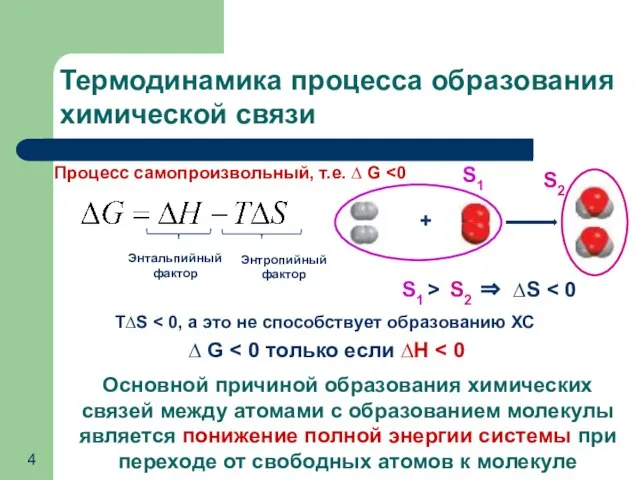
- 4. Термодинамика процесса образования химической связи Процесс самопроизвольный, т.е. ∆ G S1 > S2 ⇒ ∆S Т∆S
- 5. Изменение потенциальной энергии в системе из двух атомов водорода в зависимости от расстояния между ядрами атомов
- 6. Правило октета
- 7. Образование химической связи разных типов: модели Передача электронов Обмен электронами Объединение электронов Ионная Ковалентная Металлическая Металл/неметалл
- 8. Ионная связь: Энергия кристаллической решетки Энергия кристаллической решетки – энергия, необходимая для превращения 1 моль твердого
- 9. Hard, rigid solids at room temperature High melting point Dissolve in polar solvents (if soluble) Solutions
- 10. Ковалентная связь Атомы, образующие ковалентную связь, обобществляют электроны Каждая ковалентная связь образуется 2 общими электронами В
- 11. Механизмы образования ковалентной связи Обменный Донорно-акцепторный
- 12. Характеристики ковалентной связи 1) Длина связи – расстояние между центрами связанных атомов 2) Валентный угол –
- 13. Ковалентная связь: энергия связи versus длина связи
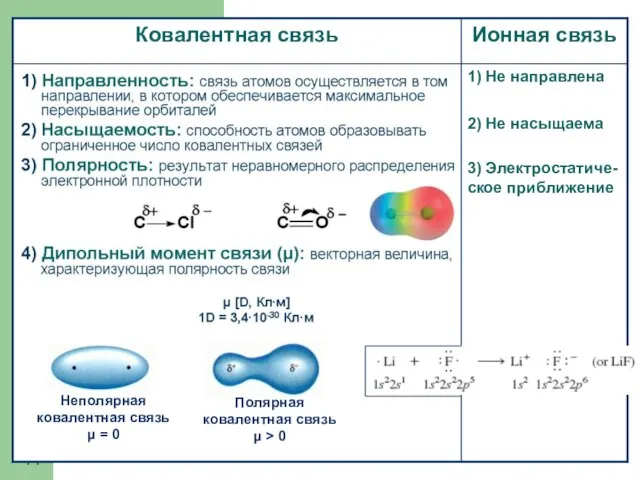
- 14. 1) Не направлена 2) Не насыщаема 3) Электростатиче-ское приближение
- 15. Степень ионности Разность электроотрицательностей Степень ионности
- 16. Резюме
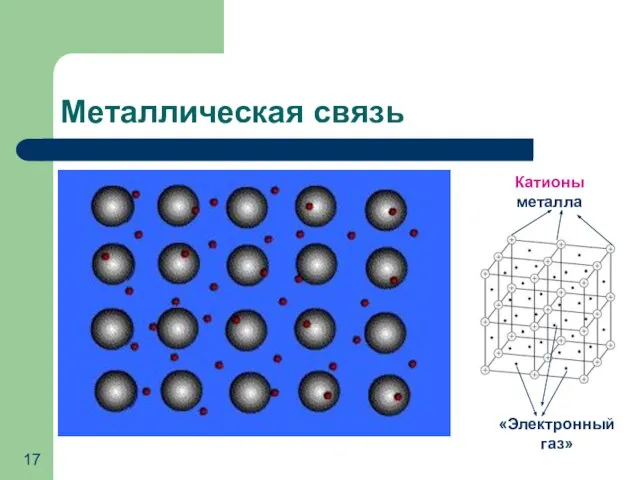
- 17. Металлическая связь Катионы металла «Электронный газ»
- 18. У d-элементов лишь небольшая часть валентных электронов делокализована по всему кристаллу. Остальные d-электроны участвуют в образовании
- 19. Межмолекулярные взаимодействия Водородная связь Слабые межмолекулярные взаимодействия (силы Ван-дер-Ваальса) Диполь-дипольные Ион-дипольные Дисперсионные
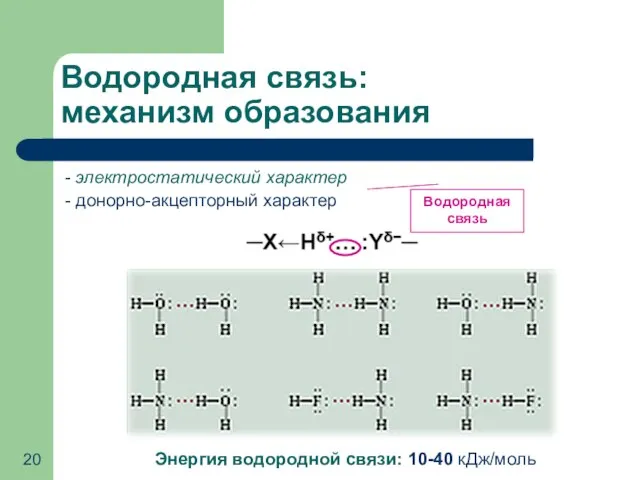
- 20. Водородная связь: механизм образования - электростатический характер - донорно-акцепторный характер Энергия водородной связи: 10-40 кДж/моль Водородная
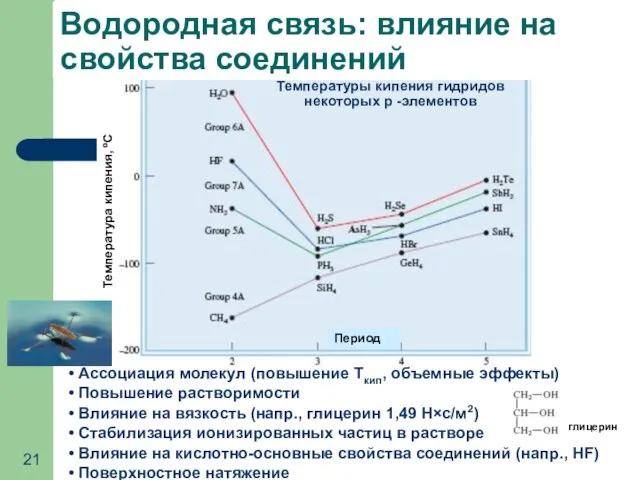
- 21. Ассоциация молекул (повышение Ткип, объемные эффекты) Повышение растворимости Влияние на вязкость (напр., глицерин 1,49 Н×с/м2) Стабилизация
- 22. Водородная связь: влияние на свойства воды Лед/вода С6Н6(тв.)/С6Н6(ж.) Температура, ºС Плотность, г/мл Четыре водородные связи Максимальная
- 23. Ориентационные силы, диполь-дипольное притяжение Осуществляется между молекулами, являющимися постоянными диполями E ~ 1/r3 Дисперсионное притяжение (лондоновские
- 25. Скачать презентацию

















 Презентация по Химии "Твердые вещества" - скачать смотреть
Презентация по Химии "Твердые вещества" - скачать смотреть  Основания, их состав, номенклатура и основные представители
Основания, их состав, номенклатура и основные представители Композитный материал
Композитный материал Формы кристаллов и агрегаты
Формы кристаллов и агрегаты Обмен простых белков. Дезаминирование и трансаминирование аминокислот
Обмен простых белков. Дезаминирование и трансаминирование аминокислот Нуклеиновые кислоты
Нуклеиновые кислоты Реакция Пфитцингера
Реакция Пфитцингера Химическая организация клетки. Неорганические вещества, входящие в состав клетки
Химическая организация клетки. Неорганические вещества, входящие в состав клетки Предмет органической химии. Теория строения органических веществ А.М. Бутлерова
Предмет органической химии. Теория строения органических веществ А.М. Бутлерова Топливо и его характеристики
Топливо и его характеристики Анализ лекарственных форм
Анализ лекарственных форм Обмен веществ. Регуляция водно-солевого обмена. (Лекция 5)
Обмен веществ. Регуляция водно-солевого обмена. (Лекция 5) Алхимический период
Алхимический период Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів
Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів Характеристика растворов. Кислоты, основания, соли в свете теории электролитической диссоциации. Гидролиз солей
Характеристика растворов. Кислоты, основания, соли в свете теории электролитической диссоциации. Гидролиз солей Дифференциальный диагноз анемий
Дифференциальный диагноз анемий Галогены Что это такое ?
Галогены Что это такое ? Химия элементов VIA группы
Химия элементов VIA группы Різноманіття карбонових кислот
Різноманіття карбонових кислот Одноатомні спирти Підготували Учениці 9-Б класу
Одноатомні спирти Підготували Учениці 9-Б класу  Презентация Проверим знания по теме «Кремний»
Презентация Проверим знания по теме «Кремний» Методы определения коэффициентов селективности
Методы определения коэффициентов селективности Моторные масла
Моторные масла Чистые вещества и смеси. Способы разделения смесей. Загадка
Чистые вещества и смеси. Способы разделения смесей. Загадка Золь. Свойства золи
Золь. Свойства золи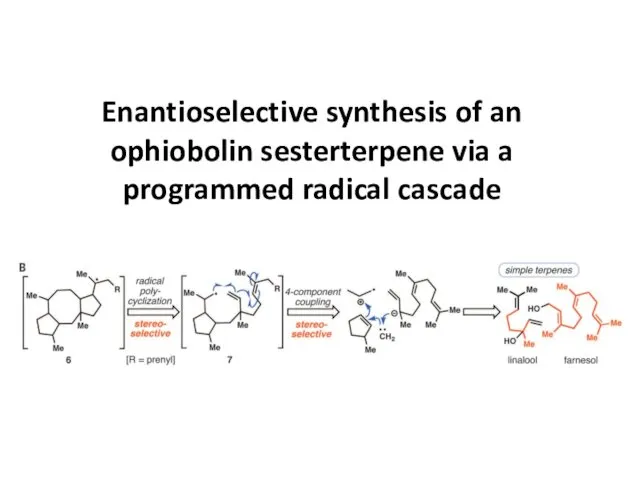 Enantioselective synthesis of an ophiobolin sesterterpene via a programmed radical cascade
Enantioselective synthesis of an ophiobolin sesterterpene via a programmed radical cascade Презентация по Химии "Металлы 9 класс" - скачать смотреть
Презентация по Химии "Металлы 9 класс" - скачать смотреть  Строение электронных оболочек атомов
Строение электронных оболочек атомов