Содержание
- 2. Цели лекции: Обучающая - Сформировать знания о строении, номенклатуре и реакционной способности стероидов. Развивающая – Расширить
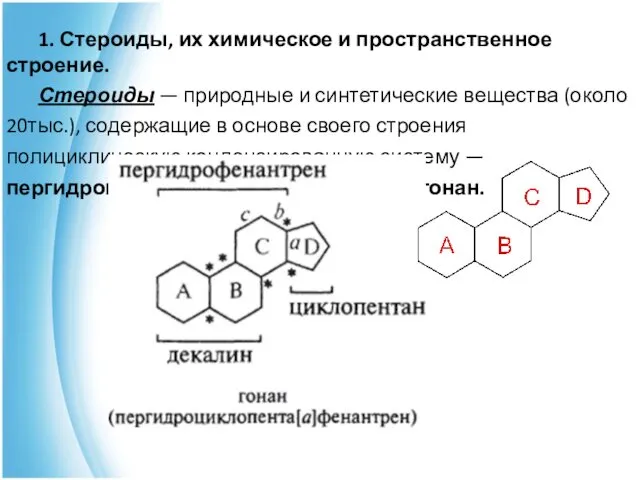
- 3. 1. Стероиды, их химическое и пространственное строение. Стероиды — природные и синтетические вещества (около 20тыс.), содержащие
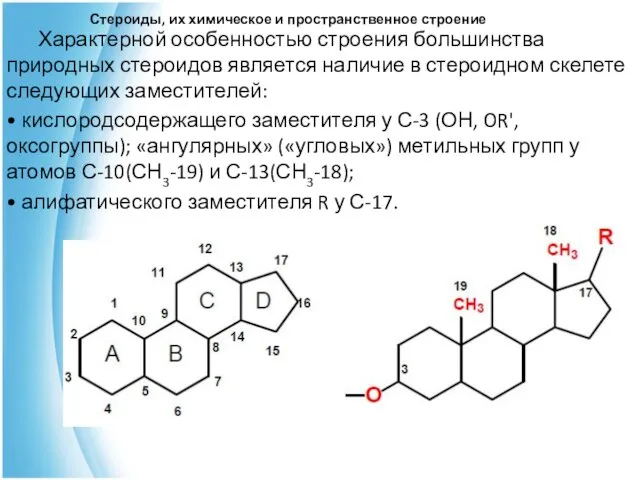
- 4. Стероиды, их химическое и пространственное строение Характерной особенностью строения большинства природных стероидов является наличие в стероидном
- 5. Стероиды, их химическое и пространственное строение Классификация стероидов по величине углеводородного радикала R у С-17
- 6. Стероиды, их химическое и пространственное строение Сочленение между собой попарно колец А и В, В и
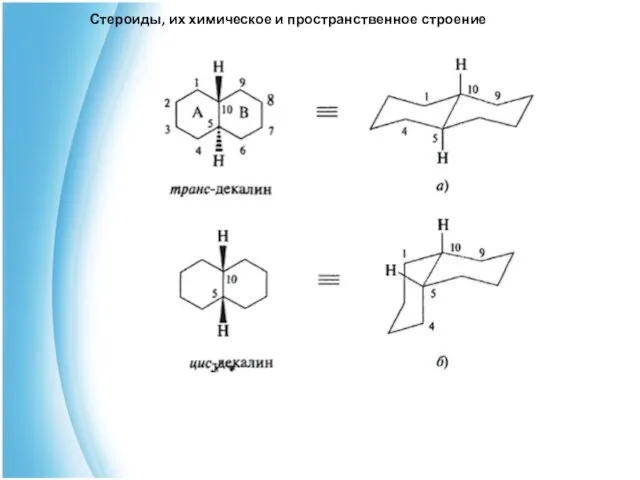
- 7. Стероиды, их химическое и пространственное строение
- 8. Стероиды, их химическое и пространственное строение В целом для природных стероидов наиболее характерны следующие типы сочленения
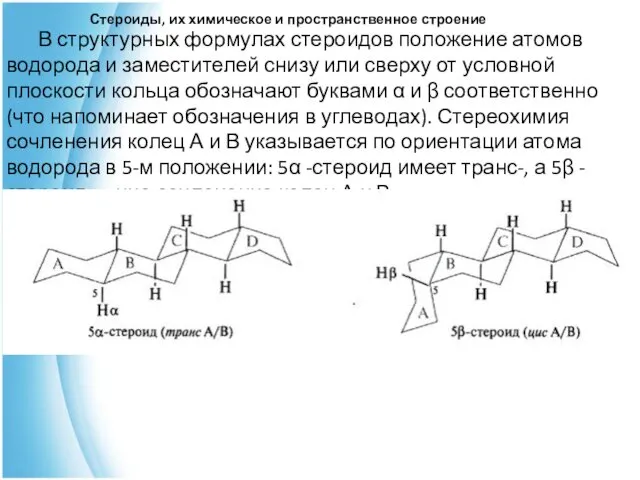
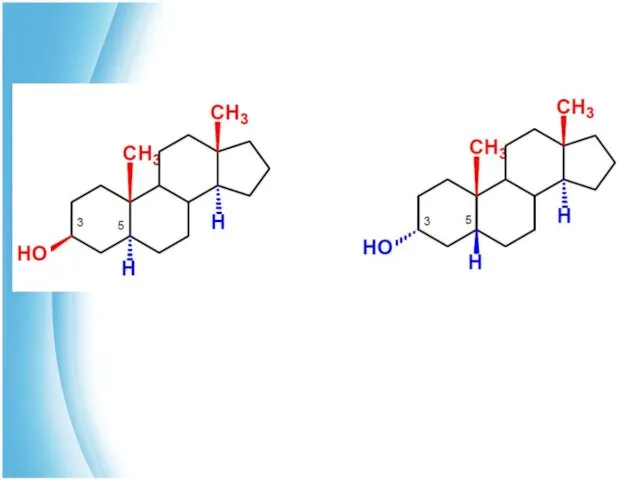
- 9. Стероиды, их химическое и пространственное строение В структурных формулах стероидов положение атомов водорода и заместителей снизу
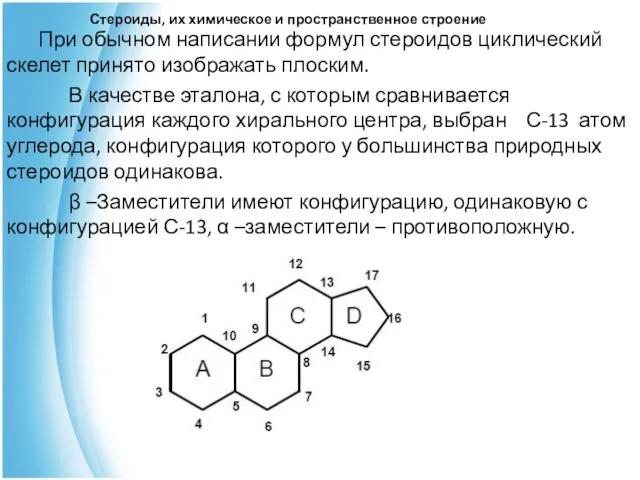
- 10. Стероиды, их химическое и пространственное строение При обычном написании формул стероидов циклический скелет принято изображать плоским.
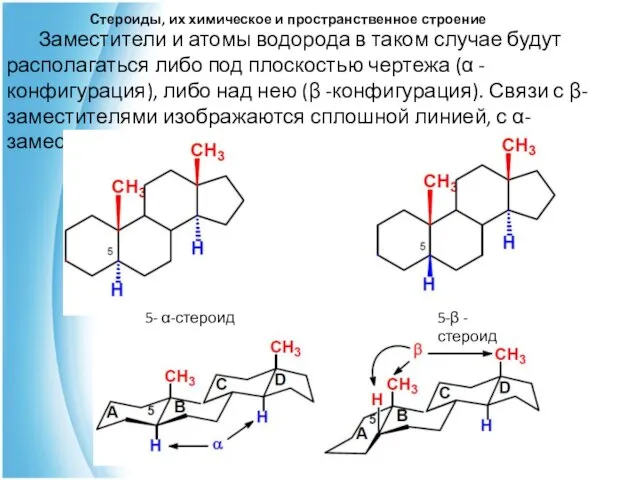
- 11. Стероиды, их химическое и пространственное строение Заместители и атомы водорода в таком случае будут располагаться либо
- 13. Стероиды, их химическое и пространственное строение Номенклатура стероидов. В основе названия стероидов лежат стереородоначальные углеводородные структуры
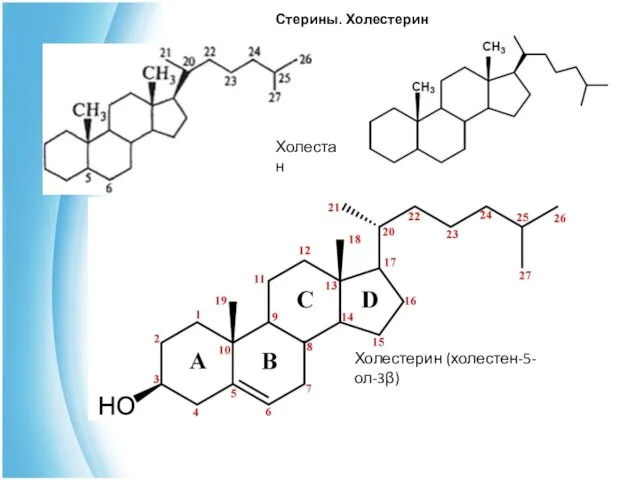
- 14. 2. Стерины. Холестерин. В основе стеринов лежат следующие углеводороды: холестан (С27), эргостан (С28) и стигмастан (С29).
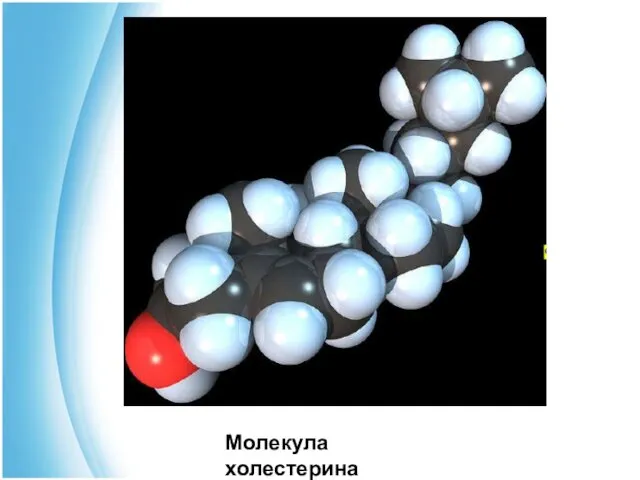
- 15. Стерины. Холестерин Холестерин (холестен-5-ол-3β) Холестан
- 16. Молекула холестерина
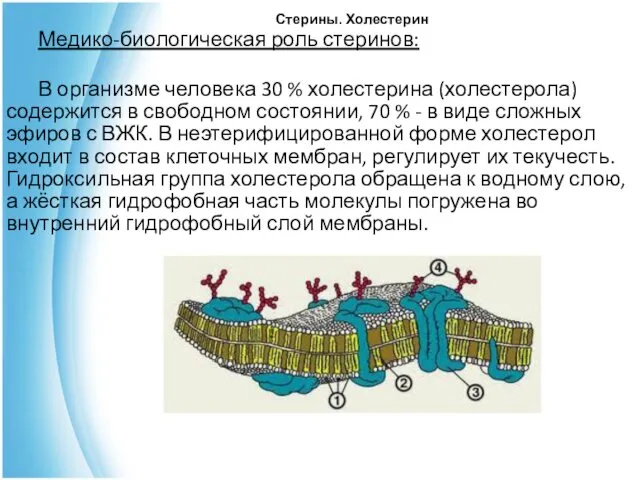
- 17. Стерины. Холестерин Медико-биологическая роль стеринов: В организме человека 30 % холестерина (холестерола) содержится в свободном состоянии,
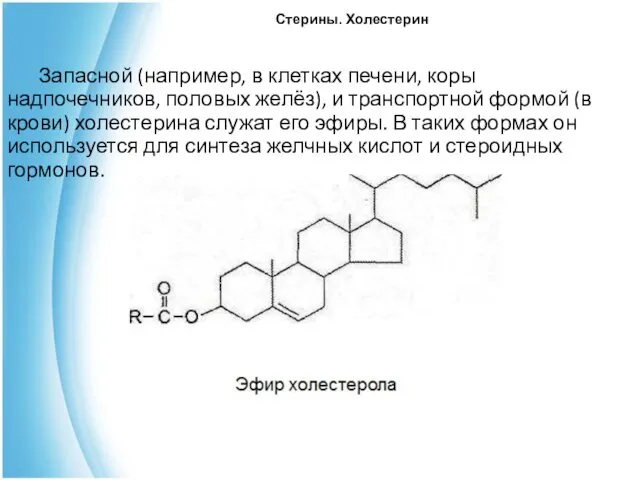
- 18. Стерины. Холестерин Запасной (например, в клетках печени, коры надпочечников, половых желёз), и транспортной формой (в крови)
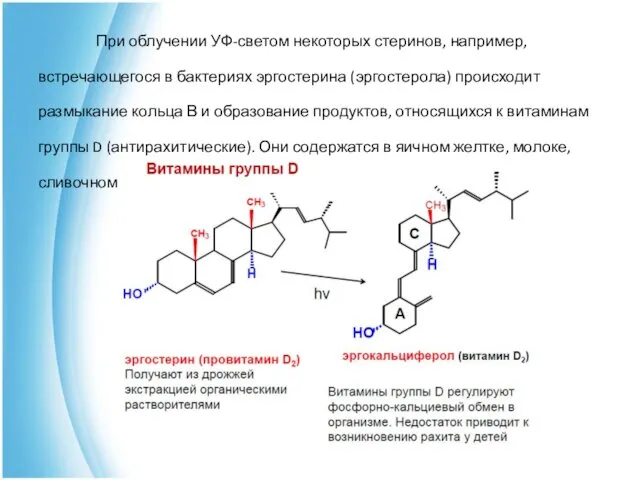
- 19. При облучении УФ-светом некоторых стеринов, например, встречающегося в бактериях эргостерина (эргостерола) происходит размыкание кольца В и
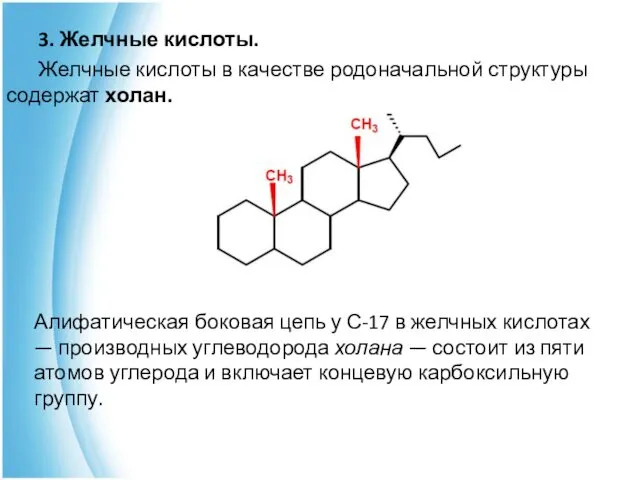
- 20. 3. Желчные кислоты. Желчные кислоты в качестве родоначальной структуры содержат холан. Алифатическая боковая цепь у С-17
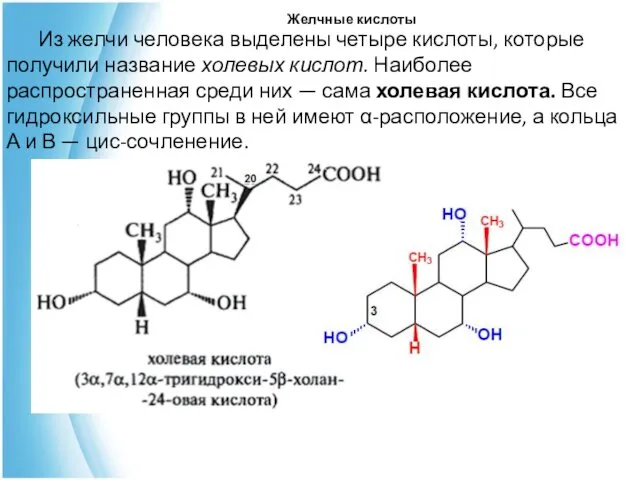
- 21. Желчные кислоты Из желчи человека выделены четыре кислоты, которые получили название холевых кислот. Наиболее распространенная среди
- 22. Желчные кислоты Другие кислоты этой группы отличаются отсутствием одной или двух гидроксильных групп у С-7 и
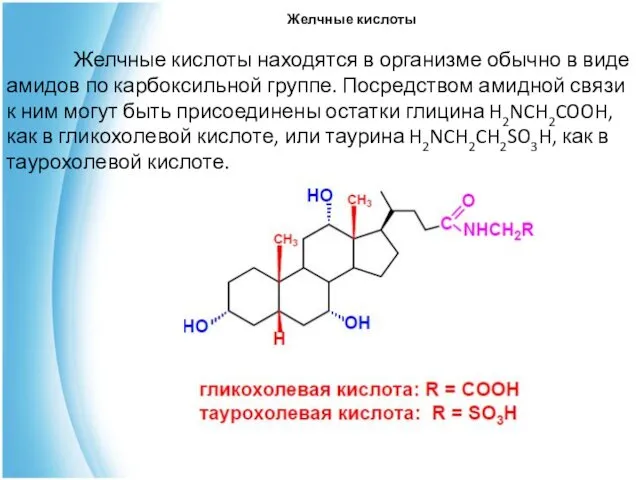
- 23. Желчные кислоты Желчные кислоты находятся в организме обычно в виде амидов по карбоксильной группе. Посредством амидной
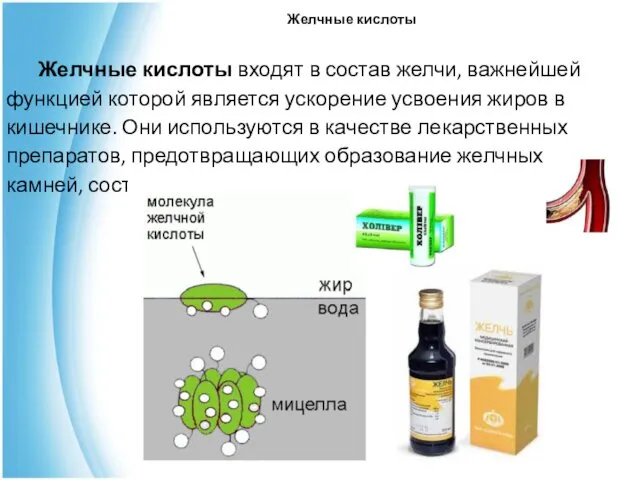
- 24. Желчные кислоты Желчные кислоты входят в состав желчи, важнейшей функцией которой является ускорение усвоения жиров в
- 25. 4. Стероидные гормоны. Гормонами называют биологически активные вещества, образующиеся в железах внутренней секреции и принимающие участие
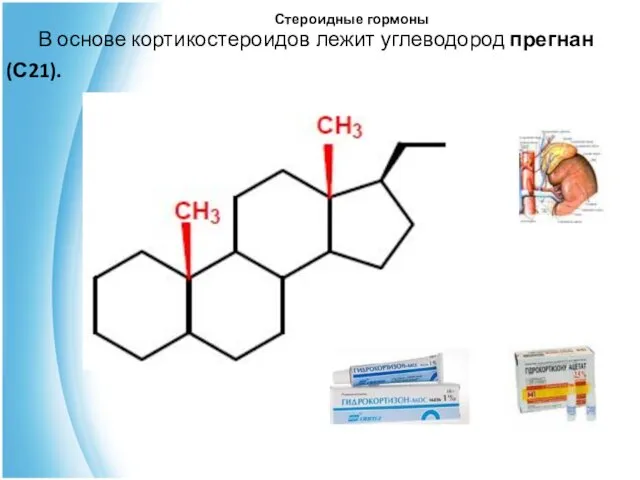
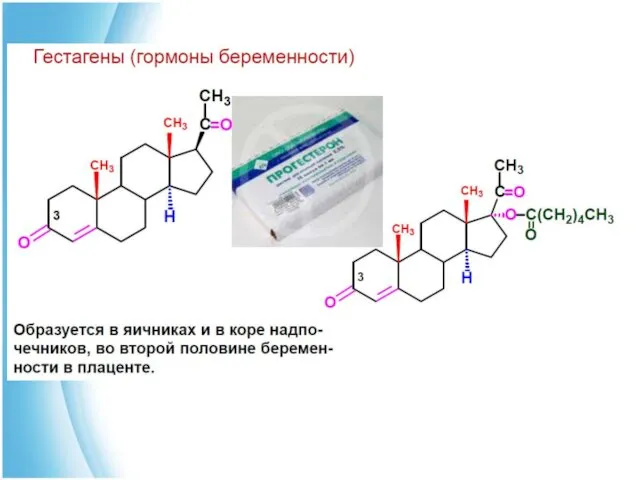
- 26. Стероидные гормоны В основе кортикостероидов лежит углеводород прегнан (С21).
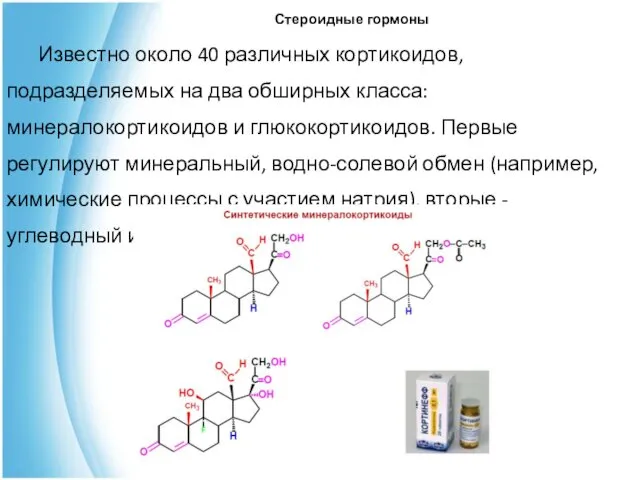
- 27. Стероидные гормоны Известно около 40 различных кортикоидов, подразделяемых на два обширных класса: минералокортикоидов и глюкокортикоидов. Первые
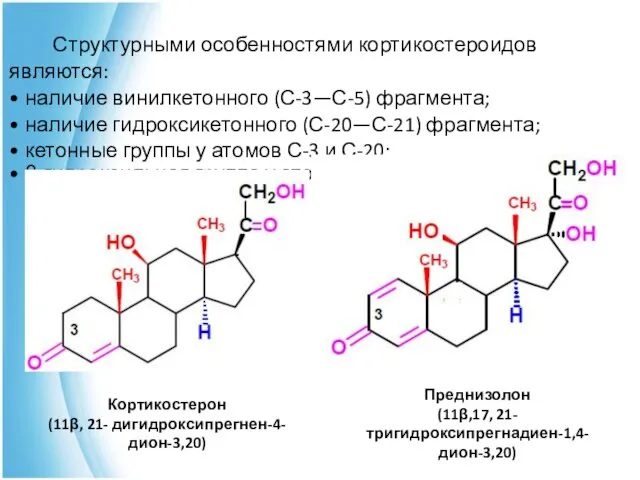
- 28. Структурными особенностями кортикостероидов являются: • наличие винилкетонного (С-3—С-5) фрагмента; • наличие гидроксикетонного (С-20—С-21) фрагмента; • кетонные
- 29. Стероидные гормоны Кортикостерон действует как антагонист инсулина, повышая содержание глюкозы в крови. Преднизолон представляет собой синтетический
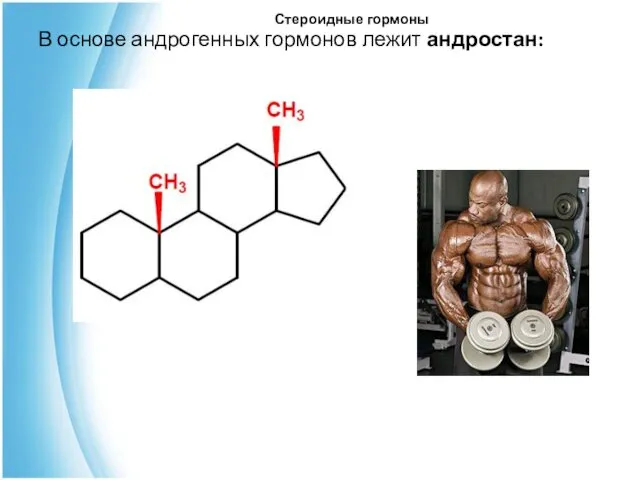
- 30. Стероидные гормоны В основе андрогенных гормонов лежит андростан:
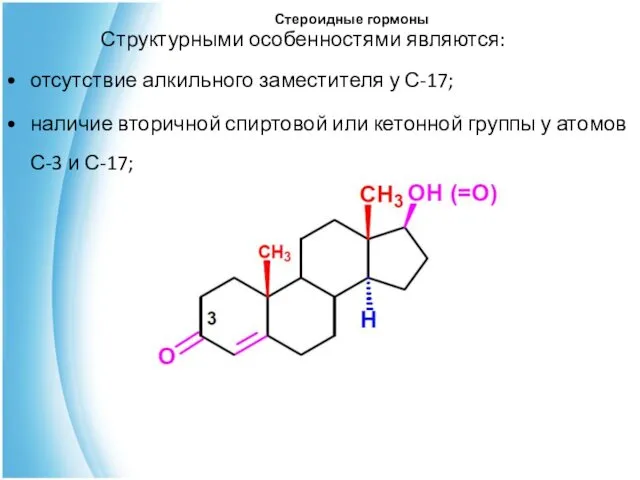
- 31. Стероидные гормоны Структурными особенностями являются: отсутствие алкильного заместителя у С-17; наличие вторичной спиртовой или кетонной группы
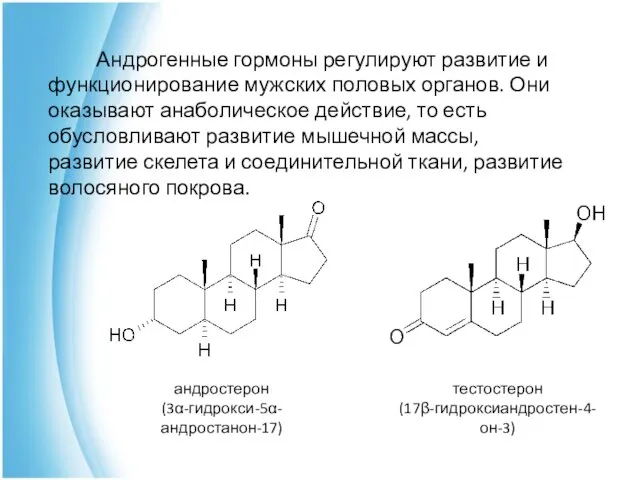
- 32. Андрогенные гормоны регулируют развитие и функционирование мужских половых органов. Они оказывают анаболическое действие, то есть обусловливают
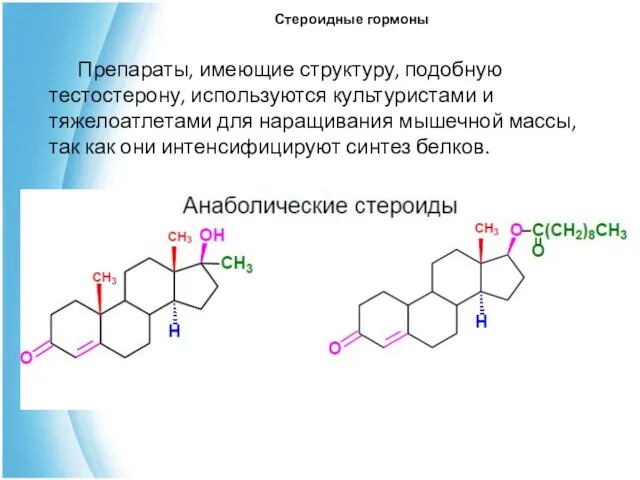
- 33. Стероидные гормоны Препараты, имеющие структуру, подобную тестостерону, используются культуристами и тяжелоатлетами для наращивания мышечной массы, так
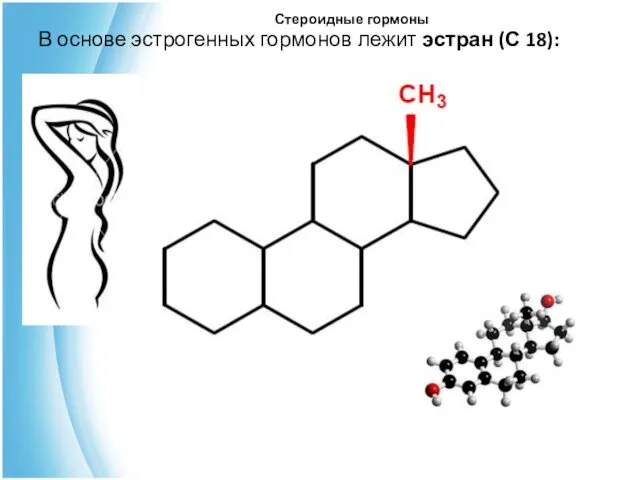
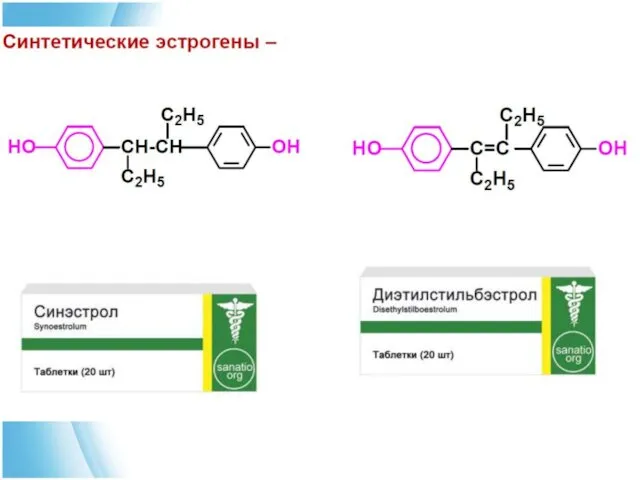
- 34. Стероидные гормоны В основе эстрогенных гормонов лежит эстран (С 18):
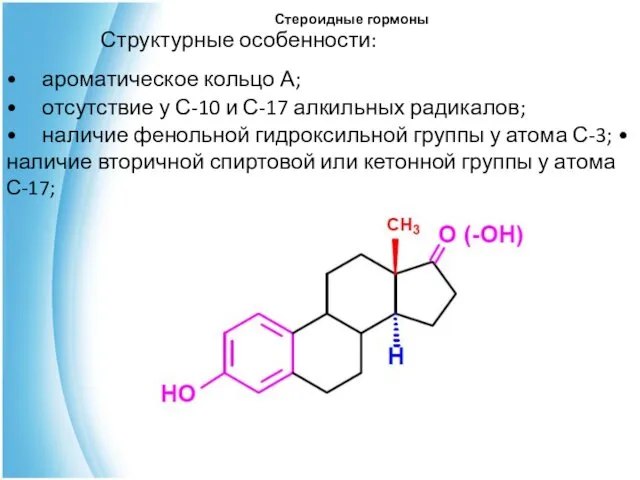
- 35. Стероидные гормоны Структурные особенности: • ароматическое кольцо А; • отсутствие у С-10 и С-17 алкильных радикалов;
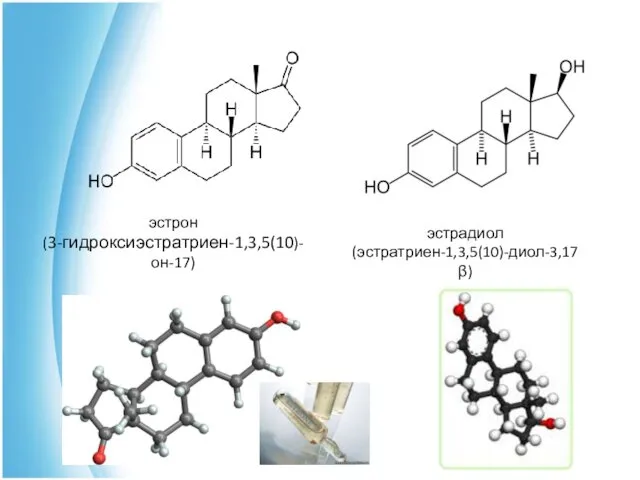
- 36. эстрон (3-гидроксиэстратриен-1,3,5(10)-он-17) эстрадиол (эстратриен-1,3,5(10)-диол-3,17β)
- 37. Стероидные гормоны Медико-биологическая роль Природные эстрогены обусловливают Развитие женских половых органов; Регуляцию овуляции Подготовку организма женщины
- 40. Андрогенные и эстрогенные гормоны играют огромную роль в регуляции не только репродуктивной функции, но и существенно
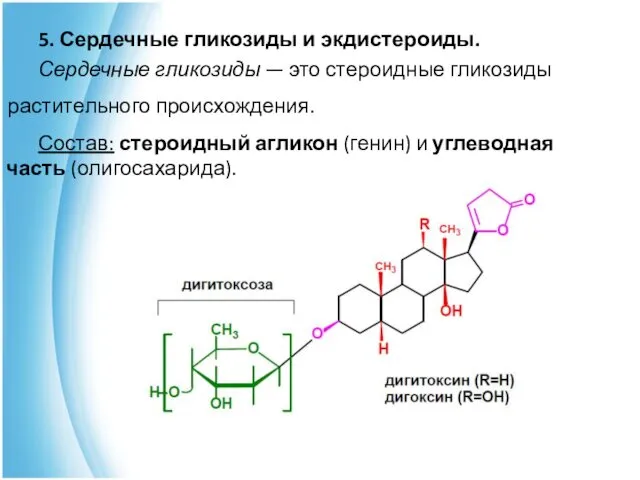
- 41. 5. Сердечные гликозиды и экдистероиды. Сердечные гликозиды — это стероидные гликозиды растительного происхождения. Состав: стероидный агликон
- 42. Структурными особенностями агликонов являются: • наличие ненасыщенного лактонного кольца в положении 17 гонановой системы; • наличие
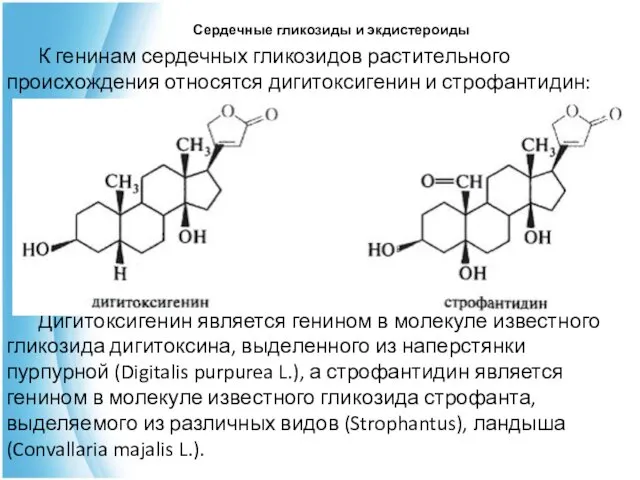
- 43. К генинам сердечных гликозидов растительного происхождения относятся дигитоксигенин и строфантидин: Дигитоксигенин является генином в молекуле известного
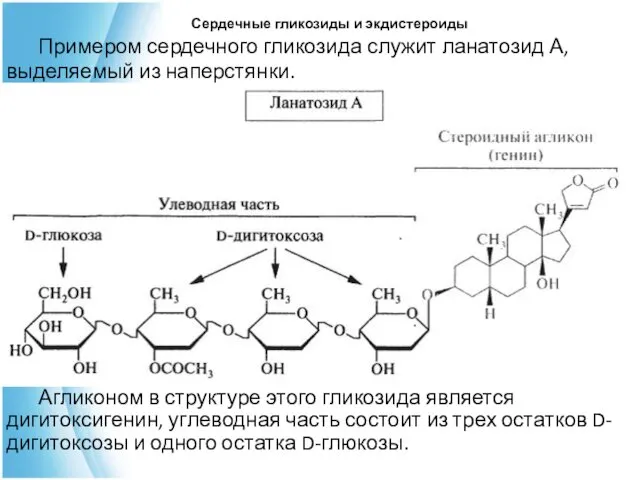
- 44. Примером сердечного гликозида служит ланатозид А, выделяемый из наперстянки. Агликоном в структуре этого гликозида является дигитоксигенин,
- 45. Медико-биологическая роль В небольших количествах сердечные гликозиды возбуждают сердечную деятельность и используются в кардиологии. В больших
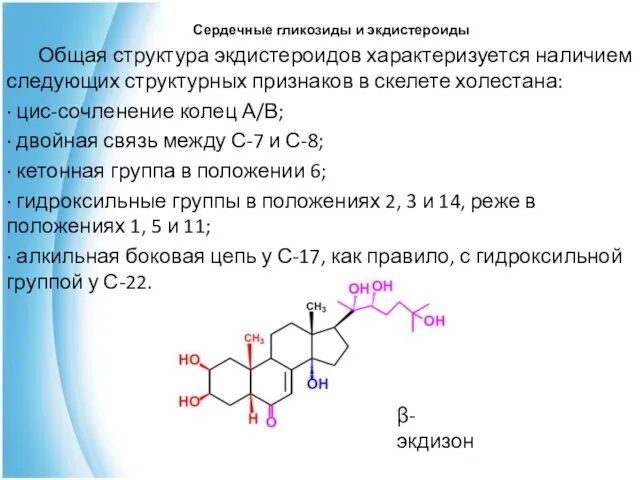
- 46. Общая структура экдистероидов характеризуется наличием следующих структурных признаков в скелете холестана: · цис-сочленение колец А/В; ·
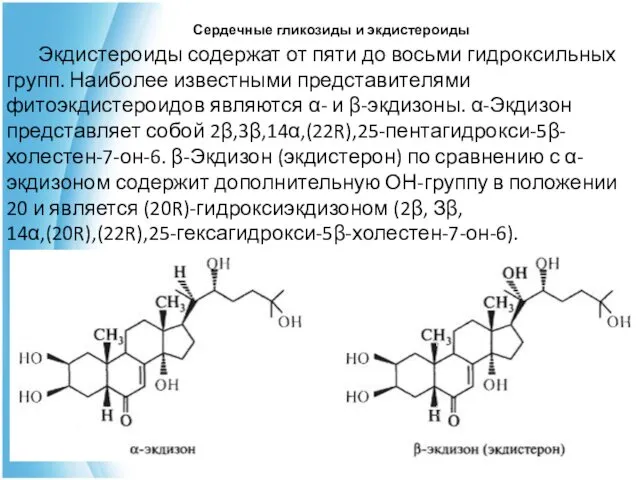
- 47. Экдистероиды содержат от пяти до восьми гидроксильных групп. Наиболее известными представителями фитоэкдистероидов являются α- и β-экдизоны.
- 48. В настоящее время идентифицировано более 250 фитоэкдистероидов. Возрастающий интерес обусловлен широким спектром биологической активности, проявляемой фитоэкдистероидами
- 49. В зависимости от источника выделения различают зооэкдистероиды и фитоэкдистероиды. Содержание фитоэкдистероидов в растительных объектах обычно составляет
- 51. Скачать презентацию














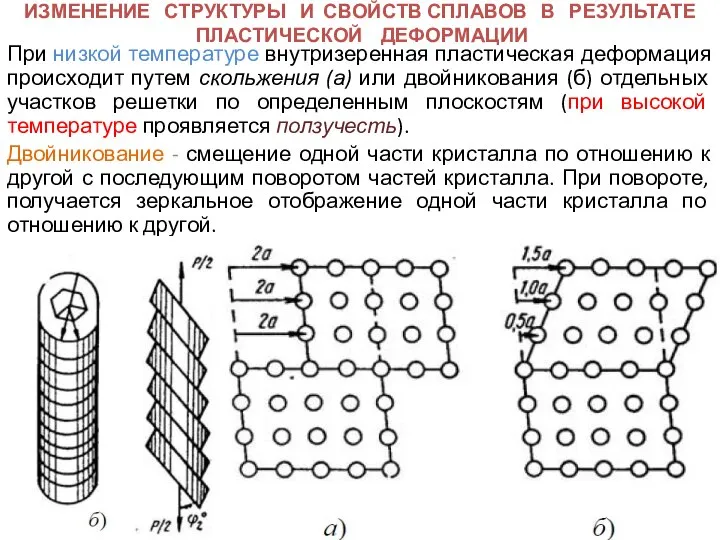 Изменение структуры и свойств сплавов в результате пластической деформации
Изменение структуры и свойств сплавов в результате пластической деформации Альдегиды. Раствор формальдегида. Гексаметилентетрамин (метенамин)
Альдегиды. Раствор формальдегида. Гексаметилентетрамин (метенамин) Ароматические углеводороды. Процессы производства. Направления использования
Ароматические углеводороды. Процессы производства. Направления использования Жевательная резинка польза или вред
Жевательная резинка польза или вред Генетика клеточного цикла. Периоды клеточного цикла. Выборка к зачету
Генетика клеточного цикла. Периоды клеточного цикла. Выборка к зачету Углеводы (сахара). Строение, свойства, участие в функционировании живых систем
Углеводы (сахара). Строение, свойства, участие в функционировании живых систем Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би
Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би Хозяйственный механизм НГХК
Хозяйственный механизм НГХК Крахмал (C6H10O5)n
Крахмал (C6H10O5)n  ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ 1.ОВР.Классификация ОВР. 2.Метод электронного баланса. 3.Метод полуреакций.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ 1.ОВР.Классификация ОВР. 2.Метод электронного баланса. 3.Метод полуреакций.  Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Proteins. Functions, structure, classification
Proteins. Functions, structure, classification Порфирины. Производные порфина. (Лекция 14)
Порфирины. Производные порфина. (Лекция 14) Основания и их свойства
Основания и их свойства Расчет концентрационных пределов воспламенения жидкости
Расчет концентрационных пределов воспламенения жидкости Ап-конверсионная люминесценция в наностеклокерамике
Ап-конверсионная люминесценция в наностеклокерамике Класс «оксиды»
Класс «оксиды» Металлы. Урок – обобщения
Металлы. Урок – обобщения Молекулярные массы и гибкость полимеров
Молекулярные массы и гибкость полимеров Фосфаттар - минералдар класы - ортофосфорлы қышқыл (Н3РO4) тұздары
Фосфаттар - минералдар класы - ортофосфорлы қышқыл (Н3РO4) тұздары Амины
Амины Қызықты химия
Қызықты химия Химическая связь. Взаимное влияние атомов в молекуле
Химическая связь. Взаимное влияние атомов в молекуле Великие химики
Великие химики Исследовательская работа Авторы: Филатова Диана,
Исследовательская работа Авторы: Филатова Диана,  Алмаз. Внутренняя структура алмаза
Алмаз. Внутренняя структура алмаза Муниципальное бюджетное общеобразовательное учреждение «Клюквинская средняя общеобразовательная школа-интернат» Верхнекетско
Муниципальное бюджетное общеобразовательное учреждение «Клюквинская средняя общеобразовательная школа-интернат» Верхнекетско Галогены
Галогены