Содержание
- 2. Определение. Номенклатура. Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-ионов.
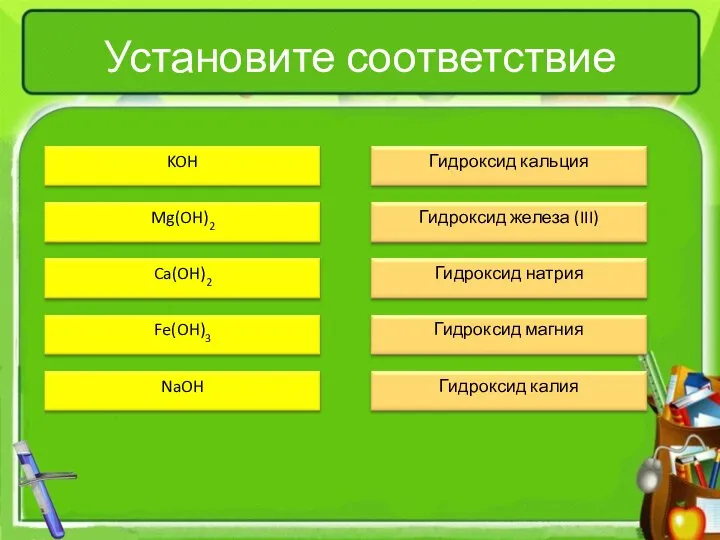
- 3. Установите соответствие
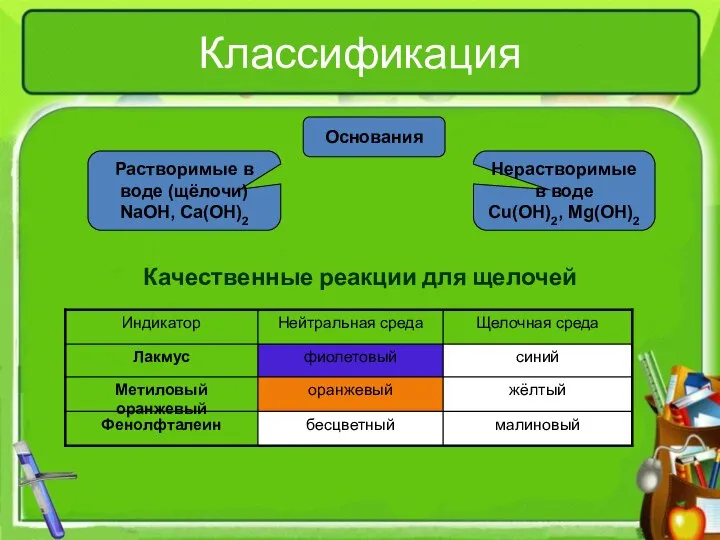
- 4. Нерастворимые в воде Cu(OH)2, Mg(OH)2 Растворимые в воде (щёлочи) NaOH, Ca(OH)2 Классификация Качественные реакции для щелочей
- 5. Химические свойства оснований Основание + кислота = соль + вода (р-ция обмена) NaOH + HCl =
- 6. Проверьте ваши знания Закончите молекулярные уравнения возможных реакций: KOH + P2O5 Cu(OH)2 + H2SO4 Mg(OH)2 +
- 8. Скачать презентацию



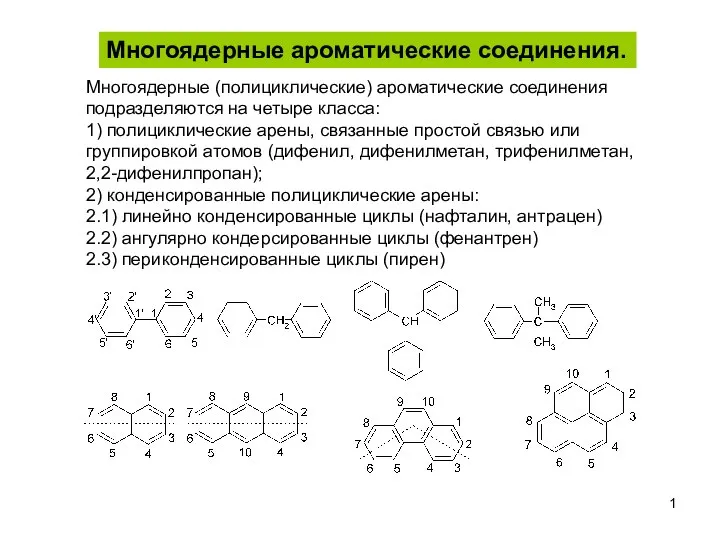 Многоядерные ароматические соединения
Многоядерные ароматические соединения Классификация углеводов
Классификация углеводов Жидкие системы
Жидкие системы Градуировка спектральных приборов
Градуировка спектральных приборов Химия в косметике
Химия в косметике Растворы высокомолекулярных соединений (ВМС)
Растворы высокомолекулярных соединений (ВМС) Презентация по Химии "Классы неорганических веществ" 8 класс
Презентация по Химии "Классы неорганических веществ" 8 класс Трифенилметановые красители
Трифенилметановые красители Гидролиз. Методы его получения и применения
Гидролиз. Методы его получения и применения Месторождения железистых кварцитов
Месторождения железистых кварцитов Опасные химикаты
Опасные химикаты 8 класс
8 класс  Электролиз.
Электролиз.  Фосфор как элемент мысли и жизни
Фосфор как элемент мысли и жизни Link reaction
Link reaction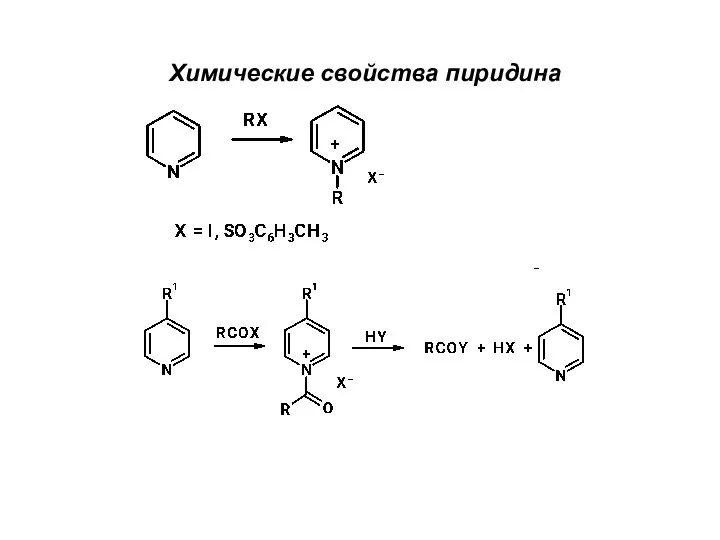 Химические свойства пиридина
Химические свойства пиридина Роль химических элементов в жизнедеятельности организма
Роль химических элементов в жизнедеятельности организма Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття
Явища природи. Фізичні явища, їх різноманітність. Хімічні явища, їх ознаки. Горіння. Гниття Полярография и измерение рН
Полярография и измерение рН Арбузный снег. Предположения
Арбузный снег. Предположения Презентация по Химии "Алкены." - скачать смотреть бесплатно_
Презентация по Химии "Алкены." - скачать смотреть бесплатно_ Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Кількість речовини в хімії
Кількість речовини в хімії 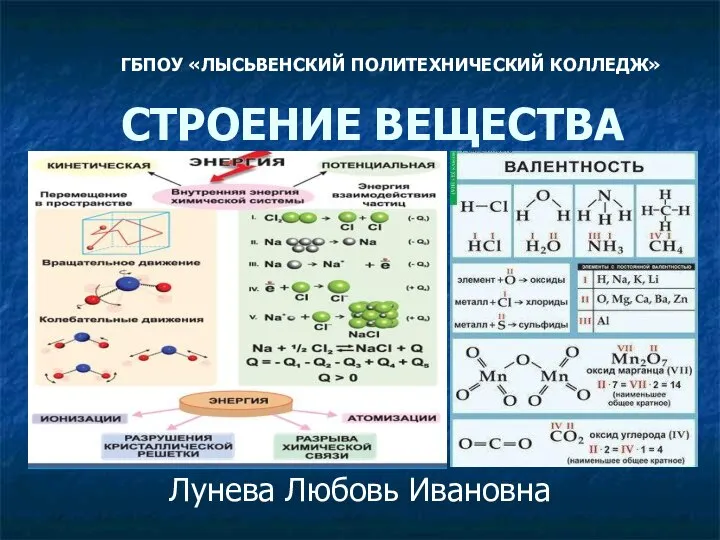 Строение вещества
Строение вещества Диктант: название алканов
Диктант: название алканов Трансформация соединений азота
Трансформация соединений азота Їх згубна дія на організм людини СПИРТИ
Їх згубна дія на організм людини СПИРТИ  Азот и фосфор
Азот и фосфор