Содержание
- 2. Пла́тина (исп. Platina) химический элемент 10-й группы (по устаревшей классификации побочной подгруппы восьмой группы), 6-го периода
- 3. История В Старом Свете платина не была известна до середины XVI века, однако цивилизации Анд добывали
- 4. Благодаря предприимчивости министра финансов Е. Ф. Канкрина с 1828 г. в Российской империи стали выпускать платиновые
- 5. Физические свойства серовато-белый пластичный ковкий металл t плавления = 1768, 3 °C t кипения = 3825
- 6. Химические свойства Платина является одним из самых инертных металлов. По химическим свойствам платина похожа на палладий,
- 7. Химические свойства При нагревании платина реагирует с кислородом с образованием летучих оксидов. Выделены следующие оксиды платины:
- 8. Применение С первой четверти XIX века применялась в России в качестве легирующей добавки для производства высокопрочных
- 9. Применение Платина и её сплавы широко используются для производства ювелирных изделий. Большинство ювелирных изделий из платины
- 10. Применение Незначительная часть платины идет в медицинскую промышленность. Из платины и ее сплавов изготовляют хирургические инструменты,
- 11. Применение в химии Платина – лучший катализатор реакции окисления аммиака до окиси азота NO в одном
- 13. Скачать презентацию










 Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23)
Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23) Инертные газы
Инертные газы Металлы II, побочной подгруппы ПСХЭ
Металлы II, побочной подгруппы ПСХЭ Chemistry
Chemistry Презентация Состав газированной воды
Презентация Состав газированной воды Соединительная ткань. Биохимия межклеточного матрикса. (Тема 8)
Соединительная ткань. Биохимия межклеточного матрикса. (Тема 8) Непредельные углеводороды: алкены
Непредельные углеводороды: алкены Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Таблица Менделеева
Таблица Менделеева Теория резонанса в неорганической химии
Теория резонанса в неорганической химии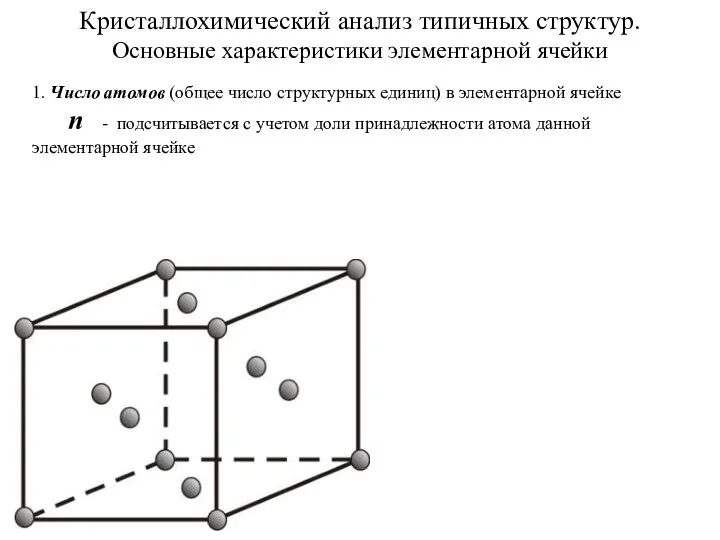 Кристаллохимический анализ типичных структур. Основные характеристики элементарной ячейки
Кристаллохимический анализ типичных структур. Основные характеристики элементарной ячейки Индикатор pH
Индикатор pH Вода – простой взгляд на химический состав
Вода – простой взгляд на химический состав Елементи головних підгруп І-ІІІ. Періодична система Менделєєва
Елементи головних підгруп І-ІІІ. Періодична система Менделєєва Координационные соединения
Координационные соединения Презентация по Химии "Мыло. Синтетические моющие средства" - скачать смотреть
Презентация по Химии "Мыло. Синтетические моющие средства" - скачать смотреть  Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Основные методы получения моно- и поликристаллического SiC. Диаграмма состояния
Основные методы получения моно- и поликристаллического SiC. Диаграмма состояния Physics and chemistry of surface phenomena
Physics and chemistry of surface phenomena Оценка срока службы для полимерных материалов методами термического анализа
Оценка срока службы для полимерных материалов методами термического анализа Действующие вещества. Лексикон
Действующие вещества. Лексикон Методы выделения и анализа биологически активных веществ
Методы выделения и анализа биологически активных веществ Газохроматографический анализ летучих ядов
Газохроматографический анализ летучих ядов Презентація уроку «Різноманітність речовин. Поняття про прості та складні речовини, неорганічні та органічні речовини» Підготув
Презентація уроку «Різноманітність речовин. Поняття про прості та складні речовини, неорганічні та органічні речовини» Підготув Основные сведения о строении атома. Состав атомных ядер
Основные сведения о строении атома. Состав атомных ядер Белоктар – биополимерлер
Белоктар – биополимерлер Качественный химический анализ воды на определение металлов
Качественный химический анализ воды на определение металлов Хімічні знання в різні епохи
Хімічні знання в різні епохи