Содержание
- 2. Стратегия подготовки обучающихся к ЕГЭ Учителя обучение химии с 8-го класса тесно связывают с подготовкой учеников
- 3. Два основных результата учения ученика: научился познавать сущность химических явлений; понял, запомнил, а также научился использовать
- 4. Для достижения результатов обучения необходимо 1. Раскрывать как устроен мир 2. Обучать познавать мир
- 5. «Раскрывать как устроен Мир» - репродуктивная модель обучения Познание трактуется как процесс ретрансляции знаний от старшего
- 6. Содержание репродуктивного опыта познания Способность запоминать учебный материал большого объема. Беспристрастное, ровное отношение к учебе. Понять
- 7. Риски репродуктивной модели обучения Угнетающее влияние на способности рефлексивно и критически мыслить не только на учеников,
- 8. Риски репродуктивной модели обучения Уровень владения упакованным продуктом легко проверить с помощью различных тестовых методик.
- 9. Источник разрушения естественных психических способностей познания Убежденность педагогов в том, что необходимо постоянно повышать требования к
- 10. Проблема обсуждается более 100 лет Преподаватели, пытающиеся сразу сформировать у студентов исчерпывающие знания, соответствующие современному состоянию
- 11. «Обучать познавать Мир» - продуктивная модель обучения Рассматривает познание, как познавательное усилие по преодолению трудности открытия
- 12. Важны не только интеллектуальные, но и личностные качества. Личностная обусловленность познания - не только мотивационная составляющая,
- 13. Содержание опыта продуктивного познания Способность к самоорганизации и самопознанию, направленным на преодоление постоянного дефицита имеющихся у
- 15. Задания ЕГЭ стали сложнее В части 1. вероятность угадывания сведена к минимуму Больше стало заданий на
- 16. Задание 30 и 31 С 2018 года к заданиям 30 и 31 дается перечень веществ. Ученику
- 17. Задание 30 При подготовке к выполнению этого задания ученики должны: запомнить перечень типичных окислителей и восстановителей;
- 18. Типичные окислители и восстановители Типичные окислители: KMnO4, MnO2, K2Cr2O7, K2CrO4, KClO, KClO3, HNO3, H2SO4(конц.), H2O2, Fe3+,
- 19. Пример из демонстрационной версии ЕГЭ 2018 Дан перечень веществ или их водных растворов: перманганат калия, гидрокарбонат
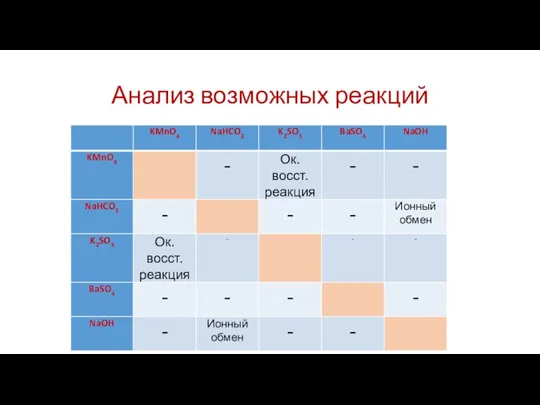
- 20. Анализ возможных реакций
- 21. Выполнение задания 30 Схема электронного баланса Сера со степенью окисления +4, в составе сульфита калия, -
- 22. Задание 31 Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. В ответе
- 23. Для обучения учеников выполнению заданий 30 и 31 целесообразно: составлять перечни веществ, учить учеников определять, какие
- 24. Задание 32 посвящено проверке знаний реакций, подтверждающих взаимосвязь различных классов неорганических веществ. В задании дается описание
- 25. Пример задания 32 (http://www.fipi.ru/) При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной
- 26. Первая реакция При электролизе водного раствора нитрата меди: на катоде выделяется медь Сu2+ + 2ē =
- 27. Вторая реакция Cu + 2H2SO4(конц.) = CuSO4 + SO2↑ + 2H2O Третья реакция 3SO2 + 2H2S
- 28. Четвертая реакция . Диспропорционирование серы (реакция обратная третьей)
- 29. Задание 33 Цепочка превращения органических соединений. От учеников требуется: составить уравнения соответствующих этой цепочке реакций; для
- 30. Пример задания 33 Составьте уравнения реакций, соответствующих следующей цепочке превращения веществ Первое уравнение Второе уравнение
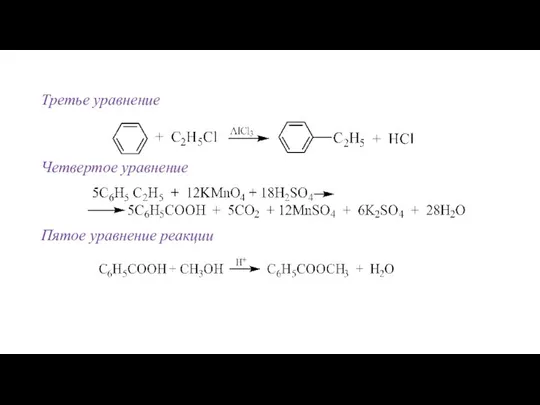
- 31. Третье уравнение Четвертое уравнение Пятое уравнение реакции
- 32. Задание 34 Приведены массы или объемы реагирующих в растворе веществ нужно определить массовую долю вещества в
- 33. Пример задания 34 (http://www.fipi.ru/) При нагревании образца карбоната кальция часть вещества разложилась. При этом выделилось 4,48
- 34. Составление схемы условия 1. Составим уравнения упомянутых реакций. 2. По объему углекислого газа определим массу оксида
- 35. Решение: 1. Уравнения реакций 2. Количество вещества выделившегося углекислого газа 4,48 л / 22,4 л/моль =
- 36. По уравнению реакции карбоната кальция с соляной кислотой n(СаCO3) = n(CO2) Масса выделившегося углекислого газа m(CO2)
- 37. Задание 35 Задача на вывод формулы органического соединения. Год от года задача усложняется. В последние годы
- 38. Пример задания 35 (http://www.fipi.ru/) Органическое вещество А содержит 11,97% азота, 9,40% водорода и 27,35% кислорода по
- 39. Этапы решения На основания данных количественного анализа вывести простейшую формулу вещества. Указание на то, что вещество
- 40. Решение: Вывод простейшей формулы вещества Массовая доля углерода w(C) = 1 – 0,1197(N) – 0,0940(H) –
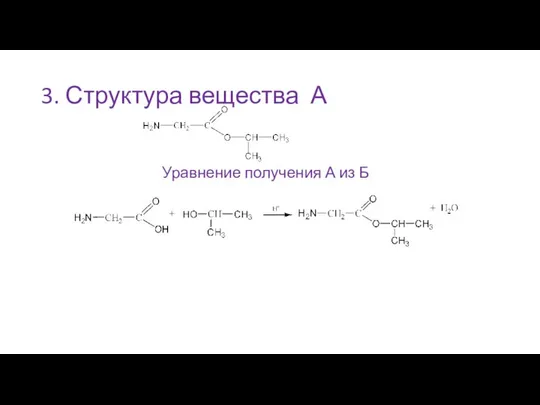
- 41. 3. Структура вещества А Уравнение получения А из Б
- 43. Скачать презентацию




































 Тема: «Самородные металлы».
Тема: «Самородные металлы». Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ
Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ Сполуки неметалічних елементів з гідрогеном. Амоніак та хлороводень
Сполуки неметалічних елементів з гідрогеном. Амоніак та хлороводень Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Презентация по Химии "Регуляторы биомолекулярных процессов" - скачать смотреть
Презентация по Химии "Регуляторы биомолекулярных процессов" - скачать смотреть  Подготовка к ГИА. А14. Определение характера среды раствора кислот и щелочей с помощью индикаторов. Реакции на ионы в растворе
Подготовка к ГИА. А14. Определение характера среды раствора кислот и щелочей с помощью индикаторов. Реакции на ионы в растворе Коллоидные растворы поверхностно-активных веществ (ПАВ)
Коллоидные растворы поверхностно-активных веществ (ПАВ) Химические аспекты выбора полимеров-предшественников для получения углеродных волокон
Химические аспекты выбора полимеров-предшественников для получения углеродных волокон Стеклообразное состояние полимеров. (Лекция 5)
Стеклообразное состояние полимеров. (Лекция 5) SNAP i.d. Workflow Value Proposition
SNAP i.d. Workflow Value Proposition Оксигеновмісні сполуки Підготувала учениця 11-Б класу Нововолинського ліцею-інтернату Волинської обласної ради Федина Вале
Оксигеновмісні сполуки Підготувала учениця 11-Б класу Нововолинського ліцею-інтернату Волинської обласної ради Федина Вале Физико-химические методы исследования и техника лабораторных работ
Физико-химические методы исследования и техника лабораторных работ Синтез метилового эфира цинкофорина
Синтез метилового эфира цинкофорина Пористые адсорбенты. Лекция 06
Пористые адсорбенты. Лекция 06 Оксидтер, жіктелуі, аталуы, алу жолдары, химиялық қасиеттері
Оксидтер, жіктелуі, аталуы, алу жолдары, химиялық қасиеттері «Строение атома и периодическая система» Химический диктант в 8 классе
«Строение атома и периодическая система» Химический диктант в 8 классе Валентность химических элементов
Валентность химических элементов Электролиттік диссоциация
Электролиттік диссоциация Лекция 8. Нуклеофильное присоединение к кратным связям углерод-гетероатом. Карбонильные соединения
Лекция 8. Нуклеофильное присоединение к кратным связям углерод-гетероатом. Карбонильные соединения Біографія Д. І. Менделєєва
Біографія Д. І. Менделєєва  Почему вода в море солёная
Почему вода в море солёная Полимеры
Полимеры Металлокомплексный катализ. (Лекция 16)
Металлокомплексный катализ. (Лекция 16) Химический состав свежих плодов и овощей
Химический состав свежих плодов и овощей Крахмал. Строение вещества
Крахмал. Строение вещества Моноядерні арени
Моноядерні арени Признаки химических реакций. (Практическая работа 5,4)
Признаки химических реакций. (Практическая работа 5,4) Явище ізомерії. Структурна ізомерія Виконав Пивоварчук Вадим
Явище ізомерії. Структурна ізомерія Виконав Пивоварчук Вадим