Содержание
- 2. Сера принадлежит к числу веществ, известных человечеству испокон веков. Ещё древние греки и римляне нашли ей
- 3. В живой природе: Входит в состав животных и растительных белков, витаминов, гормонов. СЕРА В ПРИРОДЕ Сера
- 4. Самородная сера, серный колчедан FeS2, медный колчедан CuFeS2, свинцовый блеск PbS с цинковой обманкой ZnS Ангидрит
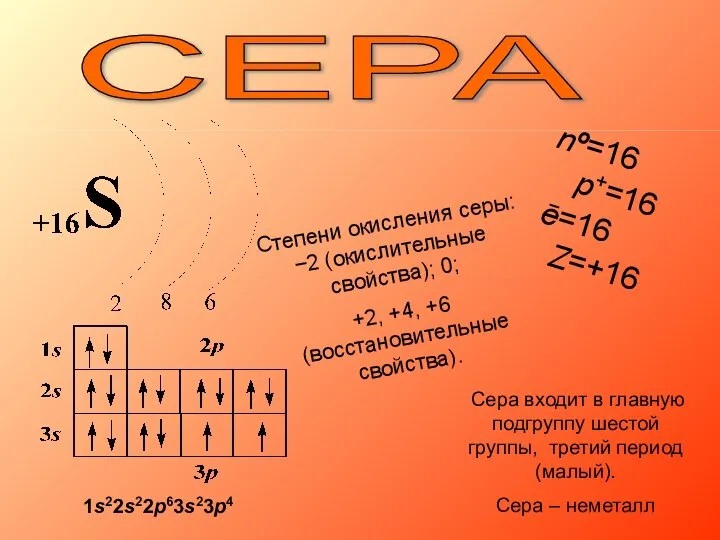
- 5. СЕРА nº=16 p+=16 ē=16 Z=+16 Степени окисления серы: −2 (окислительные свойства); 0; +2, +4, +6 (восстановительные
- 6. ФИЗИЧЕСКИЕ СВОЙСТВА СЕРЫ Сера – твердое кристаллическое вещество, не имеет запаха Не растворяется в воде. Хорошо
- 7. ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ S Реагирует с металлами (искл. золото, платина и рутений): 2Na + S =
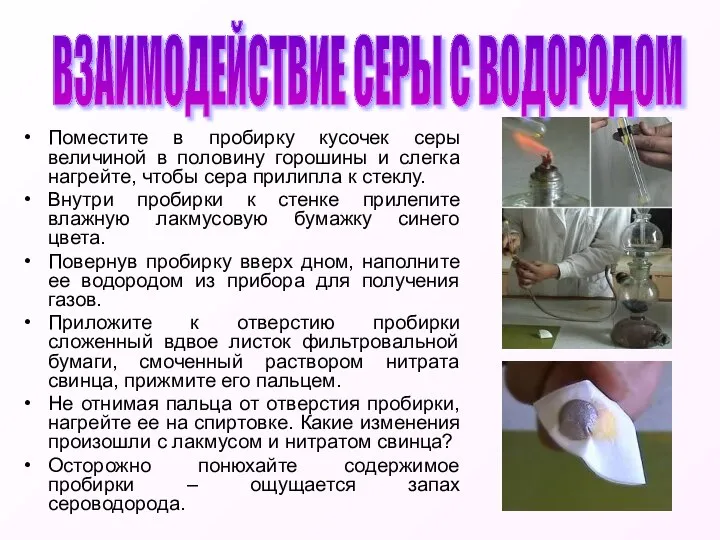
- 8. Поместите в пробирку кусочек серы величиной в половину горошины и слегка нагрейте, чтобы сера прилипла к
- 9. Заполните кислородом колбу емкостью 250–300 мл. Заполнение проверьте тлеющей лучиной, поднеся ее к краю сосуда. Прикройте
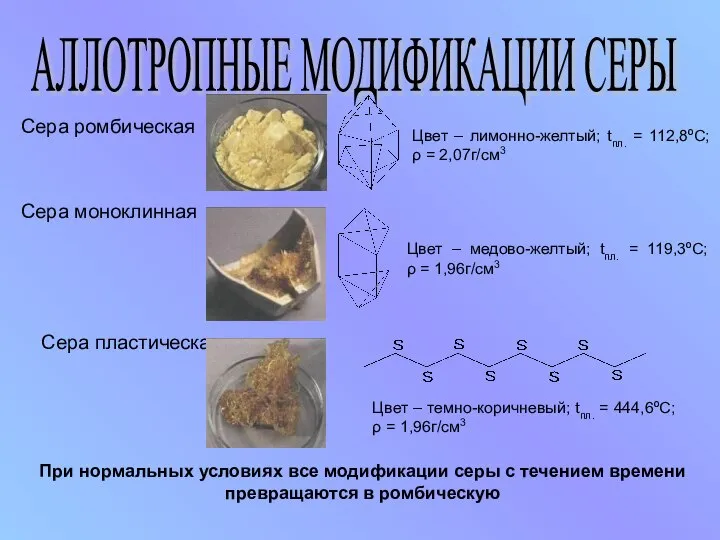
- 10. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ СЕРЫ Сера ромбическая Сера пластическая Сера моноклинная Цвет – лимонно-желтый; tпл. = 112,8ºС; ρ
- 11. В пробирку объемом 10 мл поместите мелкие кусочки серы и нагрейте ее до расплавления (при 119OС).
- 12. ПОЛУЧЕНИЕ СЕРЫ Неполное окисление сероводорода: 2H2S + O2 = 2S↓ + 2H2O (недостаток O2). 2. Реакция
- 13. ПРИМЕНЕНИЕ СЕРЫ S
- 15. Скачать презентацию









 Валентність
Валентність  Метан и его свойства.
Метан и его свойства. Стандартизація лікарської рослинної сировини
Стандартизація лікарської рослинної сировини Литология. Кремнистые породы
Литология. Кремнистые породы Электролиз расплавов, водных растворов
Электролиз расплавов, водных растворов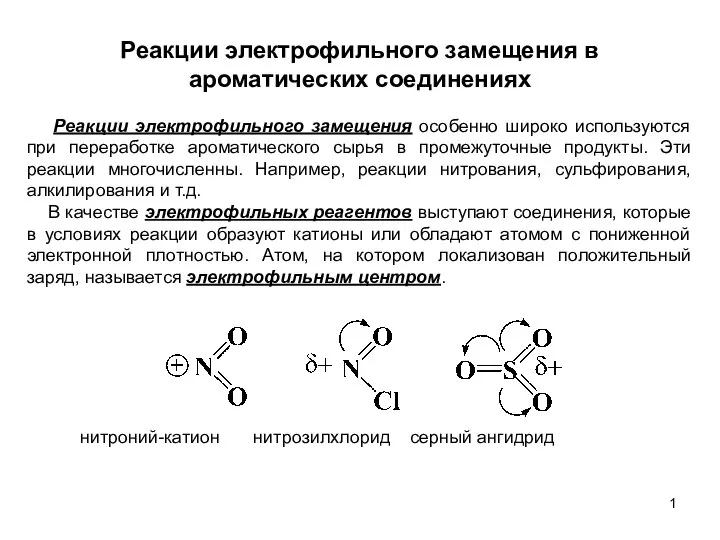 Реакции электрофильного замещения в ароматических соединениях. (Лекция 6)
Реакции электрофильного замещения в ароматических соединениях. (Лекция 6) Лантаноидтар. Лантаноидтардың қасиеттері
Лантаноидтар. Лантаноидтардың қасиеттері Способы получения оксидов, оснований, кислот и солей. Урок №2
Способы получения оксидов, оснований, кислот и солей. Урок №2 Геологические структуры МПИ. Группа доминерализационных структур
Геологические структуры МПИ. Группа доминерализационных структур Презентация по Химии "СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ" - скачать смотреть бесплатно
Презентация по Химии "СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ" - скачать смотреть бесплатно Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.
Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.  Физические величины
Физические величины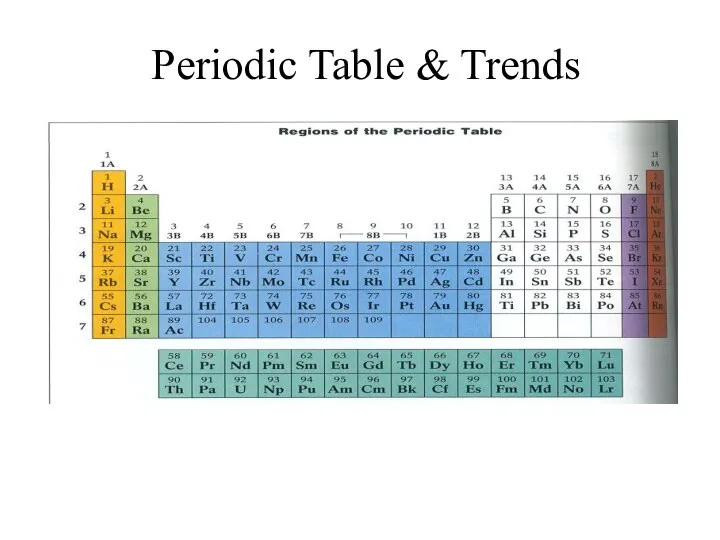 Periodic Table and Trends
Periodic Table and Trends Водород на Земле и в космосе
Водород на Земле и в космосе Образование раствора
Образование раствора Формирование химических знаний при использовании информационных технологий
Формирование химических знаний при использовании информационных технологий Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна
Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна  Правила оформления лабораторных работ
Правила оформления лабораторных работ Выбор и назначение антибиотиков в соответствии со свойствами идентифицированного микроорганизма - возбудителя инфекции
Выбор и назначение антибиотиков в соответствии со свойствами идентифицированного микроорганизма - возбудителя инфекции Влияние этанола на организм человека
Влияние этанола на организм человека Аминокислоты алифатического ряда и их производные
Аминокислоты алифатического ряда и их производные Бензол. Физические и химические свойства
Бензол. Физические и химические свойства Свойства веществ различных классов
Свойства веществ различных классов Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы”
Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы” Темір және оның маңызды қосылыстары
Темір және оның маңызды қосылыстары Полимеры в нашей жизни (10 класс)
Полимеры в нашей жизни (10 класс) Комплексные соединения
Комплексные соединения Йод, химия, 9 класс
Йод, химия, 9 класс