Содержание
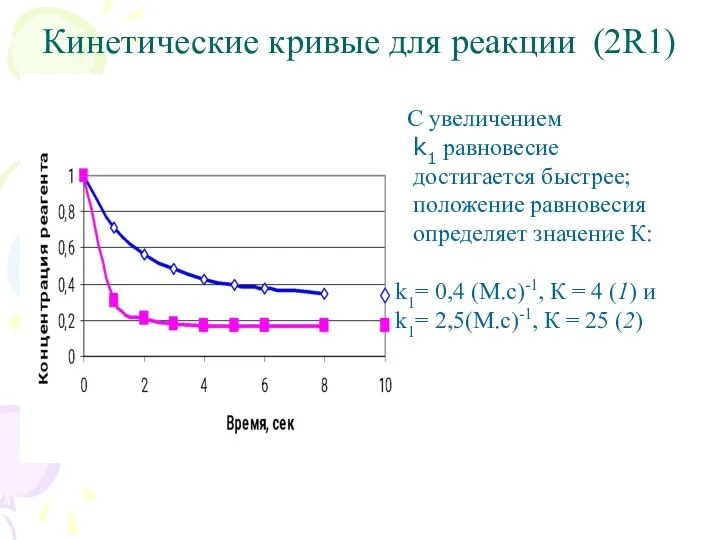
- 2. Кинетические кривые для реакции (2R1) С увеличением k1 равновесие достигается быстрее; положение равновесия определяет значение К:
- 3. 2.2 Параллельные реакции: вещество А превращается по двум (и более) направлениям k1 A ⇒ В и
- 4. 2.3 Последовательные реакции: k1 k2 A → B → D (3.R3) Запишем скорости убыли А и
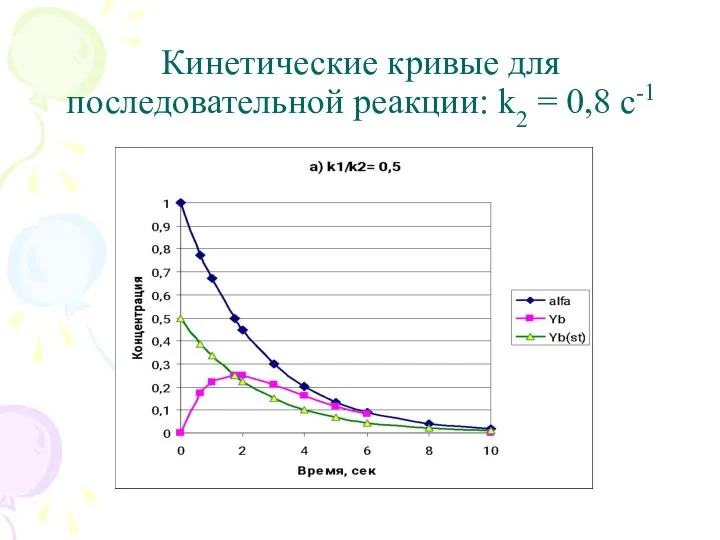
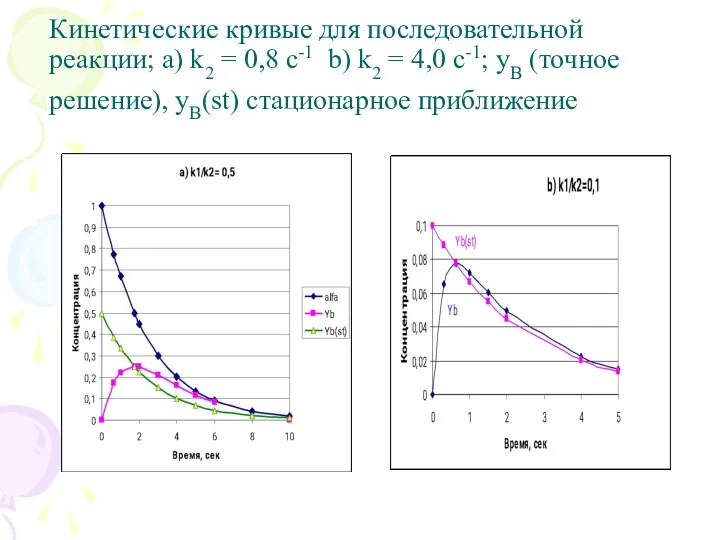
- 5. Кинетические кривые для последовательной реакции: k2 = 0,8 с-1
- 6. Важно: в последовательной схеме селективность по промежуточному продукту является функцией времени. Концентрация промежуточного продукта yB проходит
- 7. Эти особенности кинетики позволяют обосновать схему протекания сложной реакции с использованием критерия относительной селективности (ρ). Если
- 8. Зависимость отношения концентраций [П]/[A] от времени контакта ЦГД-1,2 с (56%Ni-Sn)/SiO2 553К 523К 500К
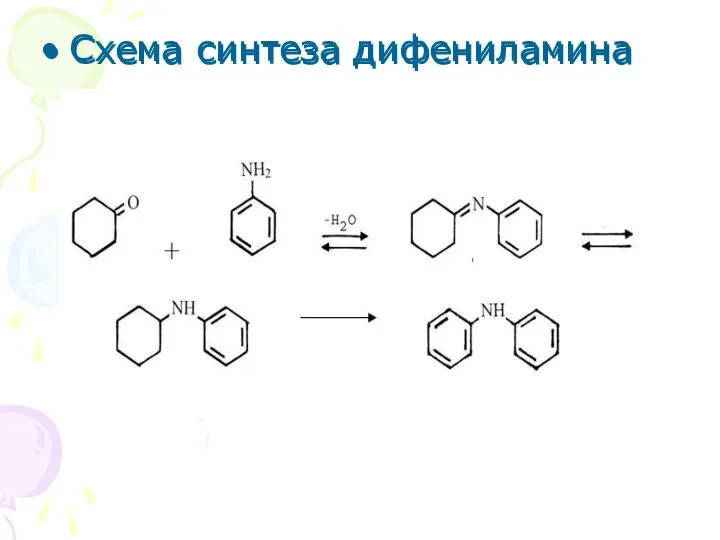
- 9. Схема синтеза дифениламина Схема синтеза дифениламина
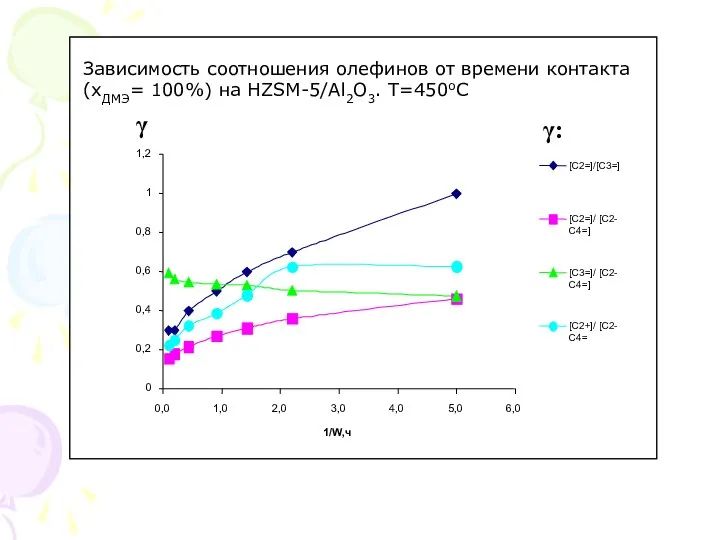
- 10. Зависимость соотношения олефинов от времени контакта (хДМЭ= 100%) на HZSM-5/Al2O3. T=450oC
- 11. Аналитическое решение и быстрый кинетический анализ невозможны для сложных схем реакции. Поэтому используют упрощения при кинетическом
- 12. Применение стационарного приближения позволяет упростить кинетический анализ. Например, система дифференциальных уравнений (3.5) превращается в алгебраические уравнения.
- 13. Кинетические кривые для последовательной реакции; a) k2 = 0,8 с-1 b) k2 = 4,0 с-1; yB
- 14. 2. Допущение о лимитирующей стадии (ЛC) в системе - т.е. предположение о том, что скорость суммарного
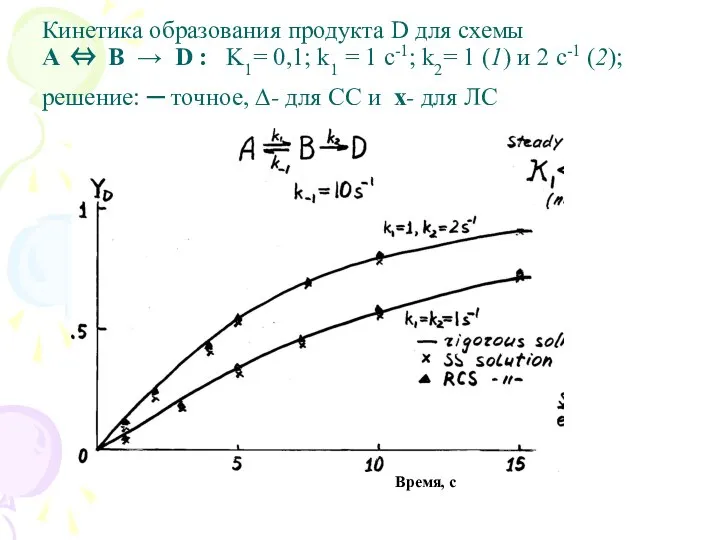
- 15. Кинетика образования продукта D для схемы A ⇔ B → D : K1= 0,1; k1 =
- 16. Лимитирующая стадия (ЛС) При наличии ЛС вся кинетическая информация относится только к этой медленной стадии. До
- 17. Найдем отношение (3.17) и оценим возможность реализации СС, а также время его достижения с точностью 90%.
- 18. Применение стационарного приближения для описания неразветвленной цепной реакции разложение ацетальдегида (А) с образованием метана, СО и
- 19. d[CН3∙]/dt = k1CA- k2CA[CН3∙]+ k3[СН3С∙=О]- k4[СН3∙]2 = 0 d[СН3С∙=О]/dt = k2CA[CН3∙] - k3[СН3С∙=О] = 0 (3.18)
- 20. Этапы разработки формальной кинетической модели процесса Экспериментальное исследование зависимости концентрации реагентов от времени реакции Ci(t), Рассчитывают
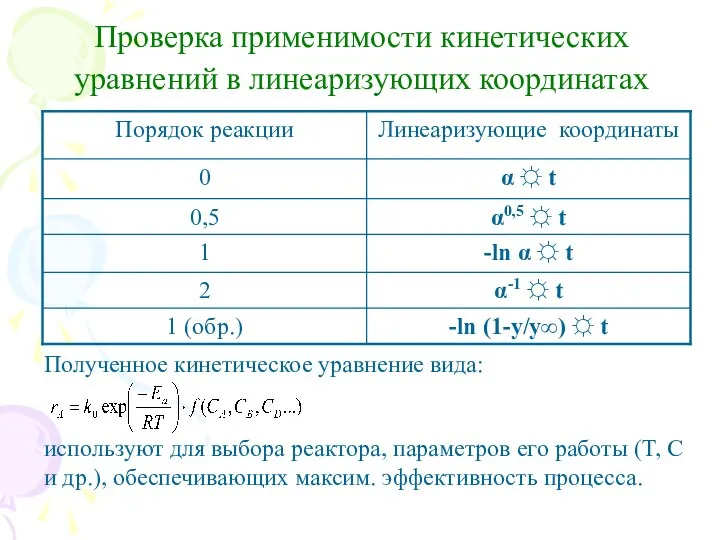
- 21. Проверка применимости кинетических уравнений в линеаризующих координатах Полученное кинетическое уравнение вида: используют для выбора реактора, параметров
- 22. Реакторы химических процессов Подразделяют по способу подачи реагентов на статические (автоклав) и проточные, по профилю концентраций
- 23. Нестационарный режим является нежелательным, особенно в промышленности, поэтому наиболее распространенными являются проточные реакторы, в которых процессы
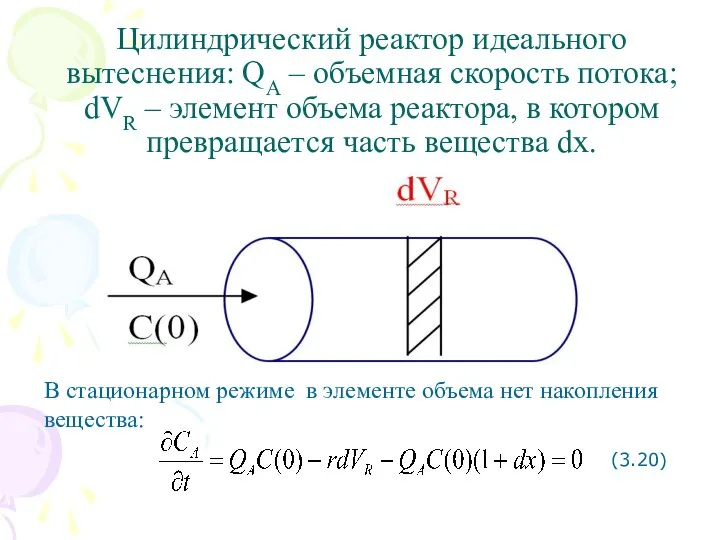
- 24. Цилиндрический реактор идеального вытеснения: QA – объемная скорость потока; dVR – элемент объема реактора, в котором
- 25. откуда rdVR = QAC(0)dx и, разделяя переменные, получим dVR/QA = C(0)dx/r (3.21) С учетом начального условия:
- 27. Скачать презентацию




![Зависимость отношения концентраций [П]/[A] от времени контакта ЦГД-1,2 с (56%Ni-Sn)/SiO2 553К 523К 500К](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1403358/slide-7.jpg)






![d[CН3∙]/dt = k1CA- k2CA[CН3∙]+ k3[СН3С∙=О]- k4[СН3∙]2 = 0 d[СН3С∙=О]/dt = k2CA[CН3∙]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1403358/slide-18.jpg)




 Презентация Химическая связь
Презентация Химическая связь  Колообіг Оксигену в природі
Колообіг Оксигену в природі  Химия и физика полимеров. Курс лекций
Химия и физика полимеров. Курс лекций Металлические элементы группы IA. ЛИТИЙ. Работу выполнила: Ученица 11 класса Иванова Ксения
Металлические элементы группы IA. ЛИТИЙ. Работу выполнила: Ученица 11 класса Иванова Ксения Коллекция учебных динамических слайдов по химии. (8 класс)
Коллекция учебных динамических слайдов по химии. (8 класс) Алканы: гомологический ряд, изомерия и номенклатура алканов. МБОУ СОШ №99 г.о. Самара Предмет: Химия Класс: 10 Учебник: О.С. Габр
Алканы: гомологический ряд, изомерия и номенклатура алканов. МБОУ СОШ №99 г.о. Самара Предмет: Химия Класс: 10 Учебник: О.С. Габр Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Этиленгликоль. Физические свойства
Этиленгликоль. Физические свойства Алкадиены (диены)
Алкадиены (диены) Строение металлов
Строение металлов Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные
Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные Презентация по Химии "КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ" - скачать смотреть бесплатно
Презентация по Химии "КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ" - скачать смотреть бесплатно Властивості газів
Властивості газів Автоматизация производства жидкой углекислоты
Автоматизация производства жидкой углекислоты Electrochemical processes
Electrochemical processes Горные породы Крыма
Горные породы Крыма Азот Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов» Бар
Азот Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов» Бар Металлическая связь
Металлическая связь Алюминий
Алюминий Использование ЭОР при подготовке к ЕГЭ и ГИА
Использование ЭОР при подготовке к ЕГЭ и ГИА Гидролиз. Лекция 03-2
Гидролиз. Лекция 03-2 Несовместимые сочетания лекарственных веществ. Способы преодоления несовместимости
Несовместимые сочетания лекарственных веществ. Способы преодоления несовместимости Полимеры
Полимеры Полимеры. Каучуки. Резина
Полимеры. Каучуки. Резина Счастливы вместе с химией
Счастливы вместе с химией Вода. Физические и химические свойства
Вода. Физические и химические свойства ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ ОБОБЩАЮЩИЙ УРОК
ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ ОБОБЩАЮЩИЙ УРОК  Презентация по Химии "Значение химии" - скачать смотреть бесплатно
Презентация по Химии "Значение химии" - скачать смотреть бесплатно