Содержание
- 6. Образующиеся в результате реакции агрегаты AgI адсорбируют на своей поверхности те ионы, которые способны достраивать кристаллическую
- 7. Часть этих ионов, составляющая адсорбционный слой, прочно удерживается у поверхности ядра за счет электростатических и адсорбционных
- 8. В качестве еще одного примера рассмотрим строение коллоидных частиц (мицелл) сульфата бария, полученного в реакции обмена
- 10. Скачать презентацию
Слайд 2
Слайд 3
Слайд 4
Слайд 5
Слайд 6
Образующиеся в результате реакции агрегаты AgI адсорбируют на своей поверхности те
Образующиеся в результате реакции агрегаты AgI адсорбируют на своей поверхности те
ионы, которые способны достраивать кристаллическую решетку AgI (правило Панета – Фаянса).
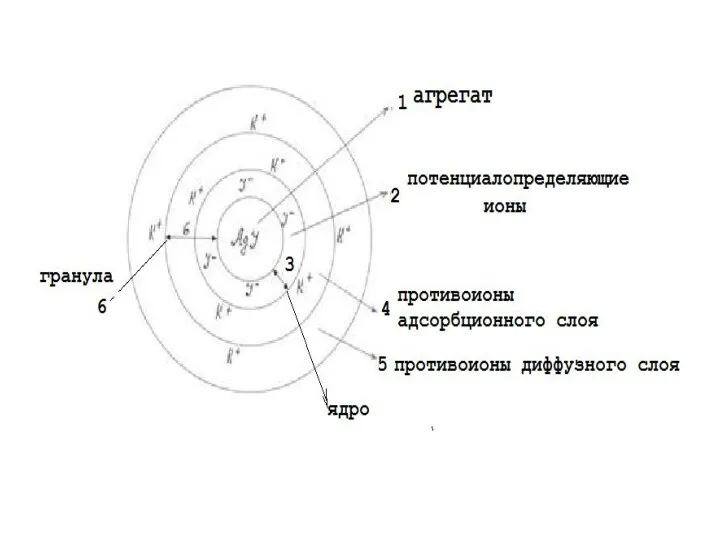
В данном случае ионы I- взяты в недостатке, поэтому агрегат AgI адсорбирует ионы Ag+. Ионы Ag+, сообщившие поверхности этот заряд называются потенциалопределяющими ионами (ПОИ), так как эти ионы определяют знак заряда коллоидной частицы.
К положительно заряженной поверхности образовавшегося ядра мицеллы притягиваются ионы противоположного знака – противоионы (ионы NO3-).
В данном случае ионы I- взяты в недостатке, поэтому агрегат AgI адсорбирует ионы Ag+. Ионы Ag+, сообщившие поверхности этот заряд называются потенциалопределяющими ионами (ПОИ), так как эти ионы определяют знак заряда коллоидной частицы.
К положительно заряженной поверхности образовавшегося ядра мицеллы притягиваются ионы противоположного знака – противоионы (ионы NO3-).
Слайд 7
Часть этих ионов, составляющая адсорбционный слой, прочно удерживается у поверхности ядра
Часть этих ионов, составляющая адсорбционный слой, прочно удерживается у поверхности ядра
за счет электростатических и адсорбционных сил. Ядро вместе с адсорбционным слоем составляет коллоидную частицу. В данном примере она заряжена положительно (так же, как ПОИ).
Слайд 8
В качестве еще одного примера рассмотрим строение коллоидных частиц (мицелл)
В качестве еще одного примера рассмотрим строение коллоидных частиц (мицелл)
сульфата бария, полученного в реакции обмена между сульфатом калия и хлоридом бария:
Na2SO4 + BaCl2 = BaSO4 + 2 NaCl
Для получения устойчивого золя необходимо, чтобы один из электролитов (Na2SO4 или BaCl2) присутствовал в избытке в качестве стабилизатора.
В этих условиях нерастворимое вещество не выпадает в осадок, а переходит в коллоидное состояние – образуется золь. Нерастворимое вещество, образовавшееся в результате реакции, называют зародышем или агрегатом и обозначают
BaSO4 . Коэффициент m указывает число частиц вещества.
Na2SO4 + BaCl2 = BaSO4 + 2 NaCl
Для получения устойчивого золя необходимо, чтобы один из электролитов (Na2SO4 или BaCl2) присутствовал в избытке в качестве стабилизатора.
В этих условиях нерастворимое вещество не выпадает в осадок, а переходит в коллоидное состояние – образуется золь. Нерастворимое вещество, образовавшееся в результате реакции, называют зародышем или агрегатом и обозначают
BaSO4 . Коэффициент m указывает число частиц вещества.






 ФОСФОР Абдуллина Альфия Ахнафовна учитель химии МБОУ СОШ с.Никифарово МР Альшеевский район РБ
ФОСФОР Абдуллина Альфия Ахнафовна учитель химии МБОУ СОШ с.Никифарово МР Альшеевский район РБ  Соединения галогенов
Соединения галогенов Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Что объединяет вещества. Классификация твёрдых веществ
Что объединяет вещества. Классификация твёрдых веществ Химическая физика горения
Химическая физика горения Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н
Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н Кольцевые силикаты
Кольцевые силикаты Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Кислоты. Индикаторы
Кислоты. Индикаторы Химическая промышленность
Химическая промышленность Алициклические и гетероциклические соединения. Тема № 7, 8
Алициклические и гетероциклические соединения. Тема № 7, 8 Производные карбоновых кислот
Производные карбоновых кислот Жир жиру рознь. Супер омега 3
Жир жиру рознь. Супер омега 3 Экстракция
Экстракция Серная кислота H2SO4
Серная кислота H2SO4 Хроматографія. Мікрогетерогенні дисперсні системи
Хроматографія. Мікрогетерогенні дисперсні системи Строение мицеллы лиофобного золя
Строение мицеллы лиофобного золя Генетическая связь между основными классами органических соединений
Генетическая связь между основными классами органических соединений Презентация по Химии "Фотосинтез" - скачать смотреть
Презентация по Химии "Фотосинтез" - скачать смотреть  Презентация по Химии "Ток в электролитах" - скачать смотреть
Презентация по Химии "Ток в электролитах" - скачать смотреть  Способы разделения смесей
Способы разделения смесей Презентация по Химии "Химические знаки и их история" - скачать смотреть
Презентация по Химии "Химические знаки и их история" - скачать смотреть  Диаграммы состояния сплавов. Диаграмма состояния Fe-C (Fe-Fe3C). Лекция №2
Диаграммы состояния сплавов. Диаграмма состояния Fe-C (Fe-Fe3C). Лекция №2 Обмен веществ. Метаболизм и его функции
Обмен веществ. Метаболизм и его функции Растворы неэлектролитов. Закон Вант- Гоффа и Рауля. Растворы электролитов. Теория электронной диссоциации
Растворы неэлектролитов. Закон Вант- Гоффа и Рауля. Растворы электролитов. Теория электронной диссоциации Окислительно-восстановительные реакции в растворах
Окислительно-восстановительные реакции в растворах Переваривание и всасывание жиров
Переваривание и всасывание жиров Фосфор
Фосфор