Содержание
- 2. План лекции Устойчивость коллоидных растворов, ее виды Коагуляция коллоидных растворов электролитами Правило Шульце-Гарди Кинетика коагуляции Взаимная
- 3. Гидрофобные коллоидные растворы Обладают большой удельной поверхностью раздела между дисперсной фазой и дисперсионной средой Большой избыточной
- 4. Кинетическая устойчивость Способность дисперсных частиц удерживаться во взвешенном состоянии под влиянием броуновского движения и противостоять действию
- 5. Агрегативная устойчивость Способность частиц дисперсной фазы поддерживать определенную степень дисперсности (препятствовать образованию агрегатов) Факторы агрегативной устойчивости:
- 6. Теория устойчивости и коагуляции гидрофобных золей (Дерягин и Ландау) Силы межмолекулярного притяжения – способствуют агрегации частиц
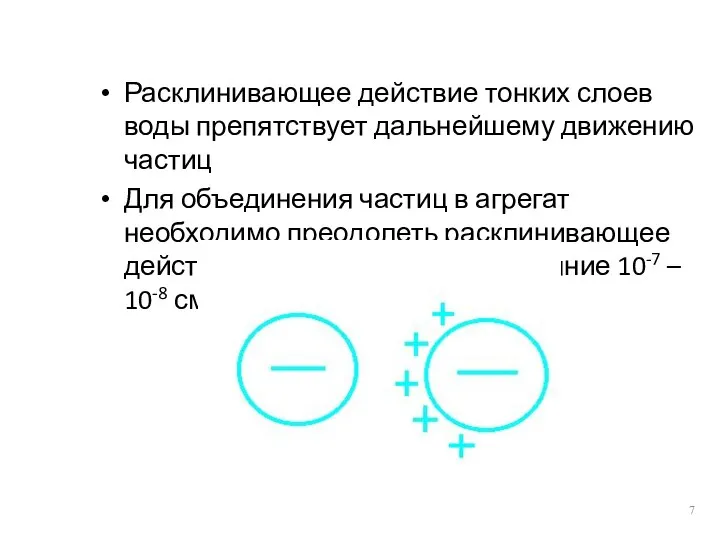
- 7. Расклинивающее действие тонких слоев воды препятствует дальнейшему движению частиц Для объединения частиц в агрегат необходимо преодолеть
- 8. Коагуляция Процесс объединения частиц в более крупные агрегаты Скорость коагуляции тем больше, чем меньше ς -
- 9. Факторы влияющие на скорость коагуляции Температура Концентрация золя Электрический ток Лучистая энергия Добавление электролитов
- 10. Коагуляция золей электролитами Коагулирующим действием в электролите обладают те ионы, которые имеют заряд, противоположный заряду гранул
- 11. Правило значности Шульце-Гарди Коагулирующая сила иона тем больше, чем больше его заряд Коагулирующая способность двухзарядных ионов
- 12. Коагулирующая способность ионов зависит От способности ионов адсорбироваться на коллоидных частицах От степени гидратации Лиотропные ряды:
- 13. Механизм коагулирующего действия ионов Сжатие диффузного слоя противоионов Избирательная адсорбция ионов Уменьшение ς - потенциала Уменьшение
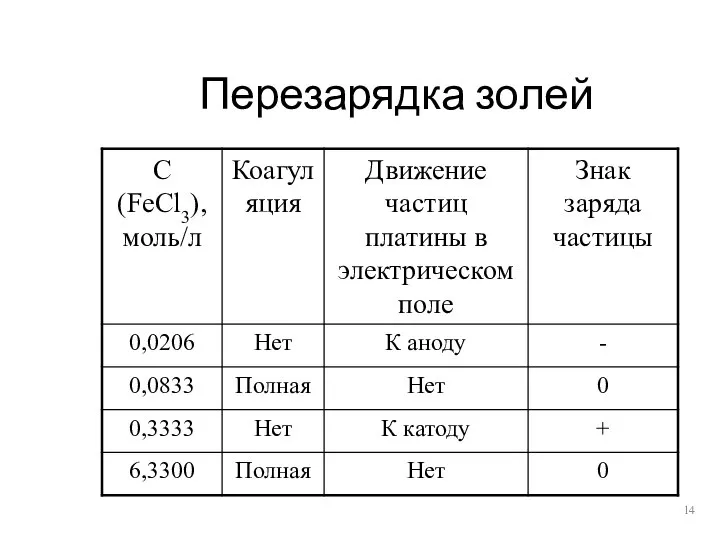
- 14. Перезарядка золей
- 15. Перезарядка наблюдается при добавлении, как правило, многозарядных ионов. Они обладают большой адсорбирующей способностью Избыток ионов Fe3+
- 16. Кинетика коагуляции Скрытая коагуляция – при увеличении концентрации электролита начинается образование частиц низших порядков Явная коагуляция
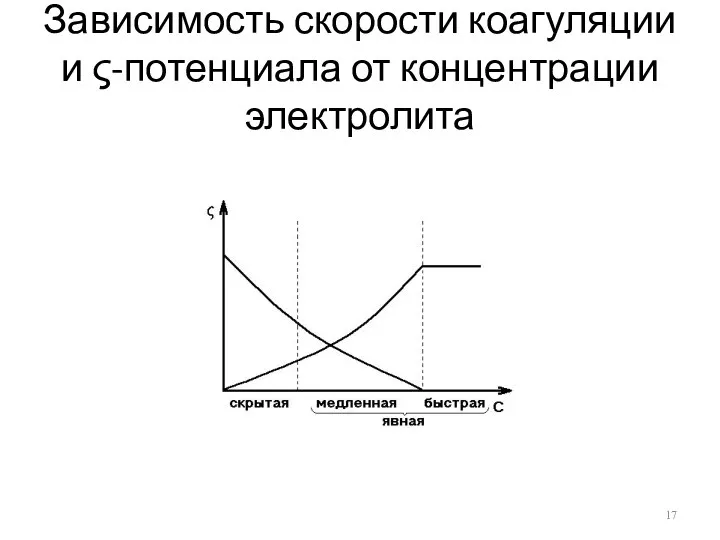
- 17. Зависимость скорости коагуляции и ς-потенциала от концентрации электролита
- 18. Коагуляция смесями электролитов Аддитивность (суммирование) – коагулирующий эффект от двух электролитов равен сумме эффектов каждого из
- 20. Явление привыкания При медленном добавлении электролита, или порциями через большие промежутки времени, коагуляция может не наступить
- 21. Взаимная коагуляция золей Происходит, если смешать два коллоидных раствора, у которых частицы имеют противоположный заряд Применяется:
- 22. Коллоидная защита При добавлении к гидрофобному золю высокомолекулярных веществ происходит их адсорбция на коллоидных частицах и
- 23. «Золотое число» (железное, серебряное, рубиновое) Число мг сухого высокомолекулярного вещества, которое нужно добавить к 10 мл
- 25. Скачать презентацию



















 СПИРТЫ Урок химии в 9-10 классе
СПИРТЫ Урок химии в 9-10 классе Методы экстрагирования ЛРС и оборудование
Методы экстрагирования ЛРС и оборудование Количество вещества
Количество вещества Капроновая (гексановая) кислота
Капроновая (гексановая) кислота Химия. 8 класс. Введение в химию
Химия. 8 класс. Введение в химию История и методология химии
История и методология химии Растворы. Свойства растворов. (Тема 3)
Растворы. Свойства растворов. (Тема 3) Металлы. Строение, свойства, применение
Металлы. Строение, свойства, применение Свойство металлов и сплавов
Свойство металлов и сплавов Օզոն. Օզոնային շերտ
Օզոն. Օզոնային շերտ 6-членные гетероциклы с одним гетероатомом
6-членные гетероциклы с одним гетероатомом Макро- и микроэлементы
Макро- и микроэлементы Обмен холестерола
Обмен холестерола Производные морфинана (фенантренизохинолина)
Производные морфинана (фенантренизохинолина) Рука руку моет. Механизм двух реакций
Рука руку моет. Механизм двух реакций Презентация по Химии "Неметаллы.Применение неметаллов" - скачать смотреть
Презентация по Химии "Неметаллы.Применение неметаллов" - скачать смотреть  Одноатомні спирти Підготували Учениці 9-Б класу
Одноатомні спирти Підготували Учениці 9-Б класу  Składniki odżywcze
Składniki odżywcze Химическая связь
Химическая связь Катализ. Лекция 1
Катализ. Лекция 1 Щелочные металлы
Щелочные металлы Влияние условий на скорость химической реакции
Влияние условий на скорость химической реакции Физические свойства металлов: пластичность, электропроводность, теплопроводность, металлический блеск, плотность
Физические свойства металлов: пластичность, электропроводность, теплопроводность, металлический блеск, плотность Электроотрицательность (ЭО). Ковалентная связь
Электроотрицательность (ЭО). Ковалентная связь Производные ксантина (дипрофиллин, ксантинола никотинат, пентоксифиллин) и гедантоина (фенитоин)
Производные ксантина (дипрофиллин, ксантинола никотинат, пентоксифиллин) и гедантоина (фенитоин) Презентация по Химии "Всё о соли" - скачать смотреть
Презентация по Химии "Всё о соли" - скачать смотреть  Олиго- и полисахариды
Олиго- и полисахариды Микроэлементы
Микроэлементы