ВОДОРОД Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов»
Содержание
- 2. Выделение горючего газа при взаимодействии кислот и металлов наблюдали в XVI и XVII веках на заре
- 3. Обычный водородный атом (протий) состоит из двух фундаментальных частиц (протона и электрона) и имеет атомную массу
- 4. На электронной орбите атома водорода могут находиться 2 электрона, поэтому водород способен также принимать электрон, образуя
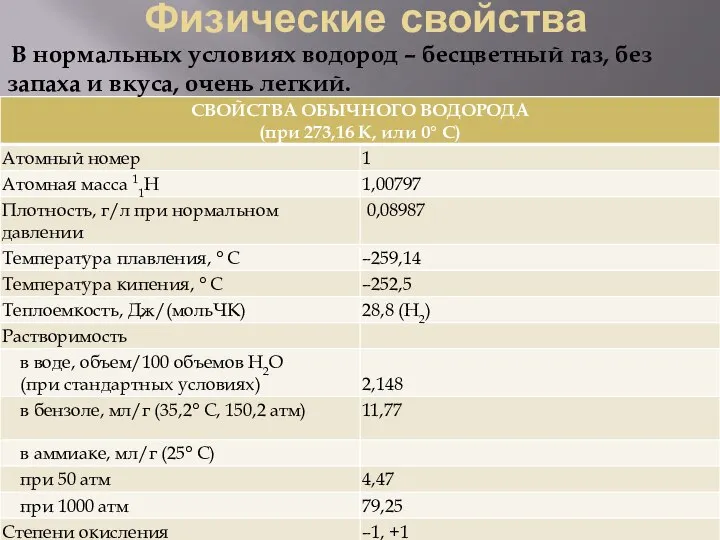
- 5. Физические свойства В нормальных условиях водород – бесцветный газ, без запаха и вкуса, очень легкий.
- 6. Правила обращения Водород при смеси с воздухом образует взрывоопасную смесь — так называемый гремучий газ. Наибольшую
- 7. Химические свойства при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя
- 8. С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например
- 9. Взаимодействие со щелочными и щёлочноземельными металлами При взаимодействии с активными металлами водород образует гидриды: 2Na +
- 10. Получение водорода В промышленности 1.Электролиз водных растворов солей: 2NaCl + 2H2O → H2↑ + 2NaOH +
- 11. В лаборатории 1.Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и
- 12. 4.Действие щелочей на цинк или алюминий: 2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑ Zn
- 13. Водород в природе Водород — самый распространённый элемент во Вселенной. На его долю приходится около 92
- 15. Скачать презентацию











 Общее понятие напряженно – деформированного состояния деталей машин из металлических материалов, применяемых в машиностроении
Общее понятие напряженно – деформированного состояния деталей машин из металлических материалов, применяемых в машиностроении Дисперсные наполнители. Пневмогидрокомпрессионное формование. Магнитоимпульсное формование
Дисперсные наполнители. Пневмогидрокомпрессионное формование. Магнитоимпульсное формование Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Карбоновые кислоты
Карбоновые кислоты Периодическая система Д.И. Менделеева (Занятие 3)
Периодическая система Д.И. Менделеева (Занятие 3) Хімічнi елементи
Хімічнi елементи Растворение. Растворяемость. Типы растворов
Растворение. Растворяемость. Типы растворов Методы восстановления и окисления
Методы восстановления и окисления Физико-химия поверхностных явлений
Физико-химия поверхностных явлений Красители для волос. Первая группа
Красители для волос. Первая группа Комбинированные задачи. 11 класс. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Комбинированные задачи. 11 класс. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Кристаллические системы
Кристаллические системы Предмет химии. Основные задачи курса
Предмет химии. Основные задачи курса Презентация по Химии "Серная кислота – хлеб химии" - скачать смотреть
Презентация по Химии "Серная кислота – хлеб химии" - скачать смотреть 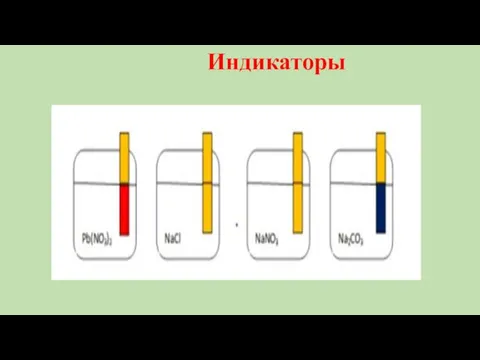 Вещества и материалы. Классификация веществ. Индикаторы. 6 класс
Вещества и материалы. Классификация веществ. Индикаторы. 6 класс Презентация по Химии "Физические и химические свойства кислот. 8-й класс" - скачать смотреть
Презентация по Химии "Физические и химические свойства кислот. 8-й класс" - скачать смотреть  Нефелиновые сиениты. Щелочные породы
Нефелиновые сиениты. Щелочные породы Основные классы органических соединений и их роль в живых организмах
Основные классы органических соединений и их роль в живых организмах Лигандообменные равновесия и процессы. Строение комплексных соединений
Лигандообменные равновесия и процессы. Строение комплексных соединений Олимпиада по химии
Олимпиада по химии Железо
Железо Важнейшие бинарные соединения
Важнейшие бинарные соединения Виникнення процесу горіння. Самоспалахування. Фактори, що впливають на температуру самоспалахування. (Розділ 2.4.5)
Виникнення процесу горіння. Самоспалахування. Фактори, що впливають на температуру самоспалахування. (Розділ 2.4.5) Влияние обработки семян фасоли растворами химических веществ на рост и развитие растений
Влияние обработки семян фасоли растворами химических веществ на рост и развитие растений Полісахариди харчових продуктів і їх властивості. Лекція 4
Полісахариди харчових продуктів і їх властивості. Лекція 4 Характеристики раствора Вкус Цвет Что растворено (раствор сахара, соли, спирта, уксусной кислоты и т.д.) Что является растворител
Характеристики раствора Вкус Цвет Что растворено (раствор сахара, соли, спирта, уксусной кислоты и т.д.) Что является растворител Основания. Классификация оснований
Основания. Классификация оснований Значение химии в жизни человека
Значение химии в жизни человека