Содержание
- 2. Ионная связь Возникает за счет электростатического притяжения + и – ионов друг к другу. Рассмотрим,как образуются
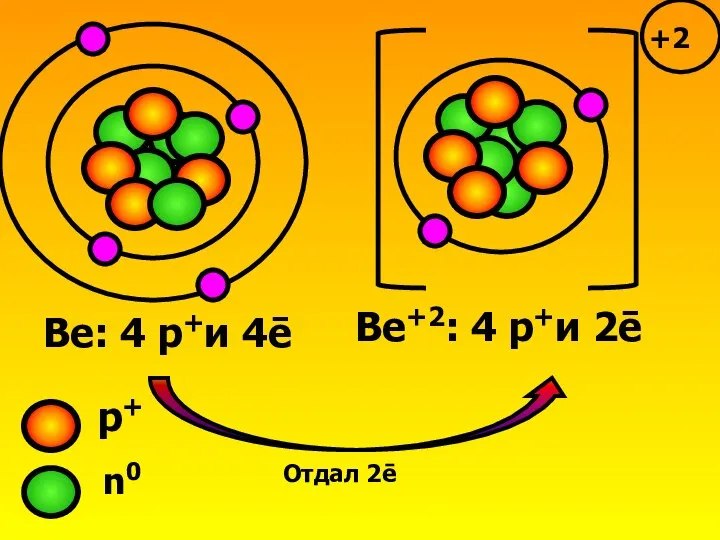
- 3. Ве: 4 р+и 4ē Ве+2: 4 р+и 2ē Отдал 2ē р+ n0 +2
- 4. Запомни! Бериллий приобрел ē-оболочку благородного газа гелия, но сам гелием не стал! У него остался прежним
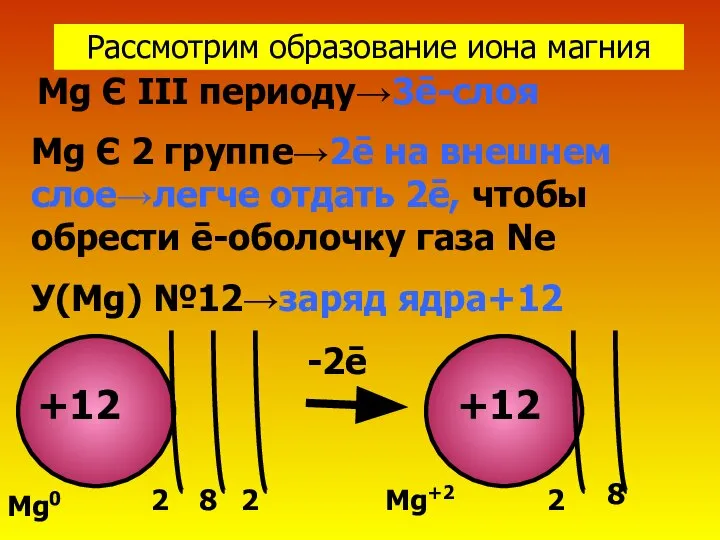
- 5. Рассмотрим образование иона магния Mg Є III периоду→3ē-слоя Mg Є 2 группе→2ē на внешнем слое→легче отдать
- 6. 2 способ Если у атома много ē на внешнем ē-слое ,то легче их у кого-то “взять”.Это
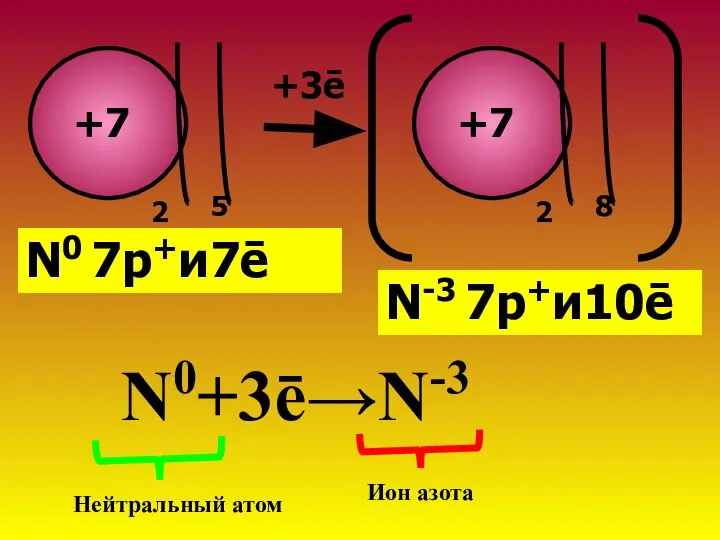
- 7. Атом водорода приобрел ē-оболочку благородного газа Не.У него ē>,чем р+→заряд частицы Рассмотрим образование иона азота: N
- 8. +7 2 5 +7 2 8 +3ē N0 7р+и7ē N-3 7р+и10ē N0+3ē→N-3 Нейтральный атом Ион азота
- 9. Встречаются атомы Na и Cl Na Є III периоду→3ē-слоя Na Є 1 группе→1ē на внешнем слое→легче
- 10. 8 2 1 +11 8 2 7 +17 Отдал 1 ē Na0 Cl0 8 2 0
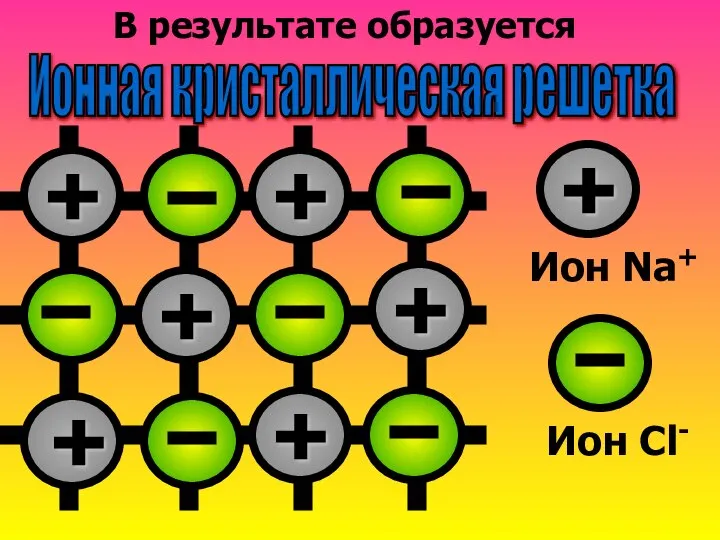
- 11. В результате образуется Ионная кристаллическая решетка + + + + + + + Ион Na+ Ион
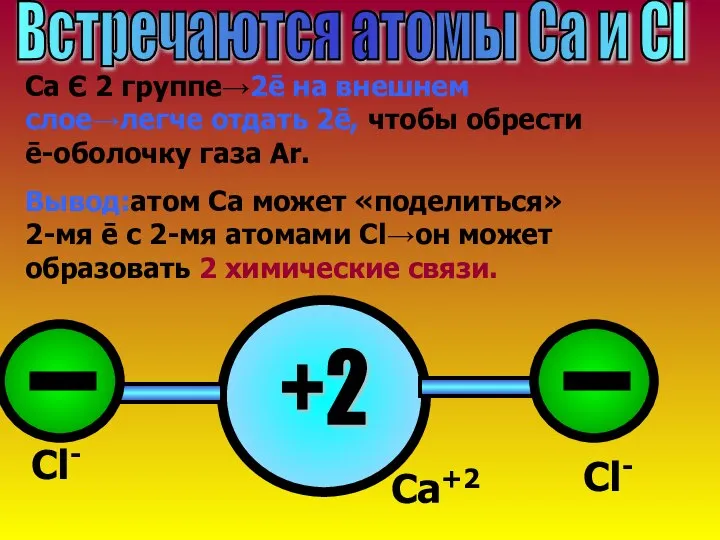
- 12. Встречаются атомы Ca и Cl Ca Є 2 группе→2ē на внешнем слое→легче отдать 2ē, чтобы обрести
- 13. Запомни! Ионная связь образуется по принципу «отдай-возьми ē»→атом может образовать столько химических связей, сколько может отдать
- 14. Запомни! «+» заряженный ион называется катион, а «-»заряженный ион называется анион. Для двух девчат подарков груз
- 15. Ковалентная связь Возникает за счет образования общих электронных пар. Запомни! Такой вид связи возникает между атомами
- 16. Встречаются атомы Cl Cl Є 7 группе→7ē на внешнем слое→ не хватает 1ē, чтобы обрести ē-оболочку
- 17. Запомни! Атом неметалла способен образовывать столько общих ē-пар(→химических связей), сколько у него имеется неспаренных ē-нов.Число неспаренных
- 18. Встречаются атомы О (О) Є 6 группе→6ē на внешнем слое→ не хватает 2ē, чтобы обрести ē-оболочку
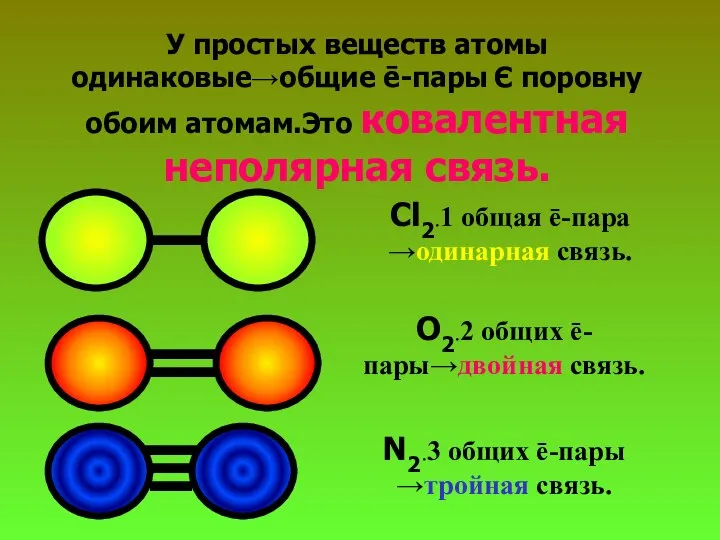
- 19. У простых веществ атомы одинаковые→общие ē-пары Є поровну обоим атомам.Это ковалентная неполярная связь. Cl2.1 общая ē-пара
- 20. У сложных веществ атомы разные→общие ē-пары Є непоровну обоим атомам.Это ковалентная полярная связь. Запомни! Для того,
- 21. электроотрицательность Это способность атомов притягивать к себе общие ē-пары.Полинг разработал шкалу ЭО для неметаллов. H, As,
- 22. Встречаются атомы Н и Сl ЭО (Сl)>ЭО(Н) →общая ē-пара будет смещена к атому (Сl)→на атоме (Сl)
- 23. Встречаются атомы Н и О (О) Є 6 группе→6ē на внешнем слое→ не хватает 2ē, чтобы
- 24. Запомни! Для удобства расчетов как в случае ионной, так и в случае ковалентной полярной связи принято
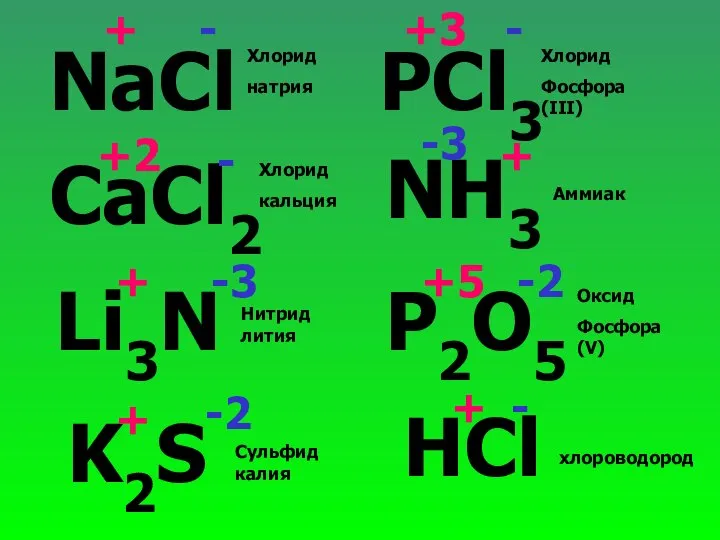
- 25. NaCl CaCl2 Li3N K2S PCl3 NH3 P2O5 HCl + + +2 + + + +3 +5
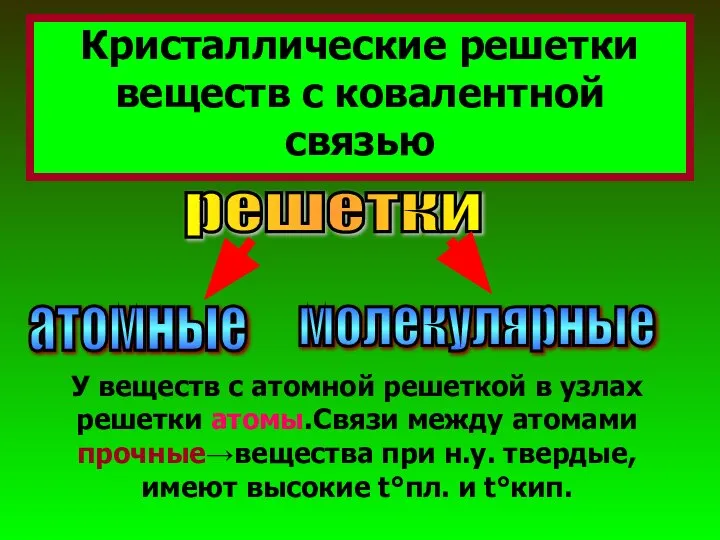
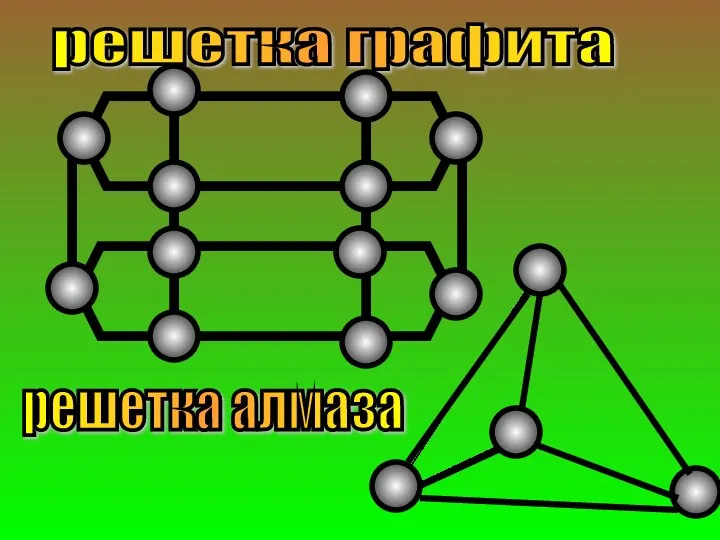
- 26. Кристаллические решетки веществ с ковалентной связью решетки атомные молекулярные У веществ с атомной решеткой в узлах
- 27. решетка графита решетка алмаза
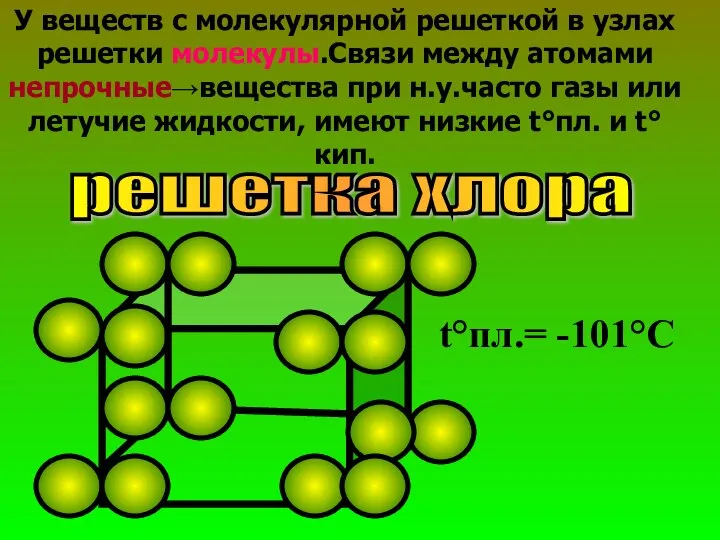
- 28. У веществ с молекулярной решеткой в узлах решетки молекулы.Связи между атомами непрочные→вещества при н.у.часто газы или
- 30. Скачать презентацию

















 Химический элемент таблицы Менделеева - Азот
Химический элемент таблицы Менделеева - Азот Химия аминокислот, пептидов и белков
Химия аминокислот, пептидов и белков Химическая связь в комплексных соединениях
Химическая связь в комплексных соединениях Буферные системы
Буферные системы Жуғыш заттар және жуғыш әсері. 1 Лекция
Жуғыш заттар және жуғыш әсері. 1 Лекция МЕТАЛЛЫ диктант 9 класс
МЕТАЛЛЫ диктант 9 класс  Поліетилен
Поліетилен Виртуозы химического эксперимента
Виртуозы химического эксперимента АЛКАНЫ Строение молекулы метана. Свойства метана и его гомологов.
АЛКАНЫ Строение молекулы метана. Свойства метана и его гомологов.  Реакции окисления и восстановления биоорганических соединений. (Лекция 5)
Реакции окисления и восстановления биоорганических соединений. (Лекция 5) Свойства соли. Эксперимент по выращиванию кристаллов соли
Свойства соли. Эксперимент по выращиванию кристаллов соли Пластмаси
Пластмаси  Химия - основы общей химии (теория)
Химия - основы общей химии (теория) Неравновесные электрохимические методы. Вольтамперометрия
Неравновесные электрохимические методы. Вольтамперометрия Клиническая биохимия азотистого обмена. (Лекция 7)
Клиническая биохимия азотистого обмена. (Лекция 7) Физические и химические свойства воды
Физические и химические свойства воды Эластомеры (резины)
Эластомеры (резины) Аминокислоты. Свойства
Аминокислоты. Свойства Минералогия и кристаллография
Минералогия и кристаллография Теория строения органических соединений А.М. Бутлерова. Классы органических соединений. Тема 1
Теория строения органических соединений А.М. Бутлерова. Классы органических соединений. Тема 1 Изучение свойств горных пород, минералов и полезных ископаемых
Изучение свойств горных пород, минералов и полезных ископаемых Пиролиз
Пиролиз Химическая кинетика
Химическая кинетика Промышленное получение аммиака
Промышленное получение аммиака Physical chemistry of surface phenomena. Basics of adsorptive therapy
Physical chemistry of surface phenomena. Basics of adsorptive therapy Предмет органической химии
Предмет органической химии План: Основні відомості Формули основ Назви основ Класифікація Фізичні властивості Хімічні властивості Способи добування
План: Основні відомості Формули основ Назви основ Класифікація Фізичні властивості Хімічні властивості Способи добування  Азот
Азот