Содержание
- 2. Химическая термодинамика рассматривает энергетические аспекты различных процессов и определяет условия их самопроизвольного протекания.
- 4. – это все, что находится в прямом или косвенном контакте с системой. Окружающая среда Система –
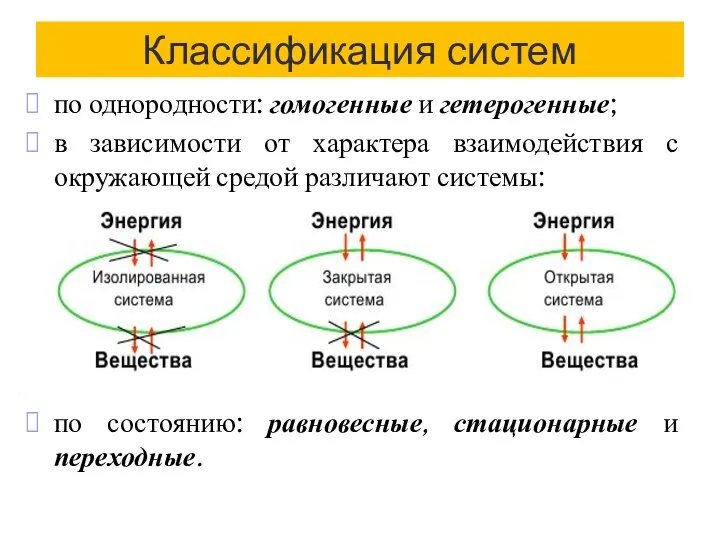
- 5. Классификация систем по однородности: гомогенные и гетерогенные; в зависимости от характера взаимодействия с окружающей средой различают
- 6. Т/д равновесное состояние - const всех свойств во времени и отсутствие потока вещества и энергии в
- 7. Совокупность всех физических и химических свойств системы называют состоянием системы. Его характеризуют термодинамическими параметрами, которые бывают:
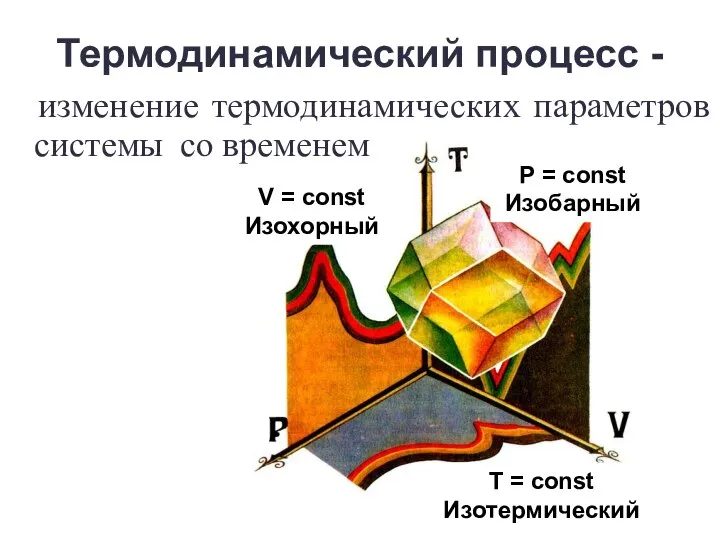
- 8. Термодинамический процесс - изменение термодинамических параметров системы со временем
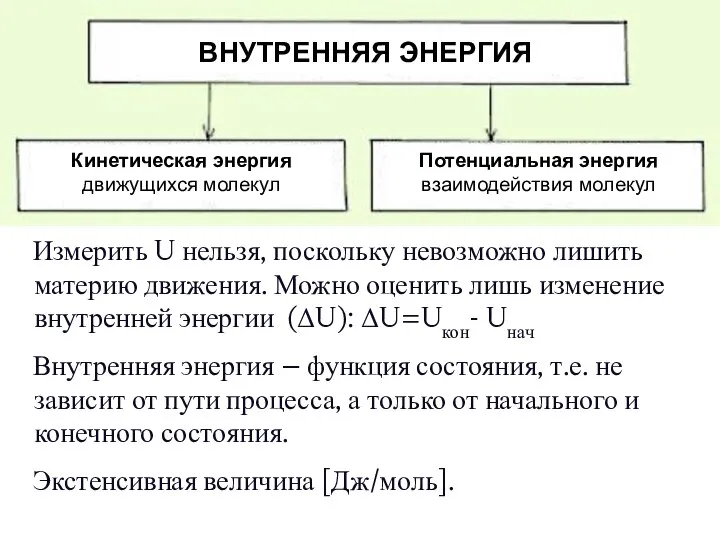
- 9. Измерить U нельзя, поскольку невозможно лишить материю движения. Можно оценить лишь изменение внутренней энергии (ΔU): ΔU=Uкон-
- 10. Теплота и работа Теплота (Q) - хаотический вид передачи энергии Работа (W) – направленный вид передачи
- 11. Первое начало термодинамики
- 12. Формулировки 2.Энергия изолированной системы постоянна. 3. Вечный двигатель I рода невозможен, т.е. машина, производящая работу без
- 13. Математический вид: Q=ΔU + W= ΔU + pΔV Количество теплоты, подведенное к системе, идет на изменение
- 14. Первый закон термодинамики в применении к некоторым процессам Изотермические процессы (Т = const): U = const,
- 15. Закон Гесса Тепловой эффект реакции не зависит от пути процесса ,а зависит только начальным и конечным
- 16. Следствия из закона Гесса 1. ΔНр-ии =∑νΔH0обр(прод) - ∑νΔH0обр(исх) Стандартной энтальпией образования (ΔH0обр ) - тепловой
- 17. 2. ΔНр-ии= ∑νΔ H0сгор(исх) - ∑νΔH0сгор (прод) Стандартная энтальпия сгорания (ΔH0сгор ) - тепловой эффект (изменение
- 18. Второе начало термодинамики
- 19. I закон термодинамики дает данные лишь о тепловом выделении и говорит о превращении одной формы энергии
- 20. Формулировки второго закона термодинамики Теплота не может самопроизвольно переходить от более холодного тела к более горячему
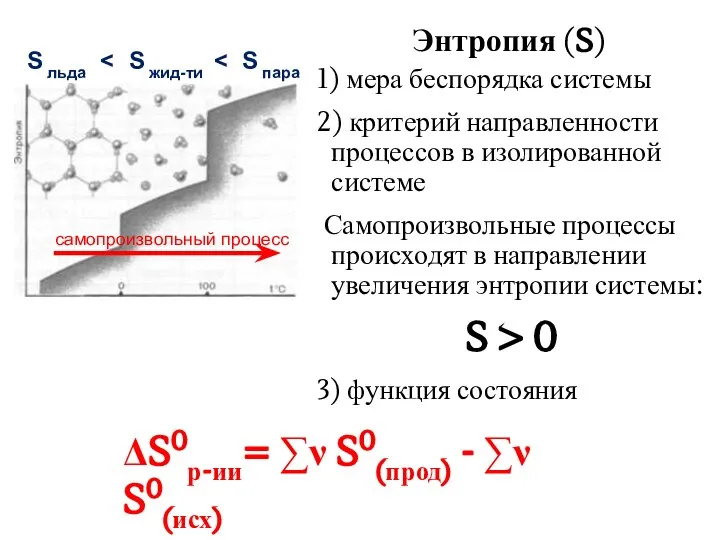
- 21. Энтропия (S) 1) мера беспорядка системы 2) критерий направленности процессов в изолированной системе Самопроизвольные процессы происходят
- 22. Термодинамические потенциалы критерии направленности процессов в открытой и закрытой системах: энергия Гиббса энергия Гельмгольца Расчет энергии
- 23. Биохимические реакции, сопровождающиеся уменьшением энергии Гиббса, называются экзергоническими реакциями. Биохимические реакции, сопровождающиеся увеличением энергии Гиббса, называются
- 24. Кинетика и катализ
- 25. Химическая кинетика изучает скорость и механизм химических реакций и зависимость их от различных факторов.
- 26. Скорость химической реакции – изменение количества вещества в единицу времени в единице объема (для гомогенных) или
- 28. Закон действующих масс (К. Гульдберг и П. Вааге) Скорость хим. реакции прямо пропорциональна произведению концентраций реагирующих
- 29. 2CO(г)+О2(г)= О2(г) Кинетическое уравнение химической реакции Общий порядок равен: n = 2 + 1 = 3.
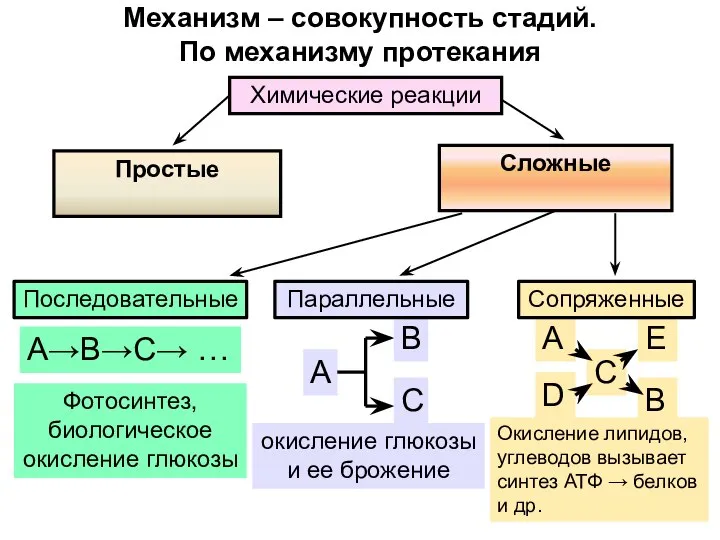
- 30. Механизм – совокупность стадий. По механизму протекания
- 31. Простые реакции – одна стадия; стехиометрическое уравнение отражает реальный ход процесса NO2 + NO2 → N2O4
- 32. Механизм процесса характеризует молекулярность реакции - число молекул(частиц), участвующих в элементарном акте реакции. Реакции делятся на:
- 33. Для простых реакций: порядок = молекулярности 2NO2 → N2O4 Молекулярность – 2 Для сложных реакций: порядок
- 34. Правило Вант – Гоффа: При обычных температурах (Т где γ = 2 ÷ 4 (температурный коэффициент).
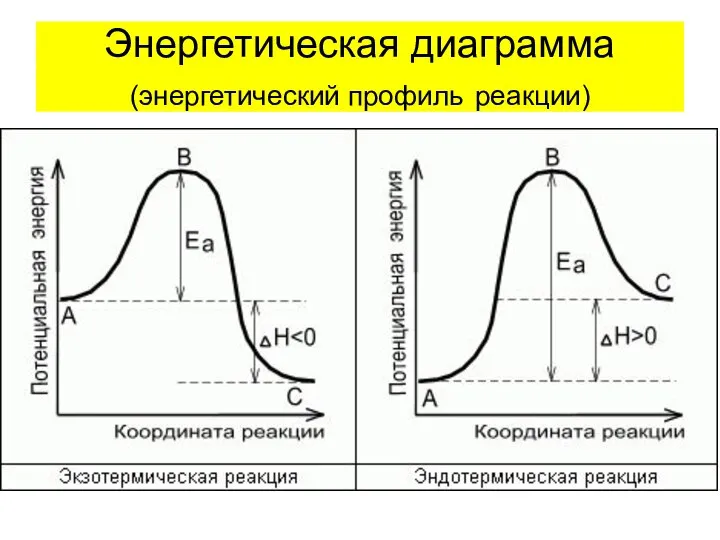
- 36. Энергетическая диаграмма (энергетический профиль реакции)
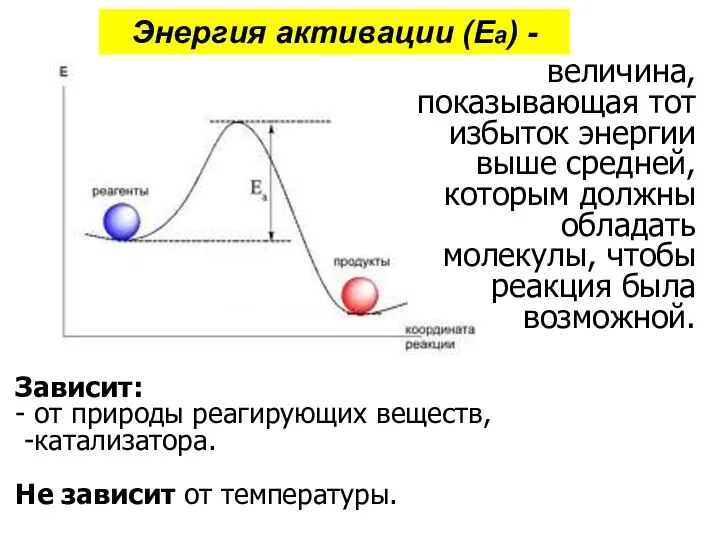
- 37. Энергия активации (Еа) - величина, показывающая тот избыток энергии выше средней, которым должны обладать молекулы, чтобы
- 40. присутствие катализаторов или ингибиторов Й. Я. Берцелиус ввел термин «катализ». В. Оствальд Нобелевская премия «в признание
- 41. Положительный и отрицательный, (когда скорость реакции уменьшается, в таком случае катализатор называют ингибитором). Гетерогенный (когда реагирующие
- 43. Ферментативный катализ -каталитические реакции, протекающие с участием ферментов (пищеварение, брожение спиртов, биологическое окисление). Ферменты – биологические
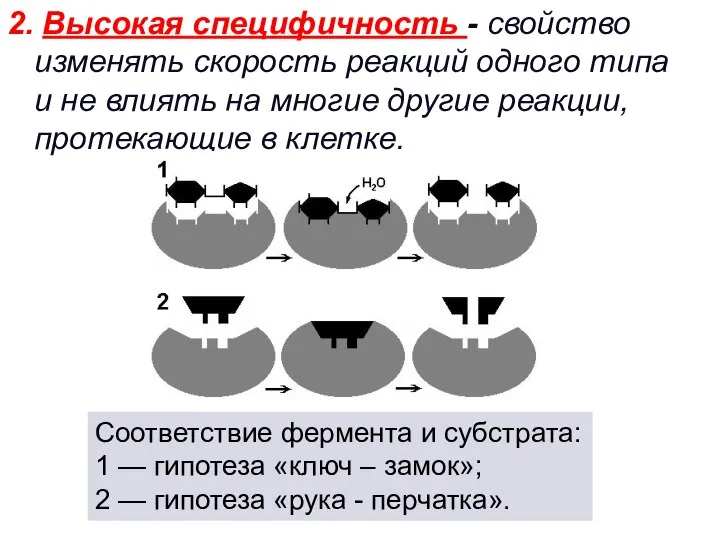
- 44. 2. Высокая специфичность - свойство изменять скорость реакций одного типа и не влиять на многие другие
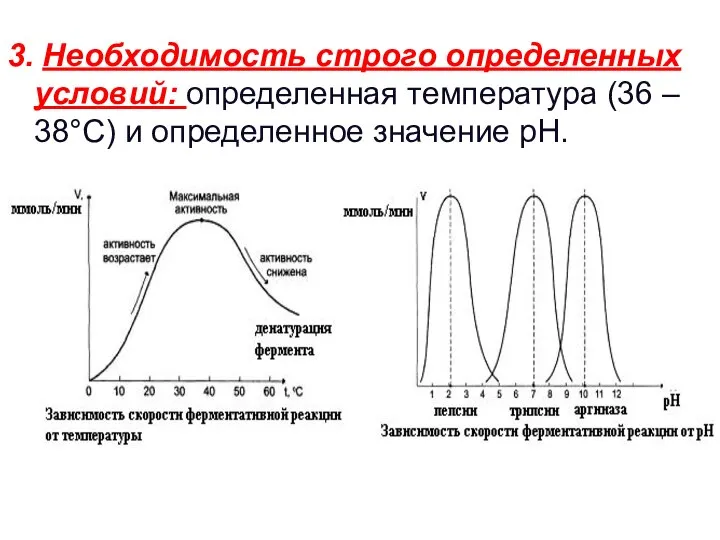
- 45. 3. Необходимость строго определенных условий: определенная температура (36 – 38°С) и определенное значение рН.
- 46. Кинетика ферментативного катализа
- 48. Скачать презентацию




































 Термодинамическое равновесие
Термодинамическое равновесие Оксид металлов
Оксид металлов Легированные конструкционные стали. Инструментальные легированные стали
Легированные конструкционные стали. Инструментальные легированные стали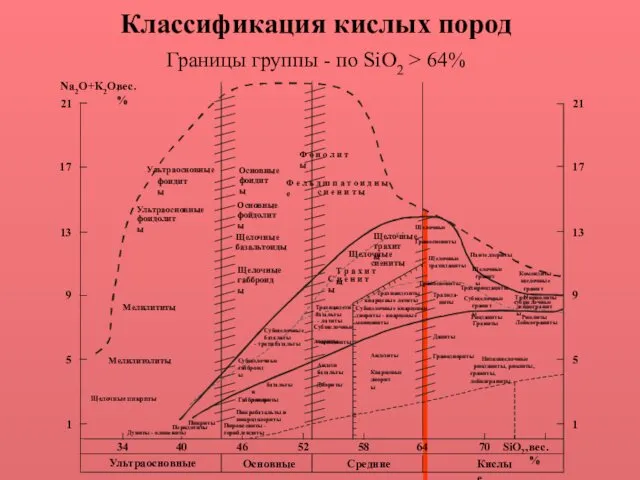 Классификация кислых пород
Классификация кислых пород Хімія та побут
Хімія та побут Биогенные элементы. Классификация. Топография биогенных элементов в организме человека
Биогенные элементы. Классификация. Топография биогенных элементов в организме человека Методы разделения и очистки биомолекул. Ультрацентрифугирование (седиментация)
Методы разделения и очистки биомолекул. Ультрацентрифугирование (седиментация) Презентация по Химии "Способы получения металлов" - скачать смотреть
Презентация по Химии "Способы получения металлов" - скачать смотреть  Аміак
Аміак  Анионно-координационная полимеризация
Анионно-координационная полимеризация Металл серебро
Металл серебро Растворы неэлектролитов и электролитов
Растворы неэлектролитов и электролитов Organic molecules
Organic molecules Атоми і хімічні елементи. Молекули, їх рух. Дифузія
Атоми і хімічні елементи. Молекули, їх рух. Дифузія Технология производства простых полиэфиров
Технология производства простых полиэфиров Литье под давлением реактопластов
Литье под давлением реактопластов Химия функциональных материалов. Адсорбционные материалы. Цеолиты
Химия функциональных материалов. Адсорбционные материалы. Цеолиты Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно
Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно Физиологические эффекты активных форм кислорода
Физиологические эффекты активных форм кислорода Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра
Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Электродные потенциалы. Гальванические элементы. ЭДС
Электродные потенциалы. Гальванические элементы. ЭДС Межмолекулярные силы (силы Ван дер Ваальса)
Межмолекулярные силы (силы Ван дер Ваальса) Углеводы. Глюкоза. ЗНАНИЯ, НЕПРОВЕРЕННЫЕ ОПЫТОМ, МАТЕРЬЮ ВСЯКОЙ ДОСТОВЕРНОСТИ, БЕСПЛОДНЫ И ПОЛНЫ ОШИБОК ЛЕОНАРДО ДА ВИНЧИ
Углеводы. Глюкоза. ЗНАНИЯ, НЕПРОВЕРЕННЫЕ ОПЫТОМ, МАТЕРЬЮ ВСЯКОЙ ДОСТОВЕРНОСТИ, БЕСПЛОДНЫ И ПОЛНЫ ОШИБОК ЛЕОНАРДО ДА ВИНЧИ  Метаморфизм
Метаморфизм Катаболизм фенилаланина, тирозина
Катаболизм фенилаланина, тирозина Живая и мертвая вода
Живая и мертвая вода Главная подгруппа V группы..Азот
Главная подгруппа V группы..Азот