Содержание
- 2. О б р а б о т к а с р е д ы Основные способы
- 3. 3) удаление солей обработкой ионообменными смолами или перегонкой; 4) фильтрация или абсорбция агрессивных компонентов и твердых
- 4. И н г и б и т о р ы к о р р о з
- 5. При равномерной коррозии эффективность ингибиторов оценивается коэффициентом торможения коррозии К (1) или степенью защиты Z (2).
- 6. В к и с л ы х с р е д а х чаще используются органические
- 7. Формальной теории действия ингибиторов: а) кинетического, т.е. изменения константы скорости за счет адсорбции на наиболее активных
- 8. Электродные реакции при кислотной коррозии протекают обычно с кинетическим контролем, тормозящие действие ПАВ проявляется через измерение
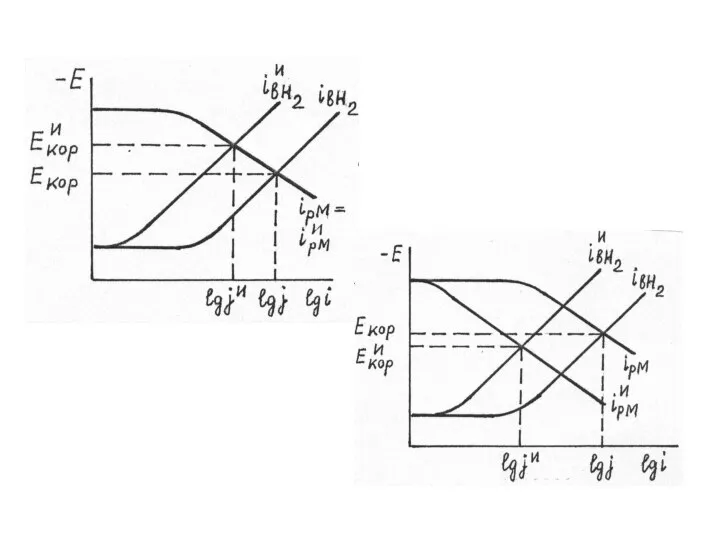
- 10. У анодных и катодных ингибиторов изменение Екор однозначно характеризует защитное действие. Выражение для коэффициента торможения катодного
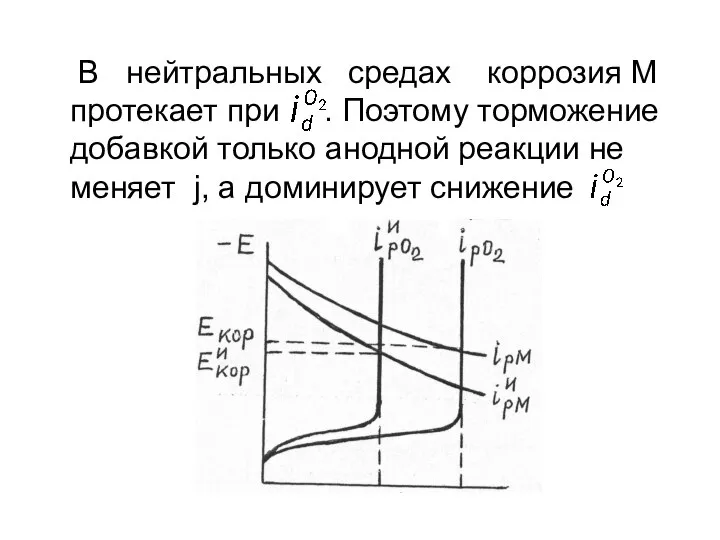
- 11. В нейтральных средах коррозия М протекает при . Поэтому торможение добавкой только анодной реакции не меняет
- 12. К такому эффекту приводит использование пленкообразователей, которые меняют и толщину диффузионного слоя. Поэтому, классификация ингибиторов, использованная
- 13. Катодными ингибиторами будем называть соединения, образующие нерастворимую пленку с продуктами катодной реакций ОН- -ионами (соли цинка,
- 14. Все эффективные ингибиторы имеют полярную ( гидрофильную, адсорбционноактивную ) и неполярную гидрофобную части. У истинно или
- 15. Коллоидно растворимые ПАВ имеют сильно развитые полярные группы и достаточно длинный углеводородный радикал. При достижении в
- 16. Это приводит к превращению вогнутого мениска 1 в выпуклый 2 и исчезновению пленки электролита. Существенным является
- 17. Маслорастворимые ингибиторы как гидрофобизаторы поверхности используются также для защиты от атмосферной коррозии. Они увеличивают краевой угол
- 18. В о д о м а с л о р а с т в о р
- 19. Летучие ингибиторы, которые вводятся одновременно с М в замкнутое пространство, стенки которого обладают низкой паро- и
- 20. Сочетание ингибиторов с электрохимической защитой является к о м б и н и р о в
- 21. Факторы, влияющие на эффективность ингибиторов 1. Химическая структура ПАВ: природа функциональных групп, гетероатомов и заместителей; заряд
- 22. 2. Природа металла: электронная структура, определяющая способность к хемосорбции, пассивации и характер контроля некоторых катодных реакций;
- 23. 3. Природа растворителя: его протолитические свойства, диэлектрическую проницаемость, способность к сольватации и к адсорбции, возможное изменение
- 24. 4. рН: при переходе от кислых к нейтральным растворам меняются принципы подбора ингибиторов, а щелочные растворы
- 25. Они также уменьшают отталкивание катионов друг от друга не зависимо от заряда поверхности. Аналогичную функцию выполняют
- 26. 6. Температура. С ростом температуры защитное действие обычно снижается. Наибольший интерес представляют высокотемпературные ингибиторы, у которых
- 27. 7. Природа кислоты действует через анионные эффекты и природу стадии катодной деполяризации. 8. Перемешивание кислоты за
- 28. 9. Время - за счет изменения состава и состояния поверхности металла и особенно сплава, а также
- 30. Скачать презентацию

























 Химия и косметика Подготовила: Аникина Алина 10 «А»
Химия и косметика Подготовила: Аникина Алина 10 «А»  Обобщение и систематизация знаний по теме Химическая связь и строение атома
Обобщение и систематизация знаний по теме Химическая связь и строение атома Ионообменная хроматография
Ионообменная хроматография Нуклеиновые кислоты Презентация по химии
Нуклеиновые кислоты Презентация по химии Использование химии в медицине
Использование химии в медицине Наиболее активные металлы: элементы I и II групп ПС
Наиболее активные металлы: элементы I и II групп ПС Хлористый водород
Хлористый водород Буферные системы в организме
Буферные системы в организме Основные положения технологии натрия как теплоносителя реакторов на быстрых нейтронах. Требования к качеству реакторного натрия
Основные положения технологии натрия как теплоносителя реакторов на быстрых нейтронах. Требования к качеству реакторного натрия Сульфат меди
Сульфат меди Химическое равновесие
Химическое равновесие Безазотистые вторичные метаболиты минорных групп в фармации. Биохимия, функциональное значение в царстве растений
Безазотистые вторичные метаболиты минорных групп в фармации. Биохимия, функциональное значение в царстве растений Биохимияға кіріспе. Белоктардың қызметтері. Белоктардың жіктелуі. Күрделі белоктар: хромопротеиндер, гликопротеиндер
Биохимияға кіріспе. Белоктардың қызметтері. Белоктардың жіктелуі. Күрделі белоктар: хромопротеиндер, гликопротеиндер Аминокислоты. Классификация
Аминокислоты. Классификация Массовая доля
Массовая доля Теоретические основы биоорганической химии
Теоретические основы биоорганической химии Спирты одноатомные предельные
Спирты одноатомные предельные Углеводы
Углеводы  ГБОУ СОШ № 661 Санкт-Петербург учитель химии Ефремова С.А.
ГБОУ СОШ № 661 Санкт-Петербург учитель химии Ефремова С.А.  Бетоны и железобетон (лекция 3)
Бетоны и железобетон (лекция 3) Состав, свойства и перегонка нефти. Нефтепродукты
Состав, свойства и перегонка нефти. Нефтепродукты Ситуационная задача по биохимии
Ситуационная задача по биохимии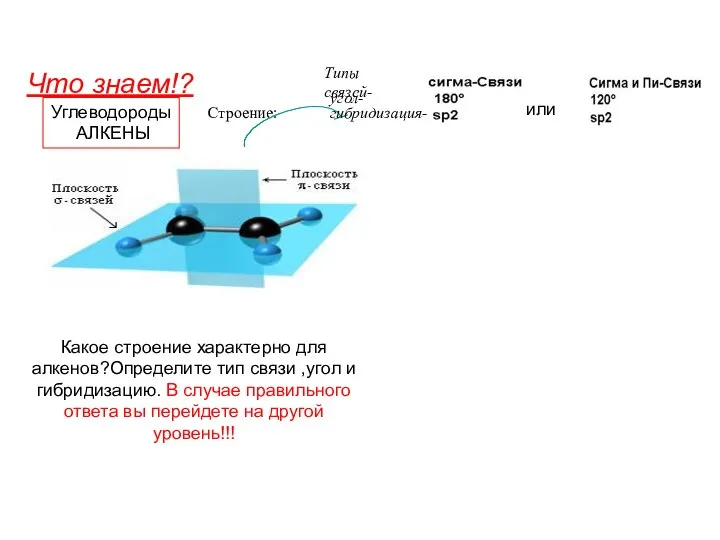 Углеводороды. Алкены
Углеводороды. Алкены L’introduction a la biochimie. La structure et les proprietes des proteines
L’introduction a la biochimie. La structure et les proprietes des proteines Непредельные углеводороды АЛКЕНЫ Алферова Мария Владимировна учитель химии ГБОУ лицей №486 Выборгского района г. Санкт-Петербу
Непредельные углеводороды АЛКЕНЫ Алферова Мария Владимировна учитель химии ГБОУ лицей №486 Выборгского района г. Санкт-Петербу Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар
Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар Окисно-відновні реакції, їхнє значення. Складання найпростіших окисно-відновних реакцій, добір коефіцієнтів
Окисно-відновні реакції, їхнє значення. Складання найпростіших окисно-відновних реакцій, добір коефіцієнтів Кристалічні та аморфні тіла. Рідкі кристали та їх властивості
Кристалічні та аморфні тіла. Рідкі кристали та їх властивості