Содержание
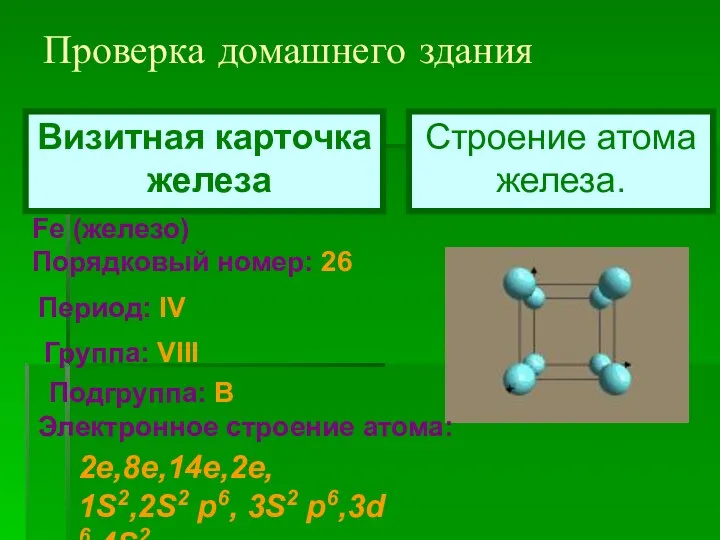
- 2. Проверка домашнего здания Fe (железо) Порядковый номер: 26 Период: IV Группа: VIII Подгруппа: В Электронное строение
- 3. Железо – восстановитель. Атомы Fe отдают электроны не только с последнего уровня, приобретая С.О.+2, но способны
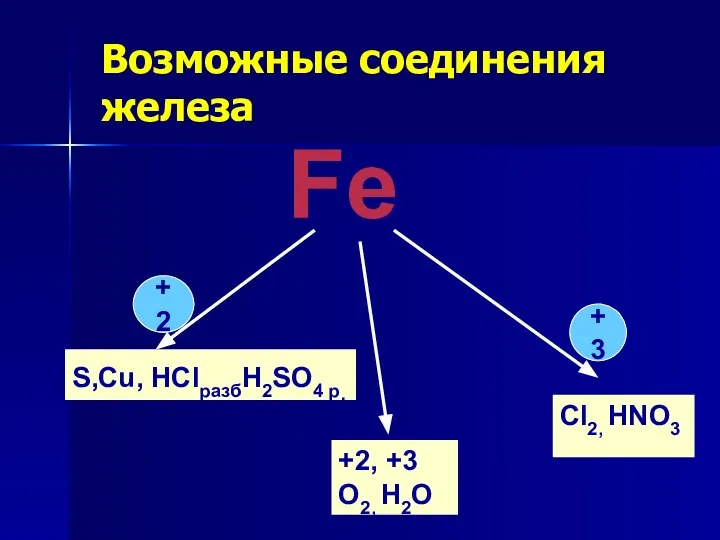
- 4. Возможные соединения железа Fe S,Cu, HClразбH2SO4 р. Cl2, HNO3 +2, +3 O2, H2O +2 +3
- 5. Проверь уравнения реакций Fe + 2HCl = FeCl2 + H2 Р.И.О. Fe + 2H+ + 2Cl
- 6. Муниципальное образовательное учреждение Быстрогорская общеобразовательная средняя школа Тацинского района Ростовской области БЕНЕФИС ЖЕЛЕЗА И ЕГО СОЕДИНЕНИЙ
- 7. Эпиграф Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа
- 8. Действие I Теоретическое
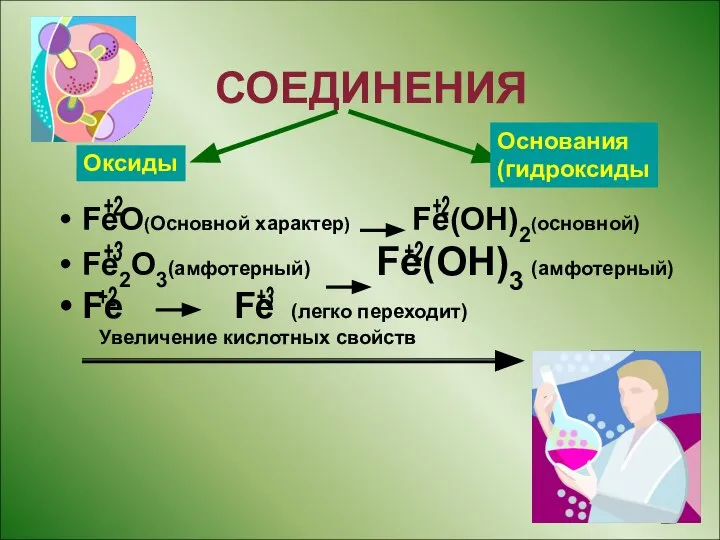
- 9. Оксиды СОЕДИНЕНИЯ FeO(Основной характер) Fe(OH)2(основной) Fe2O3(амфотерный) Fe(OH)3 (амфотерный) Fe Fe (легко переходит) Увеличение кислотных свойств Оксиды
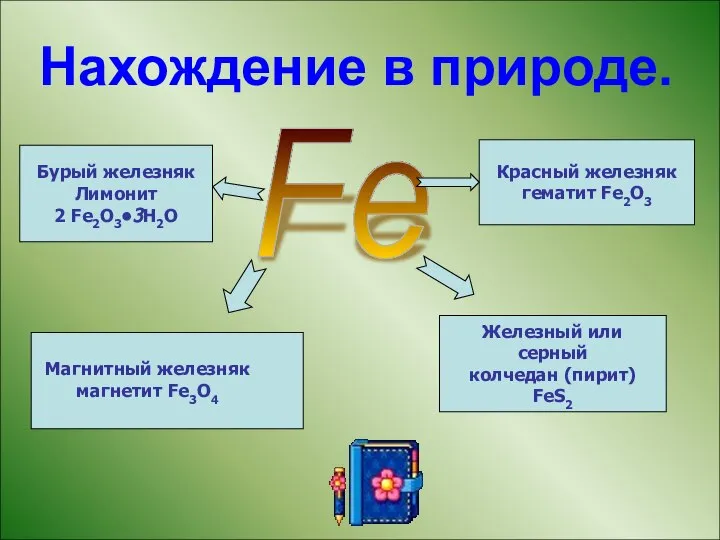
- 10. Нахождение в природе. Fe Магнитный железняк магнетит Fe3O4 Красный железняк гематит Fe2O3 Бурый железняк Лимонит 2
- 11. Действие II Химическое
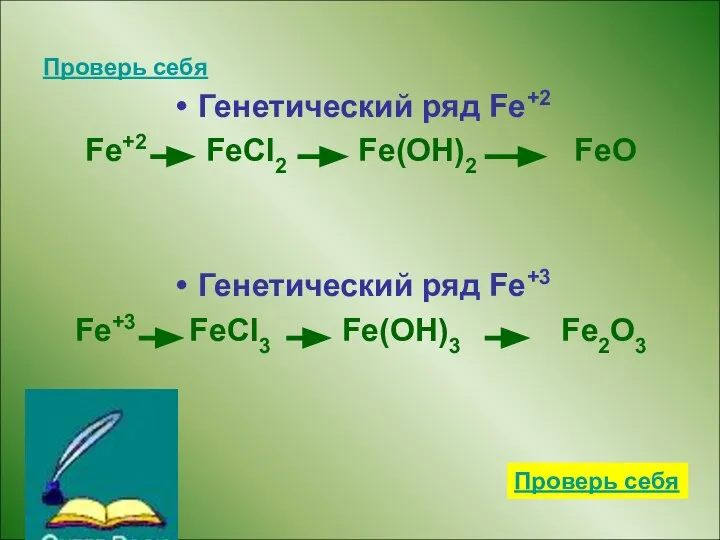
- 12. Проверь себя Генетический ряд Fe+2 Fe+2 FeCl2 Fe(OH)2 FeO Генетический ряд Fe+3 Fe+3 FeCl3 Fe(OH)3 Fe2O3
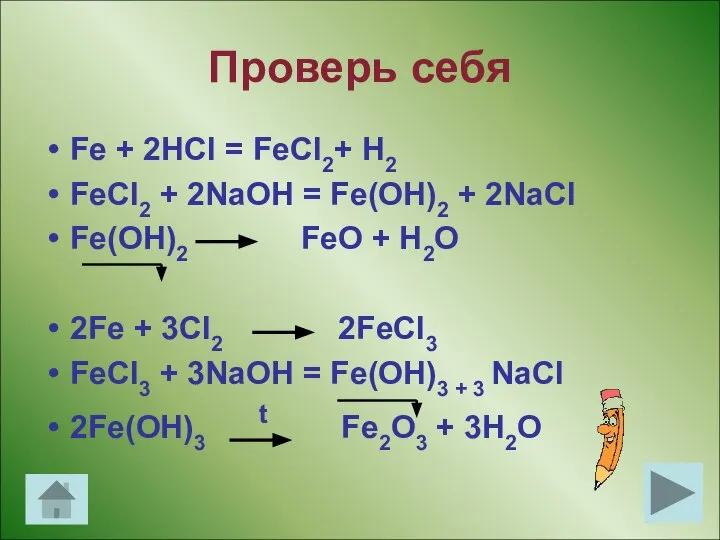
- 13. Проверь себя Fe + 2HCl = FeCl2+ H2 FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl Fe(OH)2
- 14. Действие III Биологическое Презентация 1
- 15. Тест: «Порядок ли у вас с железом». 1 Часто ли вы чувствуете усталость или подавленность? 2.
- 16. Враги Fe Компонент чая связывают Fe в труднорастворимую форму. Чашка чая, выпитая во время еды, сократит
- 17. Врагами являются молочные продукты и яичные желтки.
- 18. Действие IV Практическое
- 19. Реактивом на ионы Fe+2 являются ионы OH- Fe 2+ 2OH- = Fe (OH)2 Реактивом на ионы
- 20. Действие V Гидрологическое Презентация 2
- 21. Калометрическая шкала
- 22. Действие VI Заключительное
- 23. Допишите предложения, посвященные сегодняшнему уроку: Сегодня я узнал (а)_________________________ Я удивился (лась)_________________________ Теперь я умею ____________________________
- 25. Скачать презентацию
















 Ртуть
Ртуть Презентация по Химии "Уравнения окислительно- восстановительных реакций" - скачать смотреть
Презентация по Химии "Уравнения окислительно- восстановительных реакций" - скачать смотреть  Презентация по Химии "Основні Фракції нафти" - скачать смотреть бесплатно
Презентация по Химии "Основні Фракції нафти" - скачать смотреть бесплатно Алюминийорганические соединения
Алюминийорганические соединения Конструкция ферментатора
Конструкция ферментатора Производные пиррозилидина. (Лекция 6)
Производные пиррозилидина. (Лекция 6) Алкалоиды. Классификация алкалоидов:
Алкалоиды. Классификация алкалоидов: Презентация по Химии "Кристаллические решетки" - скачать смотреть _
Презентация по Химии "Кристаллические решетки" - скачать смотреть _ SNAP i.d. Workflow Value Proposition
SNAP i.d. Workflow Value Proposition Химические свойства и применение алканов 10 класс Презентацию подготовила учитель химии МОУ «СОШ с. Тёпловка Новобурасского ра
Химические свойства и применение алканов 10 класс Презентацию подготовила учитель химии МОУ «СОШ с. Тёпловка Новобурасского ра Оценка солености воды реки Цны и питьевой бутилированной воды
Оценка солености воды реки Цны и питьевой бутилированной воды Модельные представления силикатных структур
Модельные представления силикатных структур Исследование растворимости в системе уксусная кислота-этиловый спирт-этилацетат-вода методом изотермического титрования при 60˚C
Исследование растворимости в системе уксусная кислота-этиловый спирт-этилацетат-вода методом изотермического титрования при 60˚C Тема: Витамин Е Выполнила: студентка Шагиева А.А. ГОУ СПО ТОМУ № 1 г. Узловая 2012
Тема: Витамин Е Выполнила: студентка Шагиева А.А. ГОУ СПО ТОМУ № 1 г. Узловая 2012 Соли серной кислоты
Соли серной кислоты Реологические свойства полимерных материалов
Реологические свойства полимерных материалов Липиды и обмен липидов
Липиды и обмен липидов Эмульсии и эмульгаторы
Эмульсии и эмульгаторы Обмен углеводов
Обмен углеводов Этимология названий химических элементов периодической системы Д.И. Менделеева
Этимология названий химических элементов периодической системы Д.И. Менделеева Строение атома. Строение электронных оболочек атомов
Строение атома. Строение электронных оболочек атомов Жиры в питании спортсмена
Жиры в питании спортсмена Регуляция обменных процессов. Гормоны
Регуляция обменных процессов. Гормоны Метаболизм нуклеотидов
Метаболизм нуклеотидов Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве
Смолы и бальзамы. Воски и структурообразующие вещества в косметическом производстве Углеводы. Моносахариды и их производные. (Лекция 5)
Углеводы. Моносахариды и их производные. (Лекция 5) Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Электродитическая диссоциация
Электродитическая диссоциация