Содержание
- 3. GCP и локальные требования Локальные требования «перевешивают» требования GCP там где они противоречат друг другу Локальные
- 4. ICH GCP International Conference on Harmonization (ICH)
- 5. Good Clinical Practice Неспецифический термин Данные правила или руководства описывают обязанности сторон, вовлеченных в подготовку и
- 6. Зачем нужны правила GCP? International Conference on Harmonisation (ICH) GCP Guideline (E6), p. 1 GCP –
- 7. GCP Защита субъектов исследования Качество данных О чем правила GCP?
- 8. Совместная инициатива представителей фарминдустрии и регуляторных органов как равных партнеров для научных и технических дискуссий о
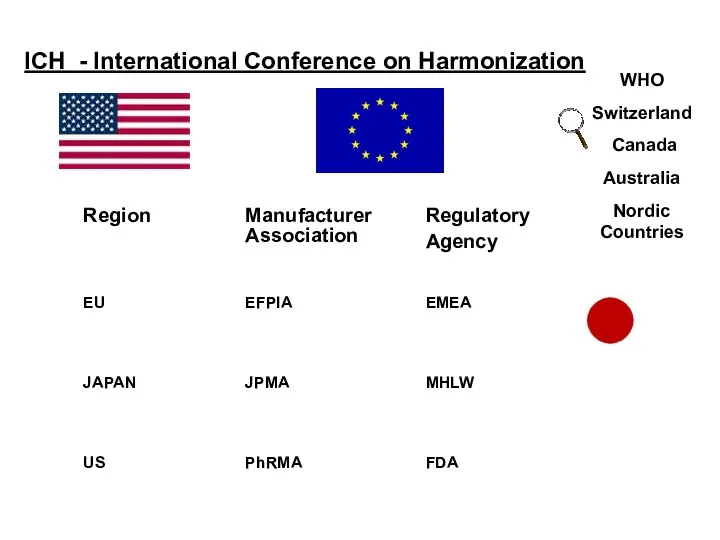
- 9. ICH - International Conference on Harmonization WHO Switzerland Canada Australia Nordic Countries
- 10. Уполномочен создать Единый стандарт для ускорения взаимного признания данных клинических исследований ICH
- 11. GCP Содержание Оглавление Терминология Принципы ICH GCP Комитеты по этике Исследователь Спонсор Протокол & Поправки Брошюра
- 12. 2. Принципы GCP Секции 2.1 – 2.13 2.1 Клинические исследования Принципы ICH GCP взяты из Нюрнбергского
- 13. Хельсинкская декларация Преступления нацистов во время 2 мировой войны “Медицинские эксперименты” http://www.ushmm.org/research/doctors/index.html 1946 Судебный процесс в
- 14. 2. Принципы ICH GCP (2): 2.2 Риск/польза и их оценка 2.3 Права субъектов исследования превалируют над
- 15. 2. Принципы ICH GСP (3) 2.8 Все привлекаемые к проведению исследования лица должны иметь соответствующие образование,
- 16. 2. Принципы ICH GСP (4) 2.9 Информированное согласие 2.10 Правила по документированию медицинских данных 2.11 Конфиденциальность
- 17. SOP Стандартные операционные процедуры Подробные письменные инструкции, предназначенные для достижения единообразия при осуществлении определенной деятельности. ICH
- 18. Стандартные операционные процедуры... …описывают процессы инициации, проведения и документирования
- 19. Регуляторные требования... …лежат в основе стандартных операционных процедур компании спонсора. Для американских компаний это US Code
- 20. IRB/IEC ЭСО/НЭК 1.31 Экспертный совет организации; ЭСО (Institutional Review Board; IRB): Независимый орган, состоящий из лиц,
- 21. ЭСО/НЭК (2) 1.27 Independent Ethics Committee (IEC) Независимый этический комитет; НЭК (Independent Ethics Committee; IEC): Независимый
- 22. 3. ЭСО/НЭК (3) 3.1 Обязанности Защита субъектов исследования Вопросы оплаты 3.2 Состав, функции, деятельность Минимум один
- 23. 3. ЭСО/НЭК Сценарий Вы монитор исследования, и за неделю до его начала Вы узнаете от исследователя
- 24. 3. ЭСО/НЭК Сценарий (2) Протокол рассмотрен и одобрен, но комитет по этике имеет мало данных о
- 25. 3. ЭСО/НЭК Сценарий (3) В комитете по этике 4 члена, и все они работают в той
- 26. 3. ЭСО/НЭК Сценарий (4) Комитет по этике имеет только одну стандартную процедуру, которая регламентирует как часто
- 27. 3. ЭСО/НЭК Сценарий (5) По запросу исследователя в комитете по этике не смогли найти документы по
- 28. 4. Исследователь 4.1 Квалификация и обязательства исследователя Образование, подготовка, опыт Знание протокола, брошюры исследователя, другой информации
- 29. 4. Исследователь (2) 4.3 Оказание медицинской помощи субъектам исследования Медицинские решения принимает врач Необходимая медицинская помощь
- 30. 4. Исследователь (3) 4.5 Соблюдение протокола Подписывает договор Не может изменить протокол без одобрения спонсора Документально
- 31. 4. Исследователь (4) 4.7 Рандомизация и раскрытие кода Соблюдает процедуры рандомизации и раскрытия кода Может раскрыть
- 32. 4. Исследователь (5) 4.9 Записи и отчеты 4.9.1 Отвечает за правильность, полноту, разборчивость и своевременность предоставления
- 33. 4. Исследователь (6) 4.10 Отчеты о ходе исследования 4.10.1 Исследователь должен представлять ЭСО/НЭК краткие письменные отчеты
- 34. 4. Исследователь (7) 4.11 Отчетность по безопасности 4. 11.1 Обо всех серьезных нежелательных явлениях (СНЯ) необходимо
- 35. Исследовательское совещание ICH 4.1.3 Исследователь “ Исследователь должен знать и соблюдать GCP и нормативные требования” ICH
- 36. Физическое или юридическое лицо, являющееся инициатором клинического исследования и несущее ответственность за его организацию и/или финансирование.
- 37. 5. Спонсор 5.1 Обеспечение качества и контроль качества 5.2 Контрактная исследовательская организация 5.3 Медицинская квалификация 5.4
- 38. 5. Спонсор (1) 5.12 Информация об исследуемых продуктах 5.13 Производство, упаковка, маркировка и кодирование исследуемых продуктов
- 39. 5. Спонсор (2) 5.1 Обеспечение качества и контроль качества 5.1.1 Спонсор отвечает за внедрение и поддержание
- 40. 5. Спонсор (3) Мониторинг (monitoring): Деятельность, заключающаяся в контроле за ходом клинического исследования, обеспечении его проведения,
- 41. 5. Спонсор (4) 5.2 Контрактная исследовательская организация 5.2.1 Спонсор может полностью или частично передать обязанности и
- 42. 5. Спонсор (5) 5.3 Медицинская квалификация Спонсор должен назначить обладающий соответствующей медицинской квалификацией персонал, который должен
- 43. 5. Спонсор (6) 5.5 Менеджмент исследования, работа с данными и ведение документации 5.5.1 Спонсор обязан привлекать
- 44. 5. Спонсор (7). Пример для дискуссии Вы сотрудник фармацевтической компании, и Вам нужно выбрать одного исследователя
- 45. 5. Спонсор (8) 5.11 Подтверждение рассмотрения ЭСО/НЭК 5.11.1 Спонсор должен получить от ЭСО/НЭК: - Наименование и
- 46. 5. Спонсор (9) 5.13 Производство, упаковка, маркировка и кодирование исследуемых продуктов 5,13.1 Маркировка по требованиям GMP
- 47. 5. Спонсор (10) 5.14 Поставка исследуемых продуктов и правила обращения с ними 5.14.1 Спонсор отвечает за
- 48. 5. Спонсор (11) 5.15 Доступ к записям 5.15.1 Спонсор обеспечивает прямой доступ к первичным данным/документации 5.15.2
- 49. 5. Спонсор (12) 5.18 Мониторинг 5.18.1 Цель удостовериться, что: A. Права пациента защищены B. Данные точные,
- 50. 5. Спонсор (13) 5.18 Мониторинг 5.18.4 Обязанности монитора - Связующее звено между спонсором и исследователем -
- 51. Мониторинг (визиты в центры) (1) Предварительный визит Pre-Study Visit (2) Инициирующий визит Initiation Visit (3) Регулярный
- 52. Мониторинг. Пример для дискуссии Вы монитор и приехали с регулярным визитом в центр. Проверяя подписанные формы
- 53. Мониторинг. Пример для дискуссии “ До начала участия в исследовании субъект или его законный представитель, а
- 54. 5. Спонсор (14) 5.19 Аудит 5.19.1 Проводится независимо от мониторинговых визитов Цель - оценка соответствия проводимого
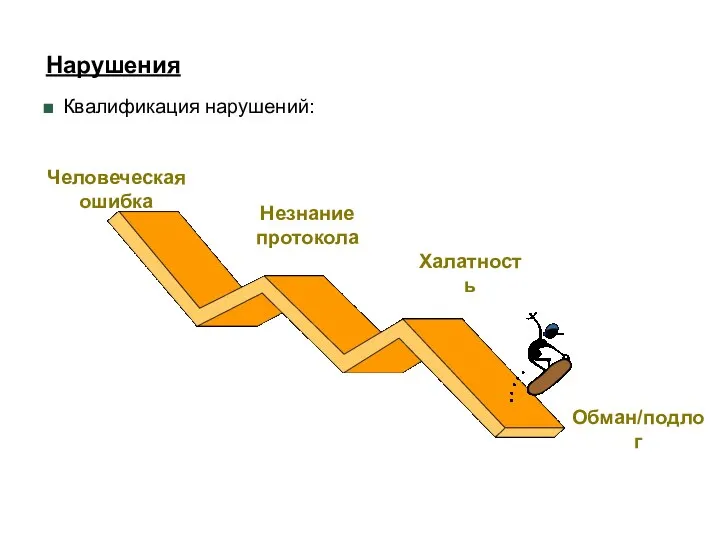
- 55. Нарушения Квалификация нарушений:
- 56. Последствия… Если не соблюдать GCP Риски для пациентов Недостоверные данные Непризнание исследования Задержки в старте продаж
- 58. Скачать презентацию




















































 Обращение с медицинскими отходами
Обращение с медицинскими отходами Лекция колики 1
Лекция колики 1 Pathogens of atypical pneumonia
Pathogens of atypical pneumonia Первая помощь при попадании инородного тела в дыхательные пути
Первая помощь при попадании инородного тела в дыхательные пути Засоби, що впливають на серцево-судинну систему у форматі підготовки до ЛІІ Крок-1. ЗЛП
Засоби, що впливають на серцево-судинну систему у форматі підготовки до ЛІІ Крок-1. ЗЛП Особенности опухолевых клеток
Особенности опухолевых клеток Дифференциальная диагностика рассеянного склероза
Дифференциальная диагностика рассеянного склероза ДНК-ның фотохимиялық түрленуі. Люминесценттік таңбалар мен сорғылар және олардың биология мен медицинада
ДНК-ның фотохимиялық түрленуі. Люминесценттік таңбалар мен сорғылар және олардың биология мен медицинада Карпо-карпальный синдром (тонельный синдром)
Карпо-карпальный синдром (тонельный синдром) Определение числа эритроцитов пробирочным методом в камере Горяева. Лабораторная работа № 4
Определение числа эритроцитов пробирочным методом в камере Горяева. Лабораторная работа № 4 Тетрада Фалло
Тетрада Фалло Белок и его роль в правильном питании и снижении веса
Белок и его роль в правильном питании и снижении веса Иммунитет - невосприимчивость, сопротивляемость организма к инфекциям и инвазиям чужеродных организмов
Иммунитет - невосприимчивость, сопротивляемость организма к инфекциям и инвазиям чужеродных организмов Патофизиология артериальных гипертензий
Патофизиология артериальных гипертензий Пневмонии у детей
Пневмонии у детей Физиологические механизмы изменения проницаемости эндотелия кровеносных сосудов
Физиологические механизмы изменения проницаемости эндотелия кровеносных сосудов Страбизм. Методы диагностики
Страбизм. Методы диагностики Электролечение – постоянные и импульсные токи
Электролечение – постоянные и импульсные токи Элементы возрастной психологии и их учет в деятельности врача
Элементы возрастной психологии и их учет в деятельности врача Пороки развития уха
Пороки развития уха Биогеохимиялық эндемиялар, олардың алдын алу
Биогеохимиялық эндемиялар, олардың алдын алу Опорно-двигательная система. Строение скелета
Опорно-двигательная система. Строение скелета Ауруханадан тыс пневмониямен ауыратын науқастарды емдеу кезіндегі пенициллин мен
Ауруханадан тыс пневмониямен ауыратын науқастарды емдеу кезіндегі пенициллин мен Методы изучения человека
Методы изучения человека Жүйелі қызыл жегі
Жүйелі қызыл жегі Проблемы современной психологии. Профориентация старшеклассников
Проблемы современной психологии. Профориентация старшеклассников Рак и беременость
Рак и беременость Особенности заполнения специализированной отчетной формы №7 (онкология сводная)
Особенности заполнения специализированной отчетной формы №7 (онкология сводная)