Содержание
- 2. Введение. Клеточный иммунитет (англ. Cell-mediated immunity) — такой тип иммунного ответа, в котором не участвуют ни
- 3. Клеточный иммунный ответ. Типы эффекторных Т-клеток и их функции. Взаимодействие адаптивных Т-клеток с эффекторами или мишенями,
- 4. Цитотоксический Т-клеточный иммунный ответ.
- 5. Цитотоксический Т-клеточный иммунный ответ. Цитотоксический иммунный ответ осуществляют Т-лимфоциты, экспрессирующие корецептор CD8. Это определяет главную особенность
- 6. Естественные и индуцированные цитотоксические Т-лимфоциты.
- 7. Цитотоксический иммунный ответ проходит в 4этапа. I. Презентация II. Пролиферация III. Дифференцировка IV. Цитолиз антигена клеток
- 8. Распознавание антигенного пептида и активация CD8 Т-клеток. Вирусом может быть инфицирована практически любая клетка организма. Однако
- 9. Распознавание антигенного пептида и активация CD8 Т-клеток. Особенности распознавания антигена при индукции развития цитотоксических Т-лимфоцитов и
- 10. Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток. Долгое время участие CD4+ Т-хелперов в развитии цитотоксического
- 11. Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток. Именно степень самообеспечения активированных CD8+ Т-клеток аутокринным ростовым
- 12. Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток. Таким образом, хотя CD8+ Т-клетки, вовлекаемые в цитотоксический
- 13. Цитотоксические Т-лимфоциты. Как и в случае Т-хелперов, дифференцировка цитотоксических Т-лимфоцитов начинается в процессе их пролиферативной экспансии.
- 14. Цитотоксические Т-лимфоциты. В процессе дифференцировки в эффекторные клетки происходит сплайсинг участков РНК, кодируемых экзонами сначала А,
- 15. Иммунный Т-клеточный цитолиз. Механизмы реализации цитотоксического эффекта через индукцию апоптоза. Цитолиз клеток-мишеней цитотоксическими Т-лимфоцитами осуществляется с
- 16. Иммунный Т-клеточный цитолиз. Как и при цитолизе, осуществляемом естественными киллерами, между цитотоксическим Т-лимфоцитом и клеткой-мишенью формируется
- 17. Иммунный Т-клеточный цитолиз. Перфорин, поступающий в микрополость, в присутствии ионов Ca2+ изменяет свою конформацию: на поверхности
- 18. Fas-зависимый цитолиз. Цитотоксические Т-лимфоциты используют еще один механизм контактного киллинга, причем в большей степени, чем естественные
- 19. Миграция клеток при цитотоксическом иммунном ответе. Цитотоксический клеточный иммунный ответ участвует преимущественно в защите от вирусных
- 20. Миграция клеток при цитотоксическом иммунном ответе. В очагах инфицирования вирусами и другими патогенами цитотоксические Т-лимфоциты реализуют
- 21. Миграция клеток при цитотоксическом иммунном ответе. После успешного завершения цитотоксического иммунного ответа происходит быстрая и радикальная
- 22. Воспалительный Т-клеточный иммунный ответ.
- 23. Воспалительный Т-клеточный иммунный ответ. Эта форма иммунного ответа предназначена для защиты от внутриклеточных патогенов, локализующихся в
- 24. Воспалительный Т-клеточный иммунный ответ. Схема развития клеточного иммунного ответа воспалительного типа. Клеточный иммунный ответ воспалительного типа
- 25. Воспалительный Т-клеточный иммунный ответ. За реализацию этой формы защиты отвечают Thl-клетки и макрофаги. Thl-клетки формируются на
- 26. Активирующее взаимодействие Thl-клеток с макрофагами. Этот этап характерен именно для воспалительного иммунного ответа. Он состоит во
- 27. Активирующее взаимодействие Thl-клеток с макрофагами. Активация макрофагов Т-хелперами. Показаны механизмы воздействия Thl-клеток на макрофаги (контактный и
- 28. Активирующее взаимодействие Thl-клеток с макрофагами. Роль интерферона у в дифференцировке и реализации функций Т-хелперов. Интерферон, продуцируемый
- 29. Воспалительная составляющая Thl-клеточного иммунного ответа. В отличие от цитотоксического иммунного ответа, не связанного очевидным образом с
- 30. Иммунное воспаление. Вариант воспаления, реализуемый с участием Th1-клеток, называют иммунным воспалением, а сам Th1-клеточный иммунный ответ
- 32. Скачать презентацию
Введение.
Клеточный иммунитет (англ. Cell-mediated immunity) — такой тип иммунного ответа, в
Введение.
Клеточный иммунитет (англ. Cell-mediated immunity) — такой тип иммунного ответа, в
Система клеточного иммунитета выполняет защитные функции следующими способами:
путём активации антиген-специфических цитотоксичных Т-лимфоцитов, которые могут вызывать апоптоз соматических клеток, демонстрируя на поверхности эпитопы чужеродных антигенов, например, клеток, заражённых вирусами, содержащими бактерии и клеток опухолей, демонстрирующих опухолевые антигены;
путём активации макрофагов и натуральных киллеров, которые разрушают внутриклеточные патогены;
путём стимулирования секреции цитокинов, которые оказывают влияние на другие клетки иммунной системы, принимающие участие в адаптивном иммунном ответе и врождённом иммунном ответе.
Клеточный иммунитет направлен преимущественно против микроорганизмов, которые выживают в фагоцитах и против микроорганизмов, поражающие другие клетки. Система клеточного иммунитета особенно эффективна против клеток, инфицированных вирусами, и принимает участие в защите от грибов, простейших, внутриклеточных бактерий и против клеток опухолей. Также система клеточного иммунитета играет важную роль в отторжении тканей.
Клеточный иммунный ответ.
Типы эффекторных Т-клеток и их функции. Взаимодействие адаптивных Т-клеток
Клеточный иммунный ответ.
Типы эффекторных Т-клеток и их функции. Взаимодействие адаптивных Т-клеток
Из сказанного выше следует, что клеточный иммунный ответ, осуществляемый Т-лимфоцитами, направлен на защиту от внутриклеточных патогенов. В зависимости от локализации патогенов в цитозоле или в гранулах различают 2 варианта клеточного иммунного ответа — цитотоксический и воспалительный. Характер иммунного ответа в наибольшей степени зависит от доминирующего направления дифференцировки Т-клеток, играющих универсальную роль в развитии иммунного ответа: они выступают в качестве не только хелперов и регуляторов, но и эффекторов, выполняющих собственные защитные функции. На рис. представлены 4 основных типа эффекторных Т-клеток, определяющих развитие иммунного ответа во всех его вариантах.
Цитотоксический Т-клеточный иммунный ответ.
Цитотоксический Т-клеточный иммунный ответ.
Цитотоксический Т-клеточный иммунный ответ.
Цитотоксический иммунный ответ осуществляют Т-лимфоциты, экспрессирующие корецептор CD8.
Цитотоксический Т-клеточный иммунный ответ.
Цитотоксический иммунный ответ осуществляют Т-лимфоциты, экспрессирующие корецептор CD8.
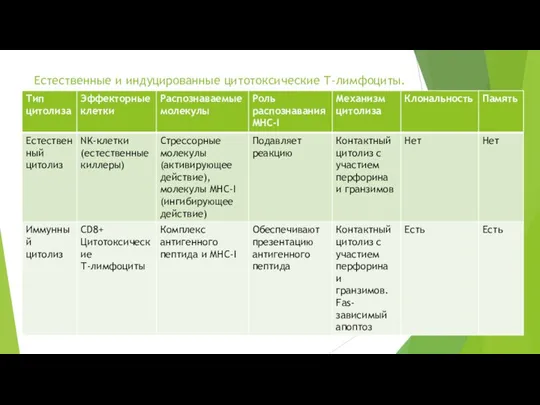
Естественные и индуцированные цитотоксические Т-лимфоциты.
Естественные и индуцированные цитотоксические Т-лимфоциты.
Цитотоксический иммунный ответ проходит в 4этапа.
I. Презентация II. Пролиферация III. Дифференцировка
Цитотоксический иммунный ответ проходит в 4этапа.
I. Презентация II. Пролиферация III. Дифференцировка
Презентация дендритными клетками антигена CD8+ Т-лимфоцитам, приводящая к их активации.
IL-2 -зависимая пролиферация CD8+ Т-клеток, аутокринная или индуцируемая CD4+ Т-лимфоцитами.
Дифференцировка CD8+ Т-клеток в цитотоксические Т-лимфоциты (CTL), сопутствующая пролиферации.
Реализация цитолиза клеток-мишеней.
Распознавание антигенного пептида и активация CD8 Т-клеток.
Вирусом может быть инфицирована практически
Распознавание антигенного пептида и активация CD8 Т-клеток.
Вирусом может быть инфицирована практически
Канонический механизм включения антигенного пептида в молекулу MHC-I может быть реализован только при инфицировании АПК, что действительно может иметь место, но происходит не при любой вирусной инфекции. В типичном случае вирус или его антигены попадают в АПК в результате эндоцитоза (пино- или фагоцитоза) и оказываются в компартменте МПС, что приводит к встраиванию антигенного пептида в молекулы MHC-II. Противоречие разрешается благодаря срабатыванию механизма перекрестной презентации, состоящего в транспортировке антигенного материала из компартмента MIIC в цитозоль или непосредственно в эндоплазматический ретикулум, в котором происходит встраивание фрагментов антигена внеклеточного происхождения в молекулы МНС-I. Это создает возможность распознавания такого пептида CD8+ Т-клетками — будущими цитотоксическими Т-лимфоцитами.
Распознавание антигенного пептида и активация CD8 Т-клеток.
Особенности распознавания антигена при индукции
Распознавание антигенного пептида и активация CD8 Т-клеток.
Особенности распознавания антигена при индукции
Презентация антигенного пептида CD8+ Т-клеткам происходит практически так же, как и презентация пептидов CD4+ Т-клеткам. Отличие заключается в том, что в распознавании комплекса пептид-MHC-I в качестве корецептора участвует молекула CD8. В соответствии с особенностями строения антигенсвязывающей щели пептид, встраиваемый в молекулу MHC-I, имеет более стандартный размер (8-10 остатков), заякорен в двух позициях и не выходит за пределы щели. Расположение варьирующих остатков, формирующих участки, распознаваемые TCR и корецептором CD8+ Т-клетки в молекуле MHC-I отличается от такового в молекуле MHC-II.
Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток.
Долгое время участие CD4+
Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток.
Долгое время участие CD4+
Спектр генов, экспрессируемых при активации CD8+ и CD4+ Т-клетками, сходен, но не идентичен. Помимо включения в случае CD8+ клеток дифференцировочной программы, обеспечивающей реализацию механизмов цитолиза, эта разница касается преимущественно степени экспрессии гена IL2. Активированные CD8+ Т-клетки экспрессируют в большом количестве альфа-цепь рецептора для IL-2, что приводит к формированию его высокоаффинной формы. Однако сам ген IL2 экспрессируется слабее, чем в CD4+ Т-клетках. Выраженность экспрессии гена IL2 зависит от интенсивности стимуляции дендритными клетками в процессе презентации антигена. В результате уровень секреции IL-2 может существенно варьировать и в разной степени обеспечивать потребность в этом цитокине на этапе пролиферативной экспансии клонов Т-лимфоцитов.
Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток.
Именно степень самообеспечения активированных
Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток.
Именно степень самообеспечения активированных
Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток.
Таким образом, хотя CD8+
Роль Т-хелперов и IL-2 в ответе CD8 Т-клеток.
Таким образом, хотя CD8+
Пролиферативная экспансия клонов CD8+ Т-клеток длится 5—7 суток, за которые клетки проходят 6—8 делений. При вирусных инфекциях эти лимфоциты осуществляют 15—20 делений за несколько более длительный период. Интенсивность деления активированных CD8+ Т-клеток выше, чем любых других лимфоцитов, вовлекаемых в иммунный ответ. Пролиферация обеспечивает увеличение численности цитотоксических Т-клеток в 50 000 раз, чего достаточно для реализации их эффекторной функции. При острых вирусных инфекциях у мышей пик численности цитотоксических Т-лимфоцитов достигается уже на 7-е сутки, а к 15-м суткам их количество снижается.
Цитотоксические Т-лимфоциты.
Как и в случае Т-хелперов, дифференцировка цитотоксических Т-лимфоцитов начинается в
Цитотоксические Т-лимфоциты.
Как и в случае Т-хелперов, дифференцировка цитотоксических Т-лимфоцитов начинается в
В процессе дифференцировки цитотоксических Т-лимфоцитов существенно изменяется экспрессия ими мембранных молекул. Для любых эффекторных Т-клеток (а также Т-клеток памяти) характерно изменение структуры мембранной молекулы CD45. Выше эта молекула упоминалась в связи с ее участием в активации Т-клеток. При дифференцировке Т-клеток в эффекторы и клетки памяти происходят изменения во внеклеточных доменах молекулы СD45. Внеклеточную часть этой очень большой молекулы кодируют 7 экзонов. Три из них (как и кодируемые ими домены с содержащимися в них эпитопами) обозначают буквами А, В и С. В наивных Т-клетках транскрибируемая мРНК транслируется в полном объеме и формируется белок, содержащий домены (и, соответственно, антигенные эпитопы) А, В и С.
Цитотоксические Т-лимфоциты.
В процессе дифференцировки в эффекторные клетки происходит сплайсинг участков РНК,
Цитотоксические Т-лимфоциты.
В процессе дифференцировки в эффекторные клетки происходит сплайсинг участков РНК,
Изменения затрагивают также комплекс мембранных молекул, определяющих направление миграции клеток. Молекулы, свойственные наивным Т-клеткам («рецептор хоминга» во вторичные лимфоидные органы CD62L, хемокиновый рецептор CCR7, направляющий клетки в Т-зоны), исчезают и заменяются другими. Эффекторные клетки приобретают ргинтегрины (в частности, VLA-4), а также — р7-интегрины (аЕР7-интегрин направляет миграцию в слизистые оболочки, а а4Р7-интегрин — только в их кишечный отдел). В ходе дифференцировки цитотоксических Т-лимфоцитов усиливается экспрессия ими р2-интегрина LFA-1 — функционально важной молекулы, обеспечивающей контакт с клеткой-мишенью. Этот интегрин впервые обнаружили именно на цитотоксических Т-лимфоцитах и его название — функциональный антиген лимфоцитов (Lymphocyte fuctional antigen) — отражает его роль в реализации киллерной функции Т-клеток. Хемокиновый рецептор CCR7 практически исчезает с поверхности Т-киллеров и заменяется рецепторами CCR4, CCR6 и других цитокинов, обусловливающих миграцию клеток не в лимфоидные органы, а в барьерные ткани и очаги воспаления.
Иммунный Т-клеточный цитолиз.
Механизмы реализации цитотоксического эффекта через индукцию апоптоза.
Цитолиз клеток-мишеней цитотоксическими
Иммунный Т-клеточный цитолиз.
Механизмы реализации цитотоксического эффекта через индукцию апоптоза.
Цитолиз клеток-мишеней цитотоксическими
распознавание клетки-мишени;
формирование конъюгата киллера и клетки-мишени с их поляризацией;
экзоцитоз гранул (программирование лизиса);
индукция гибели клетки-мишени.
Распознавание цитотоксическим Т-лимфоцитом клетки-мишени осуществляется с участием практически тех же молекул, которые формируют иммунный синапс при презентации антигенного пептида АПК. Центральное событие при этом — распознавание комплекса антигенного пептида с молекулой MHC-I, осуществляемое TCR и корецептором CD8. Наиболее существенное отличие состоит в том, что клетки-мишени лишены костимулирующих молекул, и поэтому костимуляция при распознавании клетки-мишени отсутствует (см. рис.).
Иммунный Т-клеточный цитолиз.
Как и при цитолизе, осуществляемом естественными киллерами, между цитотоксическим
Иммунный Т-клеточный цитолиз.
Как и при цитолизе, осуществляемом естественными киллерами, между цитотоксическим
Иммунный Т-клеточный цитолиз.
Перфорин, поступающий в микрополость, в присутствии ионов Ca2+ изменяет
Иммунный Т-клеточный цитолиз.
Перфорин, поступающий в микрополость, в присутствии ионов Ca2+ изменяет
После реализации цитолиза по перфоринзависимому механизму на поверхности цитотоксического Т-лимфоцита остается метка в виде молекулы CD107 (LAMP — Lysosome-associated membrane protein) — белка, содержащегося в мембране цитотоксических гранул (и вообще лизосом). При экзоцитозе CD107 выносится на поверхность клетки и некоторое время присутствует в составе наружной мембраны. Благодаря этой метке удается определить численность цитотоксических Т-лимфоцитов (а также естественных киллеров), выполнивших свою функцию.
Fas-зависимый цитолиз.
Цитотоксические Т-лимфоциты используют еще один механизм контактного киллинга, причем в
Fas-зависимый цитолиз.
Цитотоксические Т-лимфоциты используют еще один механизм контактного киллинга, причем в
Реализация апоптотического механизма цитолиза клетки-мишени при действии цитотоксических Т-лимфоцитов происходит с участием Fas-лиганда, экспрессируемого Т-клеткой, и Fas-рецептора клетки-мишени. Наличие этого рецептора на поверхности клетки-мишени служит условием реализации данного механизма апоптоза. Fas-рецептор, относимый к активационным молекулам, присутствует на поверхности многих клеток человека и млекопитающих. Его экспрессии способствует инфицирование вирусом и опухолевая трансформация. Реже апоптоз клеток-мишеней вызывает TNFa при условии его распознавания рецептором I типа — TNFRI (р55). Этот вариант апоптоза больше характерен для CD4+ Т-клеток, в определенных обстоятельствах способных индуцировать программированную гибель клеток.
Миграция клеток при цитотоксическом иммунном ответе.
Цитотоксический клеточный иммунный ответ участвует преимущественно
Миграция клеток при цитотоксическом иммунном ответе.
Цитотоксический клеточный иммунный ответ участвует преимущественно
Благодаря смене мембранных молекул адгезии и хемокиновых рецепторов, о чем говорилось выше, цитотоксические Т-лимфоциты мигрируют в нелимфоидные ткани, преимущественно барьерные. В эпителии слизистой оболочки кишечника они составляют преобладающий клеточный тип.
Миграция клеток при цитотоксическом иммунном ответе.
В очагах инфицирования вирусами и другими
Миграция клеток при цитотоксическом иммунном ответе.
В очагах инфицирования вирусами и другими
Цитотоксические реакции, осуществляемые естественными киллерами и цитотоксическими Т-лимфоцитами, отличаются друг от друга в основном специфичностью цитолиза (Т-клетки атакуют клетки, презентирующие в составе MHC-I чужеродные пептиды). Таким образом, клетки адаптивного иммунитета используют эффекторную реакцию, сформировавшуюся в рамках врожденного иммунитета, проявляя при этом более высокую избирательность, прицельность действия. Другое приобретение адаптивного иммунитета — формирование иммунологической памяти, благодаря чему при повторном инфицировании тем же вирусом пораженные клетки устраняются быстрее и эффективнее.
Миграция клеток при цитотоксическом иммунном ответе.
После успешного завершения цитотоксического иммунного ответа
Миграция клеток при цитотоксическом иммунном ответе.
После успешного завершения цитотоксического иммунного ответа
Воспалительный Т-клеточный иммунный ответ.
Воспалительный Т-клеточный иммунный ответ.
Воспалительный Т-клеточный иммунный ответ.
Эта форма иммунного ответа предназначена для защиты от
Воспалительный Т-клеточный иммунный ответ.
Эта форма иммунного ответа предназначена для защиты от
Воспалительный Т-клеточный иммунный ответ.
Схема развития клеточного иммунного ответа воспалительного типа.
Клеточный иммунный
Воспалительный Т-клеточный иммунный ответ.
Схема развития клеточного иммунного ответа воспалительного типа.
Клеточный иммунный
Презентация дендритными клетками антигена CD4+ Т-лимфоцитам, приводящая к их активации.
Развитие хелперных Т-лимфоцитов.
Презентация антигена макрофагами ранее сформировавшимся Т-хелперам, их взаимная активация и выделение цитокинов.
Активация цитолиза в фагосомах макрофагов.
Воспалительный Т-клеточный иммунный ответ.
За реализацию этой формы защиты отвечают Thl-клетки и
Воспалительный Т-клеточный иммунный ответ.
За реализацию этой формы защиты отвечают Thl-клетки и
Активирующее взаимодействие Thl-клеток с макрофагами.
Этот этап характерен именно для воспалительного иммунного
Активирующее взаимодействие Thl-клеток с макрофагами.
Этот этап характерен именно для воспалительного иммунного
Стимуляция макрофага при взаимодействии с TW-клеткой реализуется с помощью двух механизмов (рис.). Один из них — контактный — через костимулирующую молекулу CD40, с которой связывается ее лиганд CD154. CD40 спонтанно экспрессируется макрофагами, тогда как ее лиганд появляется на поверхности TM-клеток в результате активации при формировании иммунного синапса. В передаче сигнала от молекулы CD40 участвуют адапторные факторы TRAF-1, TRAF-2, TRAF-6. В результате происходят активация фактора NF-kB и запуск Rac-зависимой ветви MAP-каскада, завершающейся формированием транскрипционного фактора с-Jun. Второй механизм активации опосредуется IFNy. При связывании этого цитокина с рецептором включается сигнальный путь, вовлекающий киназы Jak1 и Jak2, транскрипционный фактор STAT1, а также дополнительные пути с участием MAP-каскада.
Активирующее взаимодействие Thl-клеток с макрофагами.
Активация макрофагов Т-хелперами. Показаны механизмы воздействия Thl-клеток
Активирующее взаимодействие Thl-клеток с макрофагами.
Активация макрофагов Т-хелперами. Показаны механизмы воздействия Thl-клеток
Результат активации макрофагов — экспрессия многочисленных генов, приводящая к повышению содержания на поверхности клетки молекул MHC-I и особенно MHC-II, сборке NADPH-оксидазы, активации ферментов окислительного метаболизма. Наиболее специфичное проявление ответа макрофагов на стимулирующее действие IFNy — экспрессия гена индуцибельной NO-синтазы. Именно NO и его производные, такиекак пероксинитрит (ОО*NO), вызывают гибель микобактерий и других внутриклеточных патогенов, сохранявшихся и даже размножавшихся в фагосомах. Все эффекты IFNy, в том числе способность индуцировать образование NO-синтазы, усиливаются TNFa, продуцируемым как Th1- клетками, так и самими макрофагами. Эффективность действия цитокинов, вырабатываемых TM-клетками, существенно повышается в связи с сосредоточением их секреции в области контакта с макрофагами. Это, кроме того, уменьшает активацию посторонних клеток и их повреждение. Для обеспечения этой ориентированной секреции необходима поляризация клеток в ходе формирования иммунного синапса.
Активирующее взаимодействие Thl-клеток с макрофагами.
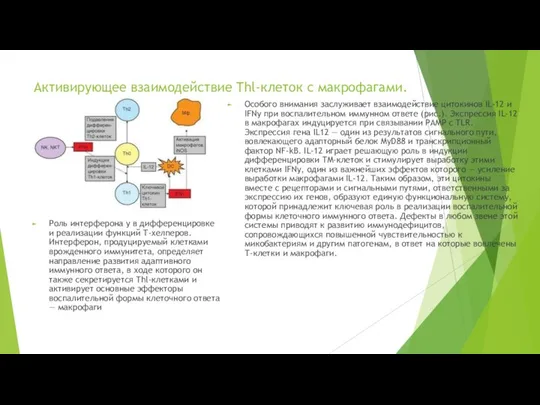
Роль интерферона у в дифференцировке и реализации
Активирующее взаимодействие Thl-клеток с макрофагами.
Роль интерферона у в дифференцировке и реализации
Особого внимания заслуживает взаимодействие цитокинов IL-12 и IFNy при воспалительном иммунном ответе (рис.). Экспрессия IL-12 в макрофагах индуцируется при связывании PAMP с TLR. Экспрессия гена IL12 — один из результатов сигнального пути, вовлекающего адапторный белок MyD88 и транскрипционный фактор NF-kB. IL-12 играет решающую роль в индукции дифференцировки TM-клеток и стимулирует выработку этими клетками IFNy, один из важнейших эффектов которого — усиление выработки макрофагами IL-12. Таким образом, эти цитокины вместе с рецепторами и сигнальными путями, ответственными за экспрессию их генов, образуют единую функциональную систему, которой принадлежит ключевая роль в реализации воспалительной формы клеточного иммунного ответа. Дефекты в любом звене этой системы приводят к развитию иммунодефицитов, сопровождающихся повышенной чувствительностью к микобактериям и другим патогенам, в ответ на которые вовлечены Т-клетки и макрофаги.
Воспалительная составляющая Thl-клеточного иммунного ответа.
В отличие от цитотоксического иммунного ответа, не
Воспалительная составляющая Thl-клеточного иммунного ответа.
В отличие от цитотоксического иммунного ответа, не
Оказавшись в очагах инфицирования, Thl-клетки в кооперации с макрофагами осуществляют реакции, описанные выше. В результате взаимодействия этих клеток, особенно действия IFNy, происходит максимально выраженная активация макрофагов. Эта активация результативна с точки зрения защиты от внутриклеточных патогенов, но деструктивна для окружающих тканей. Активированные макрофаги выделяют весь спектр своих секреторных продуктов. Он включает разнообразные провоспалительные факторы и факторы бактерицидности. К последним относят активные формы кислорода, их галоидные производные, оксид азота и его дериваты, ферменты и т.д. Среда в окружении таких клеток закисляется. Поскольку контакт макрофагов с Thl-клетками к этому моменту прекращается, секреция уже не носит ориентированного характера. Выделяемые молекулы выступают как факторы внеклеточной микробицидности и одновременно вызывают повреждение окружающих нормальных клеток организма. Таким образом, продукты Th1-клеток дополнительно усиливают воспалительную реакцию, в то же время придавая ей специфичность в отношении конкретных возбудителей.
Иммунное воспаление.
Вариант воспаления, реализуемый с участием Th1-клеток, называют иммунным воспалением, а
Иммунное воспаление.
Вариант воспаления, реализуемый с участием Th1-клеток, называют иммунным воспалением, а



























 Паратозилярлы абцесс
Паратозилярлы абцесс Особенности влияния различных заболеваний на эмоциональную сферу взрослых и детей
Особенности влияния различных заболеваний на эмоциональную сферу взрослых и детей Онкогенные вирусы. Особенности противоопухолевого иммунитета
Онкогенные вирусы. Особенности противоопухолевого иммунитета Коклюш у детей
Коклюш у детей Бронхоскопия. Показания. Противопоказания
Бронхоскопия. Показания. Противопоказания Физическая реабилитация при сколиозе II степени у детей 14-16 лет
Физическая реабилитация при сколиозе II степени у детей 14-16 лет Первая помощь при кровотечениях
Первая помощь при кровотечениях Питание ребенка дошкольного возраста (4-7 лет)
Питание ребенка дошкольного возраста (4-7 лет) Справка по заполнению формы «Перечень обособленных подразделений ЛПУ (без ФАП и ФП), требующих подключения к сети Интернет
Справка по заполнению формы «Перечень обособленных подразделений ЛПУ (без ФАП и ФП), требующих подключения к сети Интернет Факторы неспецифической и специфической защиты организма. Понятие об антигенах и антителах. Иммунокомпетентные клетки
Факторы неспецифической и специфической защиты организма. Понятие об антигенах и антителах. Иммунокомпетентные клетки Психологические и этические аспекты профессиональной деятельности фармацевтов
Психологические и этические аспекты профессиональной деятельности фармацевтов Функциональная анатомия височно-нижнечелюстного сустава (ВНЧС)
Функциональная анатомия височно-нижнечелюстного сустава (ВНЧС) Гемолитико-уремический синдром (болезнь Гассера)
Гемолитико-уремический синдром (болезнь Гассера) Комп'ютерна залежність - ознаки, стадії, причини виникнення та профілактика. Селфіманія - хвороба чи спосіб самовираження
Комп'ютерна залежність - ознаки, стадії, причини виникнення та профілактика. Селфіманія - хвороба чи спосіб самовираження Патология терморегуляции. Гипертермия и лихорадка. Стадии, виды, значение
Патология терморегуляции. Гипертермия и лихорадка. Стадии, виды, значение Что такое страх
Что такое страх Психология
Психология Психологія колективу
Психологія колективу Эргономические основы массажа
Эргономические основы массажа Постинсультная депрессия и деменция
Постинсультная депрессия и деменция Несбалансированное питание и развитие костно–суставных заболеваний
Несбалансированное питание и развитие костно–суставных заболеваний Язвенная болезнь желудка и двенадцатиперстной кишки
Язвенная болезнь желудка и двенадцатиперстной кишки Гигиеническая и хирургическая обработка рук современными методами
Гигиеническая и хирургическая обработка рук современными методами Управление конфликтами. Тема 10
Управление конфликтами. Тема 10 Введение в рентгенологию. Лекция №1
Введение в рентгенологию. Лекция №1 Аллергические реакции
Аллергические реакции Дисграфия
Дисграфия Психолого-педагогическая характеристика детей с особыми образовательными потребностями
Психолого-педагогическая характеристика детей с особыми образовательными потребностями