Содержание
- 2. Вероятность развития патогенной аутоиммунной агрессии в процессе, сенсибилизации зависит от свойств Аг, характера иммунной реакции, механизмов
- 3. Таким образом аутоиммунные процессы являются «зеркальным» отражением, естественной аутотолерантности, демонстрируя утрату организмом толерантности к «своим» Аг,
- 4. В первом случае условно можно говорить о так называемых иммунобиологических надзорных (ИБН-зависимых) болезнях иммунной аутоагрессии- образование
- 5. В норме в организме системная иммунологическая толерантность к Aг иммунопривилегированных органов отсутствует. С этим связана опасность
- 6. 1.НАРУШЕНИЕ БАЗОВОГО МЕХАНИЗМА ИНДУКЦИИ АУТОТОЛЕРАНТНОСТИ-КЛОНАЛЬНОЙ ДЕЛЕЦИИ Клональная делеция (clonal deletion) – уничтожение клона Т- или В-лимфоцитов
- 7. При дефиците гена AIRE в тимусе нет ткань-специфичных белков, По этому не происходит элиминация аутотолерантных Т-клеток-клонов
- 8. 2.Нарушение механизма редактирования гена аутоспецифических рецепторов А. Два Т-клеточных рецептора на одном лимфоците. Peаранжировка генов TCR
- 9. В. Нарушение периферической анергии клонов Нарушение баланса между пролиферацией и апоптозом лимфоцитов. Причины последствия различных мутаций,
- 11. Фенотипические проявления. В основе лежат усиление лимфопролиферации и активации аутoспецифических клонов лимфоцитов: Накопление клеток фенотипа CD3:TCRaB+
- 12. 3. Нарушение периферической аутотолерантности Естественные мутации, обусловливающие развитие aутoимиyнной патологии на основе нарушения анергии аутоспецифических лимфоцитов
- 13. Примером нарушений может служить активация Т-клеток В-клетками. Наряду с продукцией аутоантител В-клетки играют в регуляции Т-клеточного
- 14. Это обеспечивает оптимальные условия для активации, пролиферации и выживаемости аутореактивных CD4 T-клеток и увеличения секреции ими
- 15. А. Аутоиммунные процессы обусловленные перекрёстными реакциями Феномен антигенной мимикрии патогенов (внедрение в органзм Ar-детерминант, сходных с
- 16. Это является характерной чертой вирусных и/или ряла бактериальных инфекций. При лейшманиoзе, такому механизму развиваются анемия; Миокардит
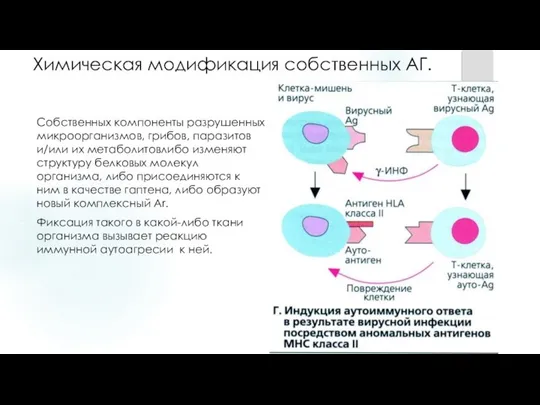
- 17. Химическая модификация собственных АГ. Собственных компоненты разрушенных микроорганизмов, грибов, паразитов и/или их метаболитовлибо изменяют структуру белковых
- 18. Нарушение оптимального соотношения в системе идиотип-адиотип Сопровождается деструкцией тканей патогеном. Перекрестная реактивность развивается при аутоиммунных процессов
- 19. Причинами нарушения оптимального соотношения в системе идиотип-антиидиотип могут быть: Дефицит T-супрессоров (например, при наследственных при обретенных
- 21. 4.Нарушение функций регуляторных Т-лимфоцитов Нарушение супрессорной активности Treg-клеток от экспрессии транскрипционного фактора FoxpЗ, связанного с Х-
- 22. функциональные отклонения Функциональные отклонения и поликлональная Aг-неспецифическая активация Т- и В-лимфоцитов с неадаптивным формированием клеток памяти
- 23. Регенерация лимфоидной ткани Регенерация лимфоидной ткани (опосредованная гомеостатической рацией Т-лимфоцитов). Вновь формирующиеся клетки отличающиеся наивных Т-лимфоцитов,
- 25. Скачать презентацию





















 Ультразвуковое исследование легких и плевры
Ультразвуковое исследование легких и плевры Предмет і завдання психіатрії та наркології. Класифікація психічних розладів і захворювань
Предмет і завдання психіатрії та наркології. Класифікація психічних розладів і захворювань Печень. Поджелудочная железа. Гистология
Печень. Поджелудочная железа. Гистология Спортивная медицина
Спортивная медицина Энцефалиты
Энцефалиты Завтрак школьника в условиях пандемии
Завтрак школьника в условиях пандемии Жұқпалы ауру және жүктілік
Жұқпалы ауру және жүктілік Антиген
Антиген Гемолитические анемии
Гемолитические анемии Мотивационно-потребностная сфера подростков(11-14 лет)
Мотивационно-потребностная сфера подростков(11-14 лет) Способности и прирожденные условия развития способностей
Способности и прирожденные условия развития способностей История и перспективы развития медико-социальной экспертизы Санкт-Петербурга. К 100-летию службы МСЭ
История и перспективы развития медико-социальной экспертизы Санкт-Петербурга. К 100-летию службы МСЭ Сердце. Физиология
Сердце. Физиология Агранулоцитарная ангина
Агранулоцитарная ангина Психология, патопсихология и психопатология сознания
Психология, патопсихология и психопатология сознания Ощущение, восприятие, память (занятие 14)
Ощущение, восприятие, память (занятие 14) Еңбек жағдайының гигиеналық бағалау критерийлері мен жіктелуі
Еңбек жағдайының гигиеналық бағалау критерийлері мен жіктелуі Гиповолемический шок
Гиповолемический шок Сестринский уход за пациентами с заболеваниями глотки
Сестринский уход за пациентами с заболеваниями глотки Патофизиология системы иммунобиологического надзора. Иммунодефицитные и иммунодепрессивные состояния. (Лекция 9, 10, 11)
Патофизиология системы иммунобиологического надзора. Иммунодефицитные и иммунодепрессивные состояния. (Лекция 9, 10, 11) Психологические особенности межличностных отношений в подростковом возрасте
Психологические особенности межличностных отношений в подростковом возрасте Топография таза и операции на органах таза
Топография таза и операции на органах таза Особенности новорожденного ребенка
Особенности новорожденного ребенка Высшая нервная деятельность
Высшая нервная деятельность ЭКГ в норме и при основных поражениях сердца
ЭКГ в норме и при основных поражениях сердца Анализ многолетней динамики заболеваемости в эпидемиологической диагностике
Анализ многолетней динамики заболеваемости в эпидемиологической диагностике Перфоративная язва желудка и двенадцатиперстной кишки
Перфоративная язва желудка и двенадцатиперстной кишки Темперамент
Темперамент