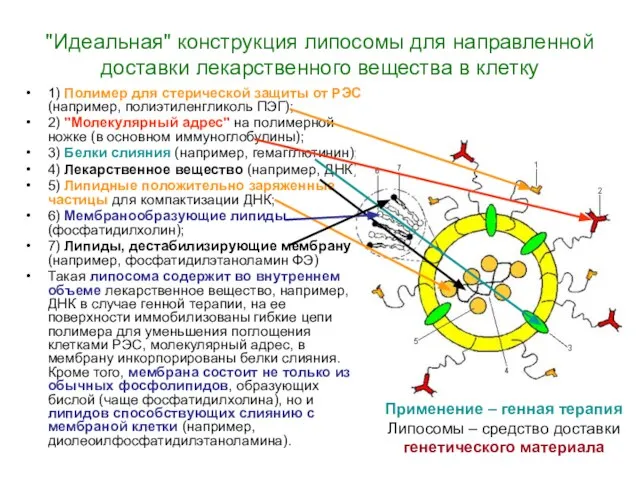
"Идеальная" конструкция липосомы для направленной доставки лекарственного вещества в клетку
1) Полимер
для стерической защиты от РЭС (например, полиэтиленгликоль ПЭГ);
2) "Молекулярный адрес" на полимерной ножке (в основном иммуноглобулины);
3) Белки слияния (например, гемагглютинин);
4) Лекарственное вещество (например, ДНК);
5) Липидные положительно заряженные частицы для компактизации ДНК;
6) Мембранообразующие липиды (фосфатидилхолин);
7) Липиды, дестабилизирующие мембрану (например, фосфатидилэтаноламин ФЭ)
Такая липосома содержит во внутреннем объеме лекарственное вещество, например, ДНК в случае генной терапии, на ее поверхности иммобилизованы гибкие цепи полимера для уменьшения поглощения клетками РЭС, молекулярный адрес, в мембрану инкорпорированы белки слияния. Кроме того, мембрана состоит не только из обычных фосфолипидов, образующих бислой (чаще фосфатидилхолина), но и липидов способствующих слиянию с мембраной клетки (например, диолеоилфосфатидилэтаноламина).
Применение – генная терапия
Липосомы – средство доставки генетического материала


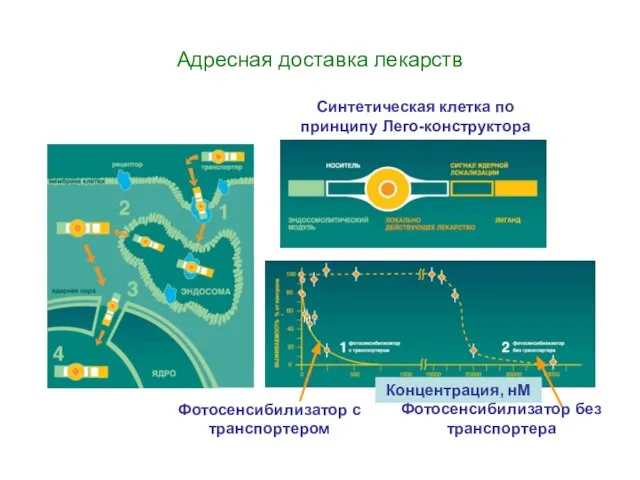
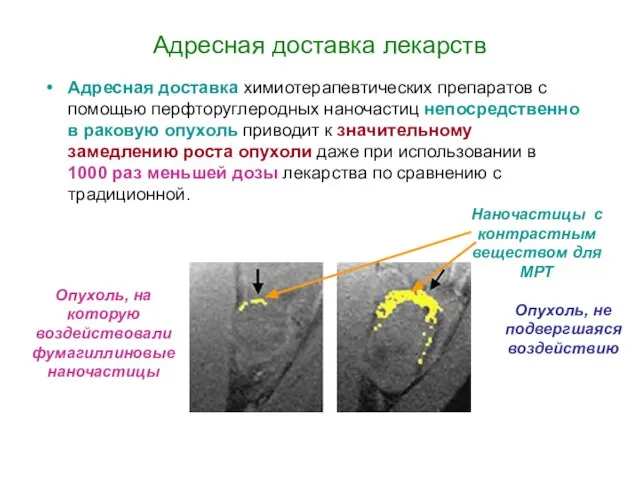


 Медицинский туризм в Югре
Медицинский туризм в Югре Общий анализ крови. Лейкоцитарная и тромбоцитарная форма
Общий анализ крови. Лейкоцитарная и тромбоцитарная форма Вирус клещевого энцефалита
Вирус клещевого энцефалита Оқытушы мен студенттің тұлғааралық өзара әрекеттесігінің мәселелері
Оқытушы мен студенттің тұлғааралық өзара әрекеттесігінің мәселелері Болезни печени
Болезни печени Л. С. Выготский. Развитие личности. Стадии и стратегии
Л. С. Выготский. Развитие личности. Стадии и стратегии Глазные лекарственные средства
Глазные лекарственные средства Діти із розумовою відсталістю, діти із захворюваннями нервової системи. Лекція 6
Діти із розумовою відсталістю, діти із захворюваннями нервової системи. Лекція 6 Қазақстан Республикасында мүгедектерді әлеуметтік қорғау
Қазақстан Республикасында мүгедектерді әлеуметтік қорғау Ревматические болезни. Пороки сердца
Ревматические болезни. Пороки сердца Конфликтология как наука. Становление конфликтологии
Конфликтология как наука. Становление конфликтологии Особенности организации медико-социального патронажа
Особенности организации медико-социального патронажа Армысыңдар менің бауырларым мен қарындастарым. Болашақ тигрлер ( жолбарыстар)
Армысыңдар менің бауырларым мен қарындастарым. Болашақ тигрлер ( жолбарыстар) Эффективность сестринского ухода за пациентом с пневмонией
Эффективность сестринского ухода за пациентом с пневмонией Туберкулез женских половых органов
Туберкулез женских половых органов Ведение беременности и родов при тазовом предлежании плода. Многоводие и маловодие
Ведение беременности и родов при тазовом предлежании плода. Многоводие и маловодие Родовой травматизм матери
Родовой травматизм матери Сепсис. Классификация
Сепсис. Классификация Гигиена и режим беременной женщины. Урок № 69
Гигиена и режим беременной женщины. Урок № 69 «Трудные» сотрудники
«Трудные» сотрудники Айқасқан тістем
Айқасқан тістем Повреждения груди
Повреждения груди Paediatric Anaesthesia
Paediatric Anaesthesia Сериал «Притяжение». День 3
Сериал «Притяжение». День 3 Методы эмпирического уровня
Методы эмпирического уровня Особенности болевого синдрома в паллиативной педиатрии
Особенности болевого синдрома в паллиативной педиатрии Коллаген гетерологичный I типа биологического происхождения биорепарант
Коллаген гетерологичный I типа биологического происхождения биорепарант Базовые реанимационные мероприятия
Базовые реанимационные мероприятия