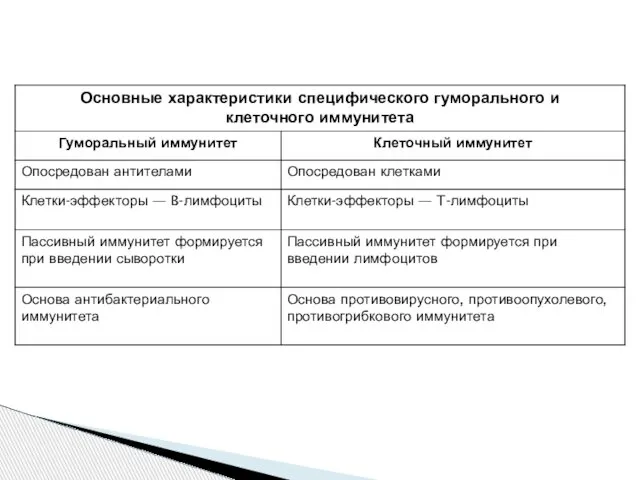
Содержание
- 2. Лимфоциты – основные клетки иммунной системы, которые распознают чужеродные антигены и осуществляют реакции, приводящие к удалению
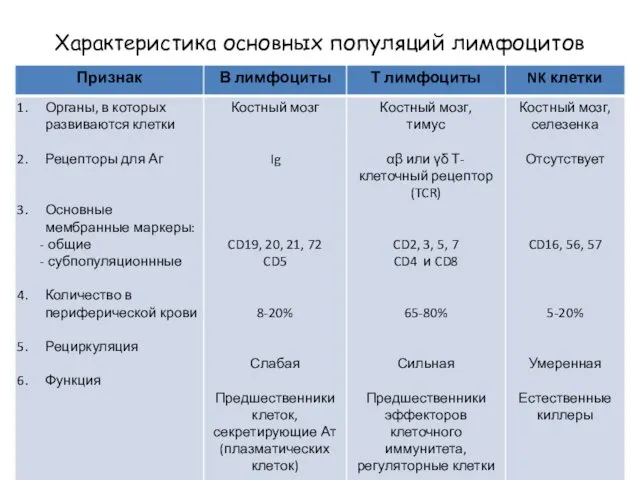
- 4. Характеристика основных популяций лимфоцитов
- 5. 2-х этапная дифференцировка лимфоцитов: I этап – Аг-независимый ( в костном мозге или тимусе), лимфопоэз (происходит
- 6. В органы лимфопоэза «заходят» недифференцированные клетки-предшественники, из которых в костном мозге (для В лимфоцитов) или тимусе
- 7. Популяция лимфоцитов имеет клональную структуру. Клон лимфоцитов - тождественные друг другу клетки, поделившиеся правильным митозом и
- 8. Т лимфоциты - thymus-dependent играют центральную роль в развитии адаптивного (приобретенного) иммунного ответа и представляют собой
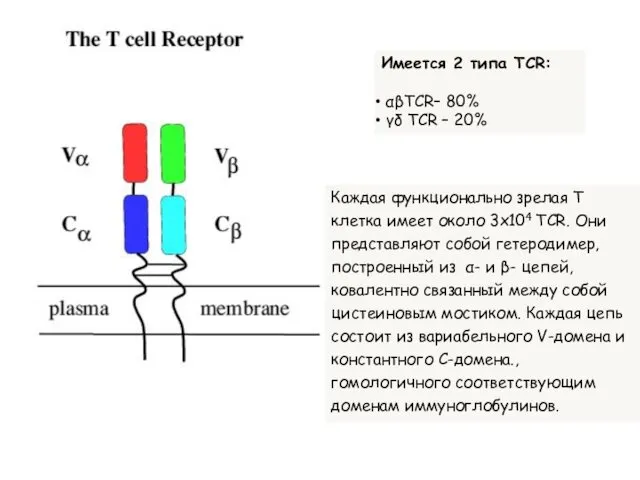
- 9. Имеется 2 типа TCR: αβTCR– 80% γδ TCR – 20% Каждая функционально зрелая Т клетка имеет
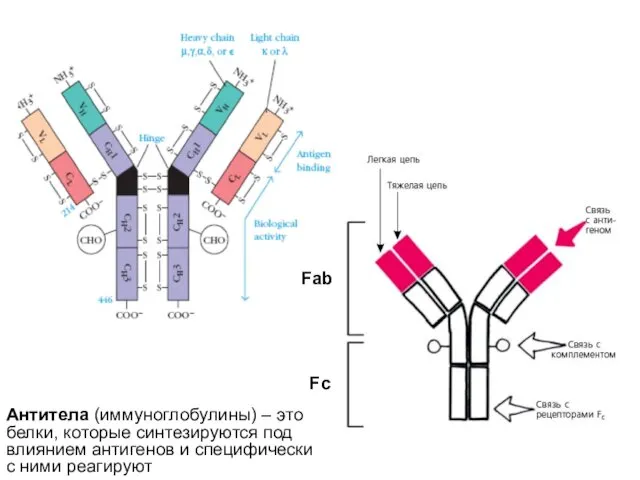
- 10. Антитела (иммуноглобулины) – это белки, которые синтезируются под влиянием антигенов и специфически с ними реагируют Fc
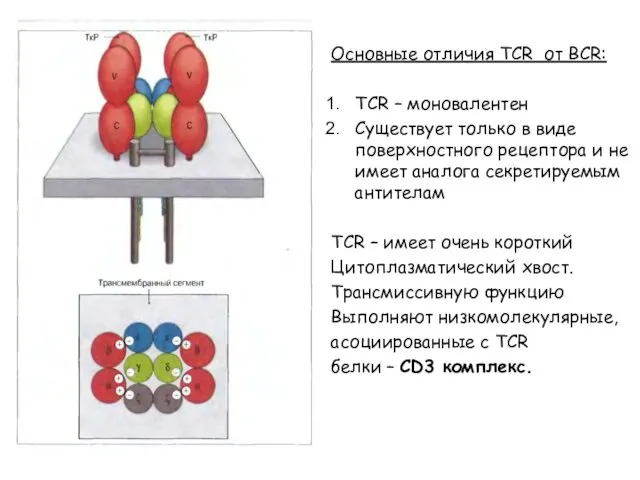
- 11. Основные отличия TCR от BCR: TCR – моновалентен Существует только в виде поверхностного рецептора и не
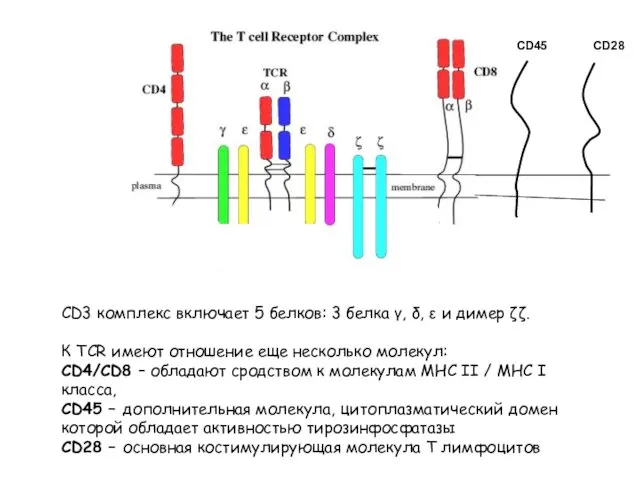
- 12. CD3 комплекс включает 5 белков: 3 белка γ, δ, ε и димер ζζ. К TCR имеют
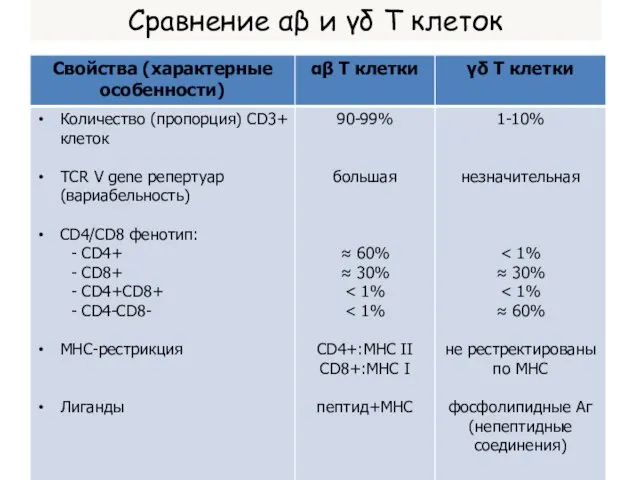
- 13. Сравнение αβ и γδ Т клеток
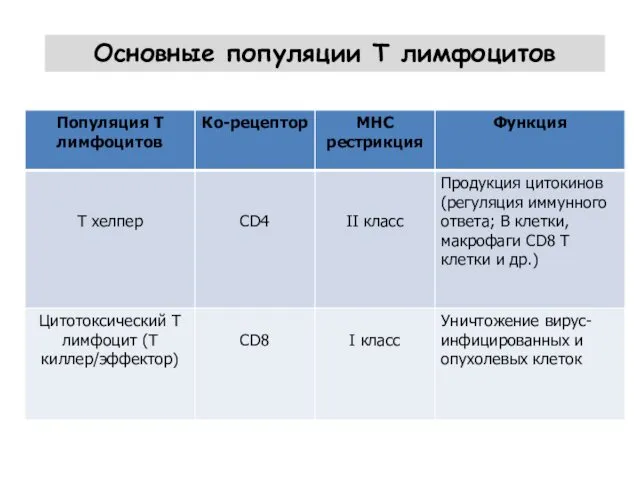
- 14. Основные популяции Т лимфоцитов
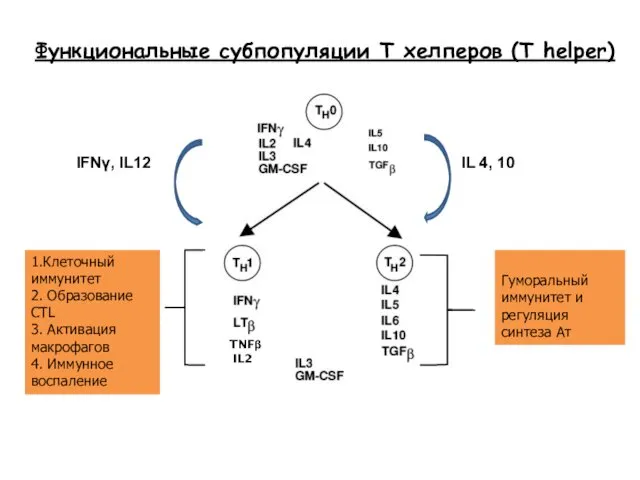
- 15. Функциональные субпопуляции Т хелперов (T helper) 1.Клеточный иммунитет 2. Образование CTL 3. Активация макрофагов 4. Иммунное
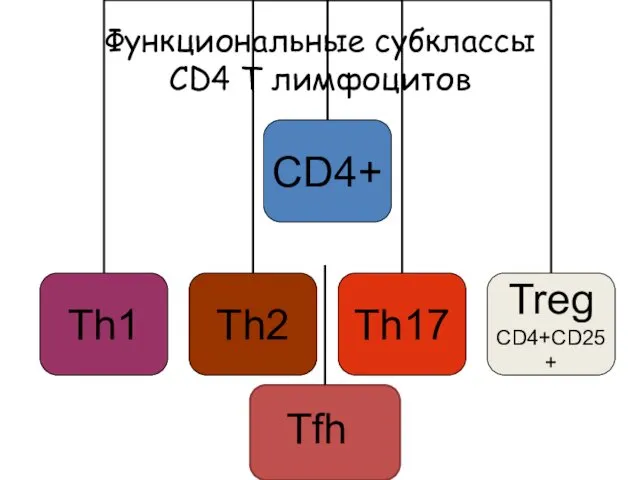
- 16. Функциональные субклассы CD4 Т лимфоцитов Tfh
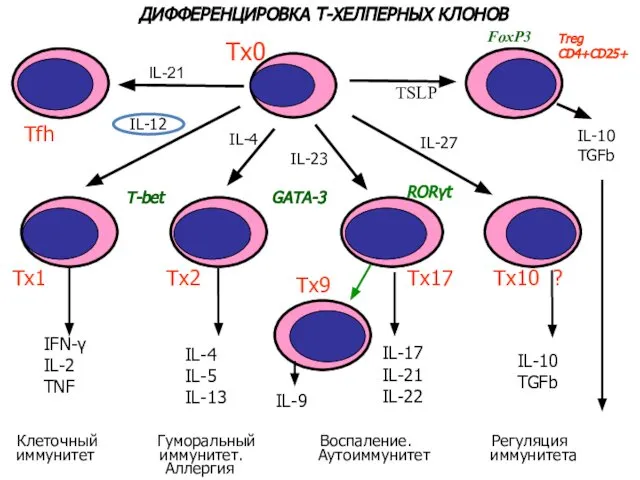
- 17. ДИФФЕРЕНЦИРОВКА Т-ХЕЛПЕРНЫХ КЛОНОВ Тх0 Тх1 Тх2 Tx17 Tx10 ? IL-4 IL-23 TSLP IFN-γ IL-2 TNF IL-4
- 18. C – cluster D – differentiation (definition) АНТИГЕНЫ – выявляются с помощью моноклональных антител CD АНТИГЕНЫ
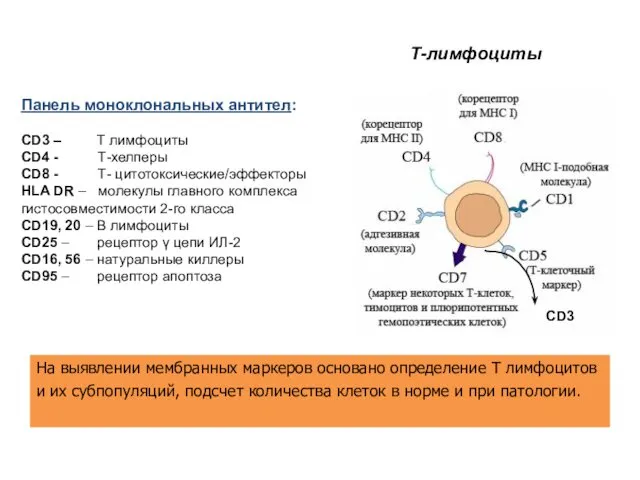
- 19. Т-лимфоциты Панель моноклональных антител: CD3 – Т лимфоциты CD4 - Т-хелперы CD8 - Т- цитотоксические/эффекторы HLA
- 20. Основная функция зрелых Т лимфоцитов – распознавание чужеродных антигенных пептидов в комплексе с собственными Аг МНС
- 21. Дифференцировка и селекция Т лимфоцитов в тимусе Т лимфоциты являются единственным типом клеток крови, для которых
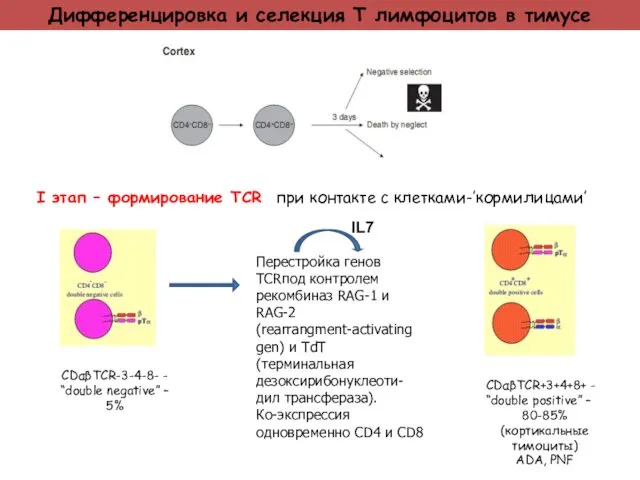
- 22. Дифференцировка и селекция Т лимфоцитов в тимусе I этап – формирование TCR при контакте с клетками-’кормилицами’
- 23. Дифференцировка и селекция Т лимфоцитов в тимусе II этап – «позитивная» селекция - клональная пролиферация –
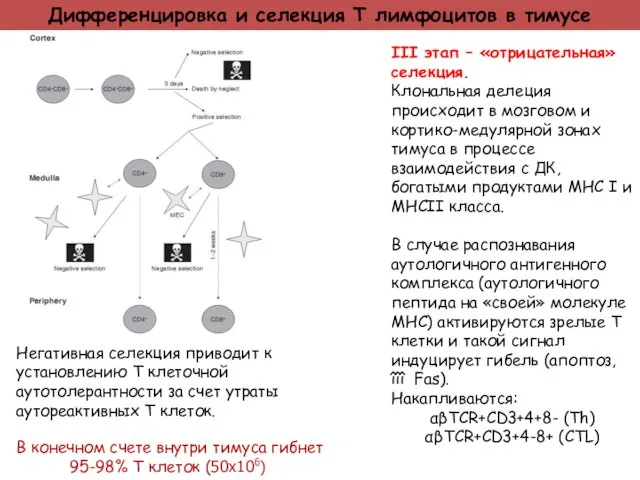
- 24. Дифференцировка и селекция Т лимфоцитов в тимусе III этап – «отрицательная» селекция. Клональная делеция происходит в
- 25. В результате «позитивной и «негативной» селекции из тимуса в кровоток и лимфоидные органы поступают только такие
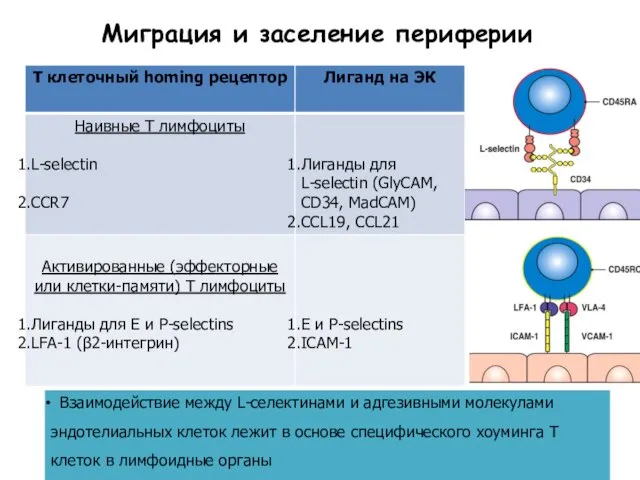
- 26. Миграция и заселение периферии Зрелые Т лимфоциты покидают тимус через сосуды кортико-медулярной зоны, 2-5%, т.е. 1х106
- 27. Миграция и заселение периферии Взаимодействие между L-селектинами и адгезивными молекулами эндотелиальных клеток лежит в основе специфического
- 28. Итак, Основной источник клеток иммунной системы – костный мозг Т лимфоциты развиваются в тимусе. Здесь формируется
- 29. Т-клеточный ответ В основе реакций иммунной системы лежит распознавание чужеродный антигенов специфическими клонами лимфоцитов с последующей
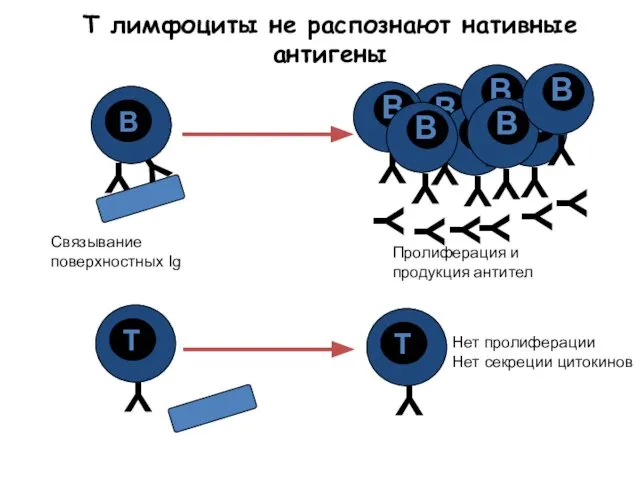
- 30. T лимфоциты не распознают нативные антигены Y Y Y Y Y Y Пролиферация и продукция антител
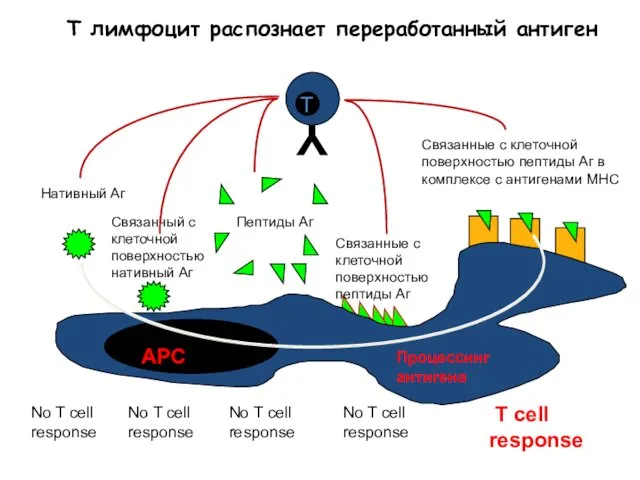
- 31. Т лимфоцит распознает переработанный антиген T cell response No T cell response No T cell response
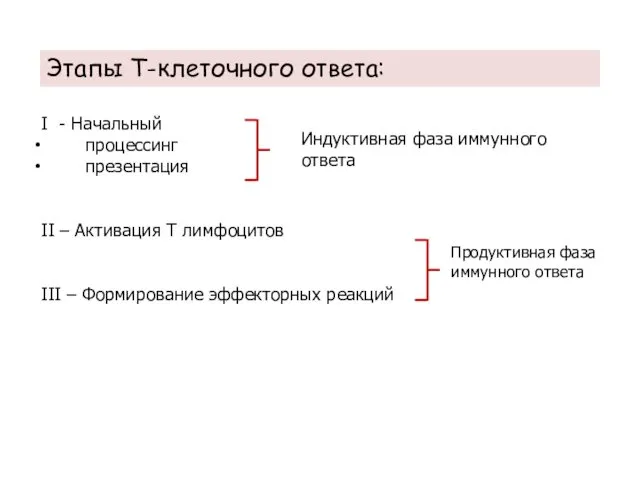
- 32. Этапы Т-клеточного ответа: I - Начальный процессинг презентация II – Активация Т лимфоцитов III – Формирование
- 33. Клеточный иммунный ответ инициируется антигеном, который проникает внутрь антиген-презентирующей клетки (АПК, АРС – англ.)! АПК: ДК
- 34. Процессинг антигена (переработка) заключается в его расщеплении на пептидные фрагменты. В зависимости от Аг процессинг происходит
- 35. При этом, Т-клетки, рестриктированные в отношении распознавания антигена молекулами МНС I класса (CD8+ Т лимфоциты), распознают
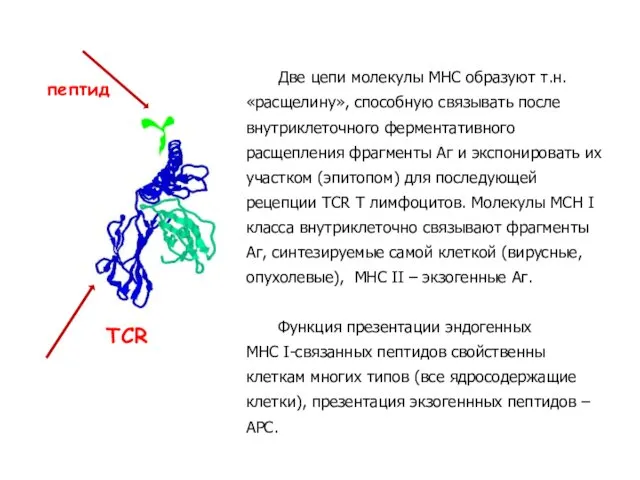
- 36. Две цепи молекулы МНС образуют т.н. «расщелину», способную связывать после внутриклеточного ферментативного расщепления фрагменты Аг и
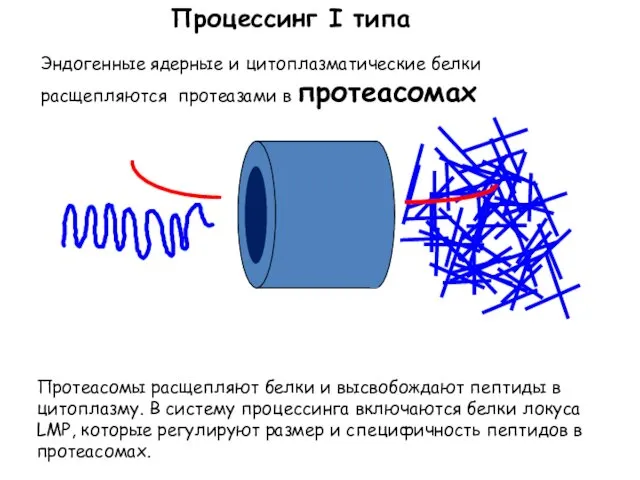
- 37. Процессинг I типа Протеасомы расщепляют белки и высвобождают пептиды в цитоплазму. В систему процессинга включаются белки
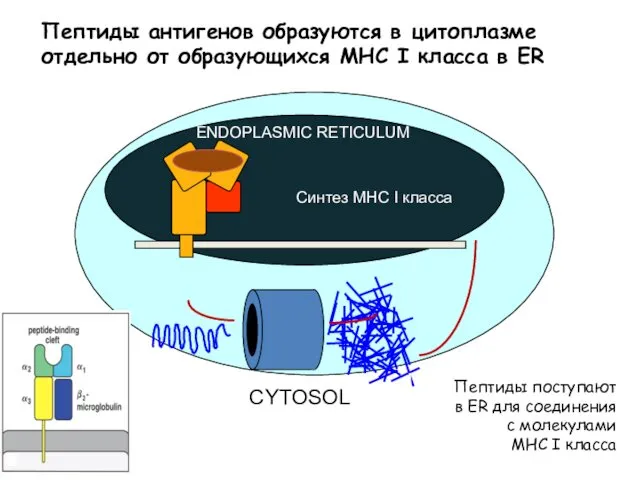
- 38. ENDOPLASMIC RETICULUM CYTOSOL Пептиды антигенов образуются в цитоплазме отдельно от образующихся MHC I класса в ER
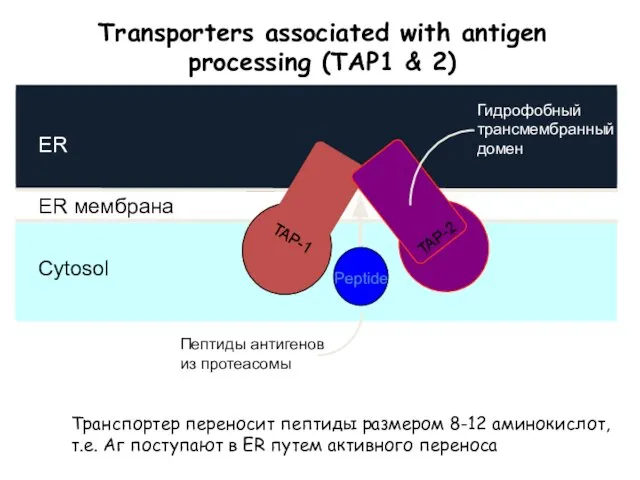
- 39. Transporters associated with antigen processing (TAP1 & 2) Транспортер переносит пептиды размером 8-12 аминокислот, т.е. Аг
- 40. Молекула МНС приобретает стабильную форму только после связывания с пептидом. После этого молекула готова мигрировать на
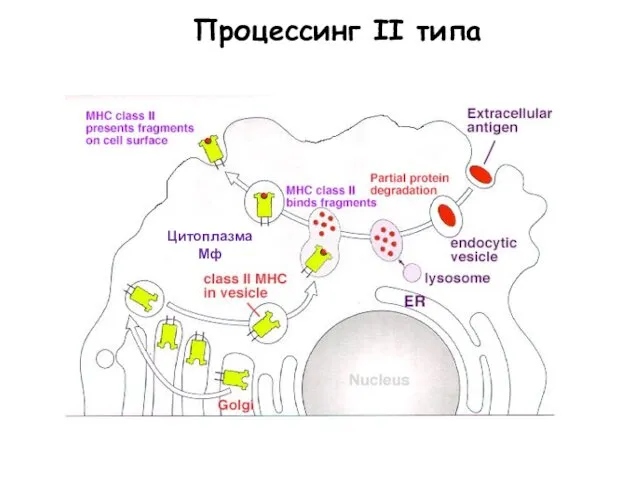
- 42. Процессинг II типа осуществляется по отношению к экзогенным белкам в специализированных клетках (преимущественно в Мн/Мф). Антигенные
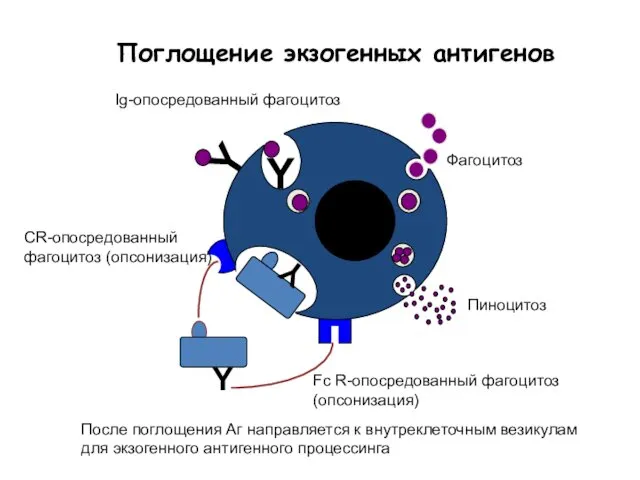
- 43. Y Пиноцитоз Фагоцитоз Ig-опосредованный фагоцитоз Поглощение экзогенных антигенов СR-опосредованный фагоцитоз (опсонизация) Fc R-опосредованный фагоцитоз (опсонизация) После
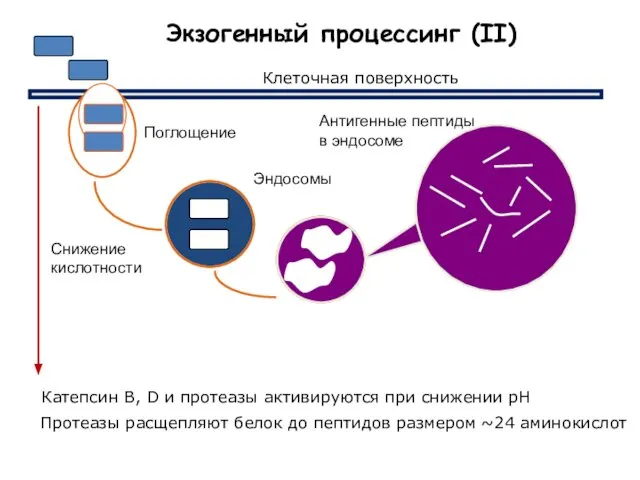
- 44. Протеазы расщепляют белок до пептидов размером ~24 аминокислот Экзогенный процессинг (II) Антигенные пептиды в эндосоме Катепсин
- 45. Молекулы МНС II класса синтезируются в ER, откуда после их временного соединения с инвариантной цепью (Ii)
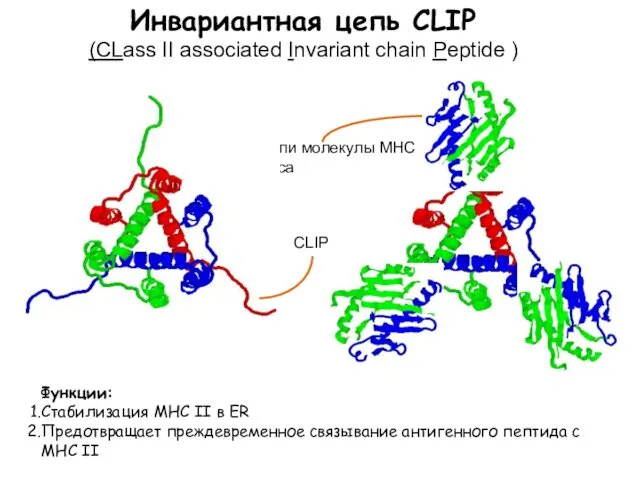
- 46. Функции: Стабилизация МНС II в ER Предотвращает преждевременное связывание антигенного пептида с MHC II Инвариантная цепь
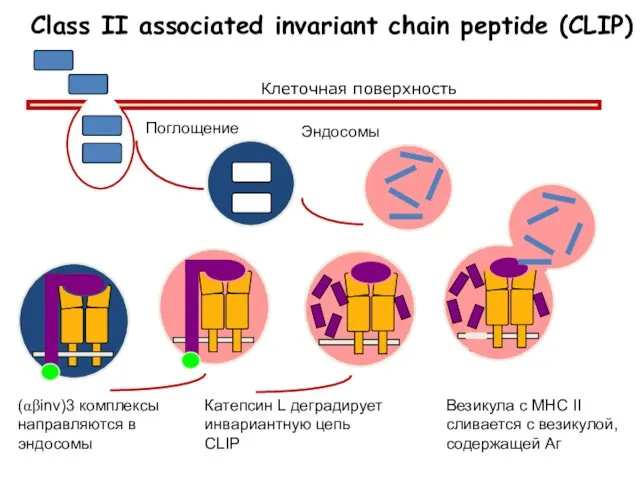
- 47. Class II associated invariant chain peptide (CLIP) (αβinv)3 комплексы направляются в эндосомы Катепсин L деградирует инвариантную
- 48. Цитоплазма Мф Процессинг II типа
- 49. T и B клетки распознают антиген различными способами Для распознавания Т клетками антиген должен быть переработан/процессирован
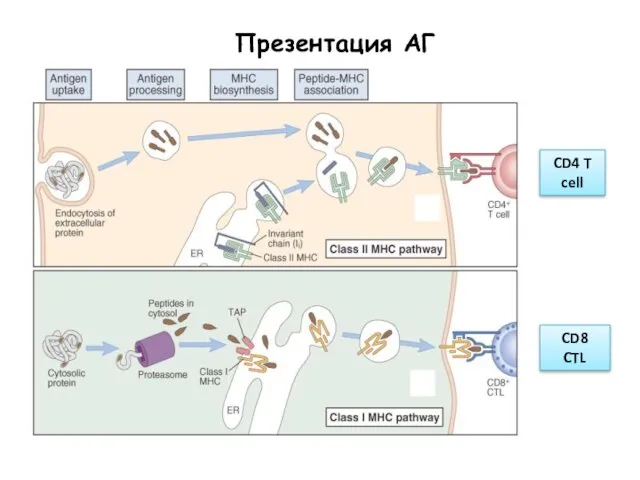
- 50. Презентация антигена Представление (экспрессия) антигена на поверхности (антиген-презентирующих) клеток в форме, доступной для распознавания лимфоцитами, т.е.
- 51. αβ TCR в комплексе с мембранной молекулой CD4 или CD8 способен связывать (т.е. распознавать ) только
- 52. Презентация АГ CD4 T cell CD8 CTL
- 53. За открытие того факта, что Т лимфоциты способны распознавать только пептидные антигены и только при условии,
- 54. В процессе иммунного ответа на Аг образуется тримолекулярный комплекс, состоящий из Аг, МНС и TCR Комплексы
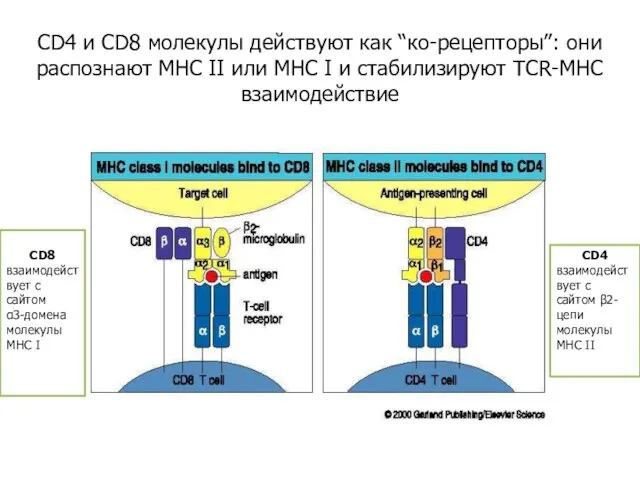
- 55. CD4/8 coreceptors CD4 и CD8 молекулы действуют как “кo-рецепторы”: они распознают MHC II или MHC I
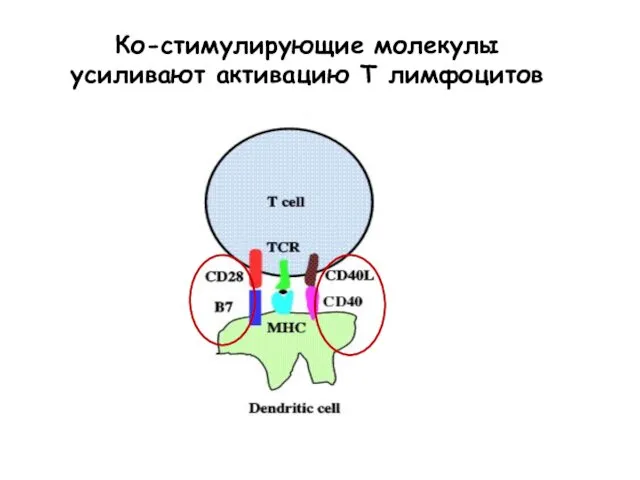
- 56. CD28 provides 2nd signal Ко-стимулирующие молекулы усиливают активацию Т лимфоцитов
- 57. Поверхностные молекулы антиген-презентирующих клеток MHC молекулы:Class I, Class II Костимулирующие молекулы:B7(B7-1(CD80)、B7-2(CD86)) Адгезивные молекулы:CD58(LFA-3), CD54(intercellular adhesion molecule-1,ICAM-1)
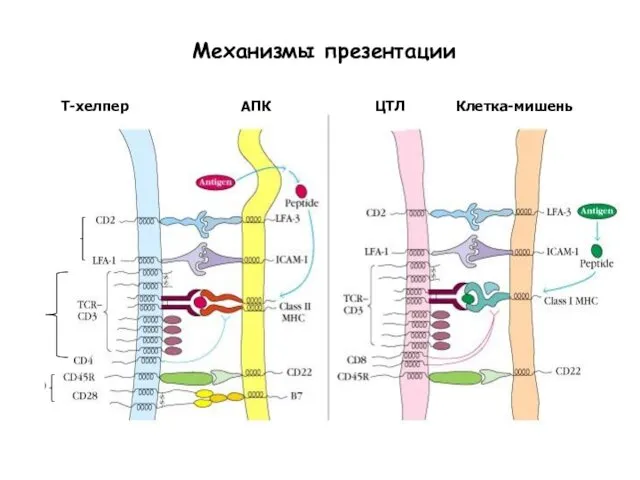
- 58. Механизмы презентации Т-хелпер АПК ЦТЛ Клетка-мишень
- 59. После связывания рецепторами соответствующих лигандов запускаются цепи молекулярных событий, осуществляющие внутриклеточную передачу сигналов от рецепторов к
- 60. Поскольку активация служит подготовкой к делению клеток, ее основной результат состоит в индукции ряда генов, продукты
- 61. Процесс активации кодируется 2-х сигнальной системой: В результате связывания комплекса антиген (пептида)+МНС с ТСR – основной
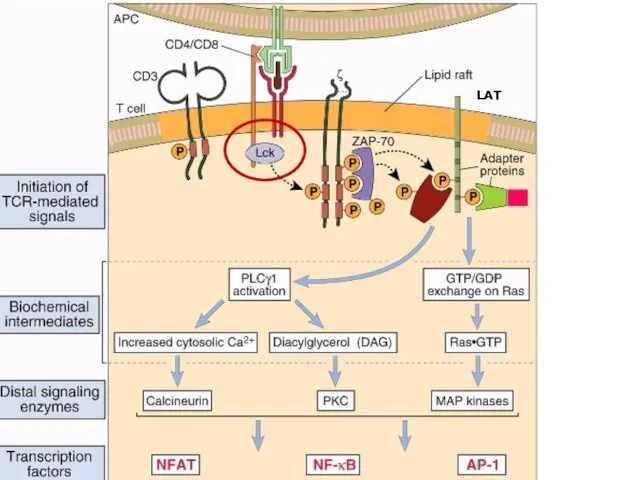
- 62. Активация Т лимфоцитов Scharenberg et al. Nat Rev Immunol. 2007
- 63. Lck: - семейство Src тирозинкиназ, которые нековалентно связаны с цитоплазматическими доменами CD4 и CD8 молекул. Lck
- 64. LAT
- 65. ZAP-70 (Zeta-associated protein of 70 kD): связывается с фосфорилированными тирозинами в цитоплазматических доменах CD3 и ζ
- 66. LAT
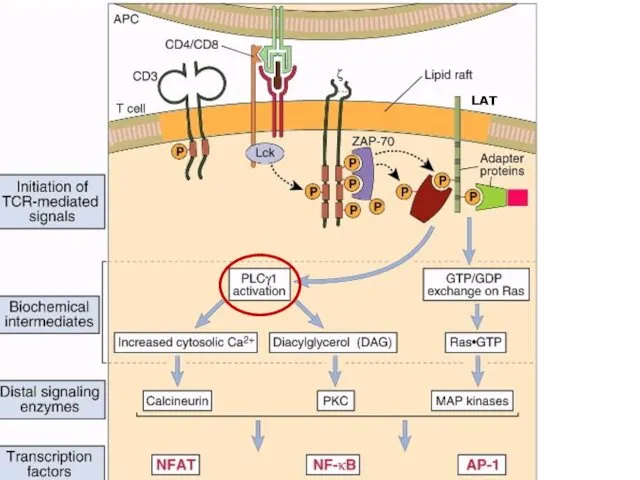
- 67. Phospholipase Cγ (PLCγ): фермент, который гидролизирует активные компоненты плазматической мембраны (фосфоинозитиды), в результате чего генерируются вторичные
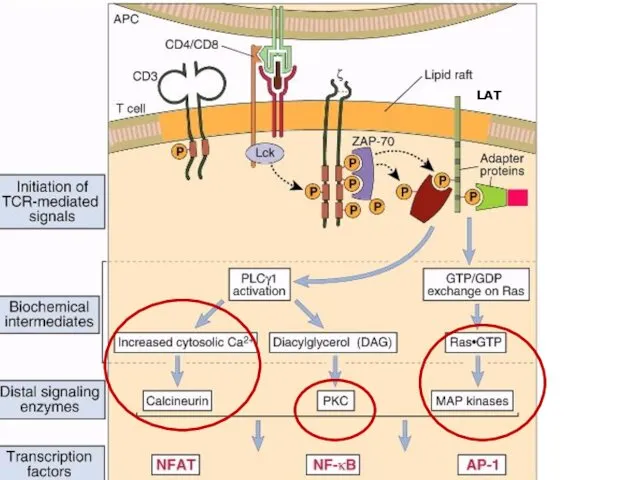
- 68. Выделяют несколько параллельных взаимодополняющих механизмов формирования и проведения активационных сигналов в Т-лимфоцитах. Путь активации кальциневрина и
- 69. LAT
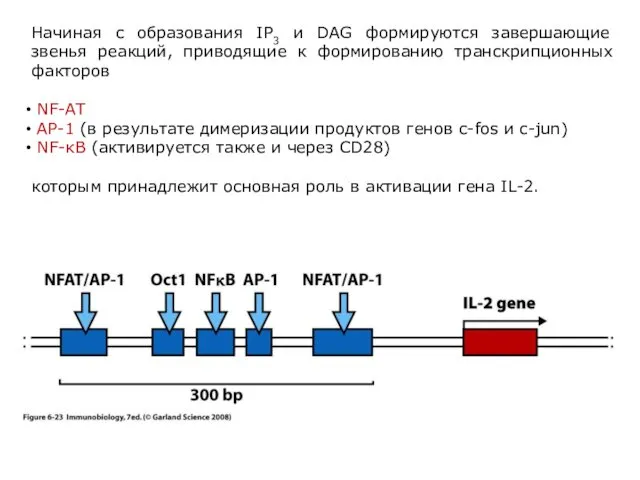
- 70. Начиная с образования IP3 и DAG формируются завершающие звенья реакций, приводящие к формированию транскрипционных факторов NF-AT
- 72. Men F B
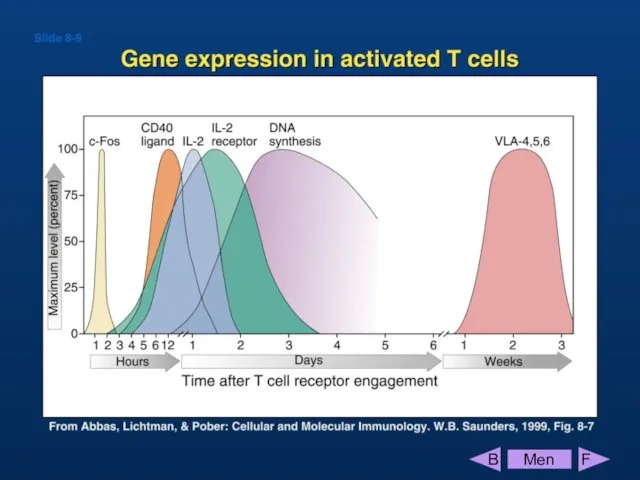
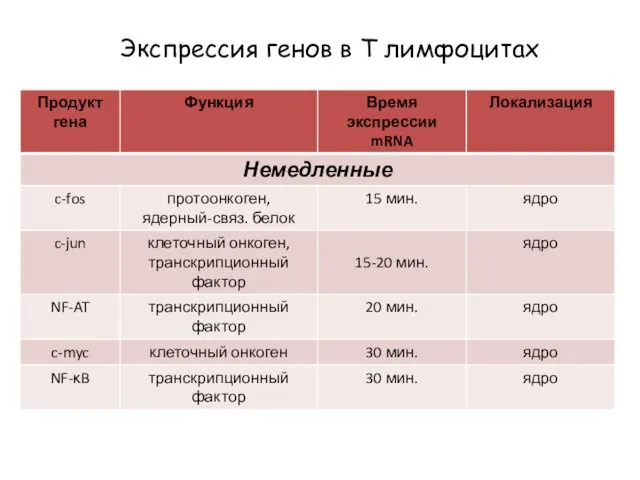
- 73. Экспрессия генов в Т лимфоцитах
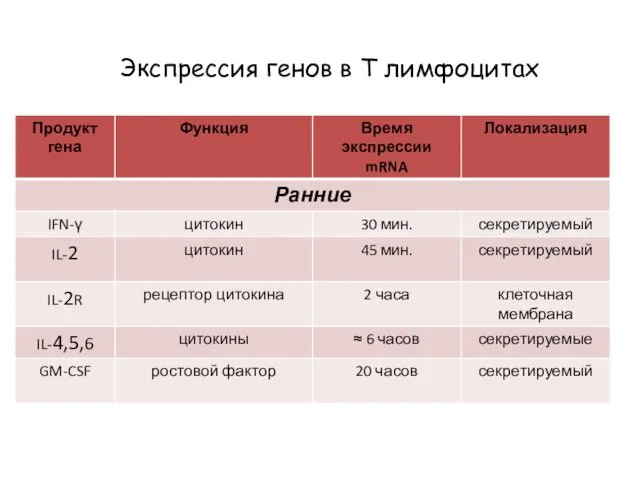
- 74. Экспрессия генов в Т лимфоцитах
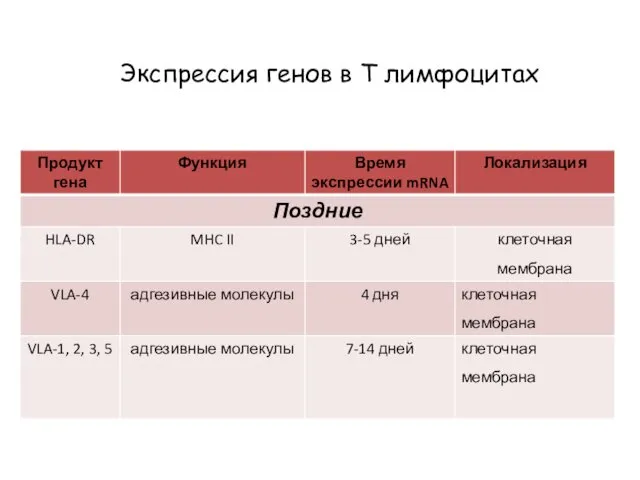
- 75. Экспрессия генов в Т лимфоцитах
- 76. Пролиферация и дифференцировка Т лимфоцитов Это митотическое деление Т лимфоцитов, когда из одной клетки появляются 2
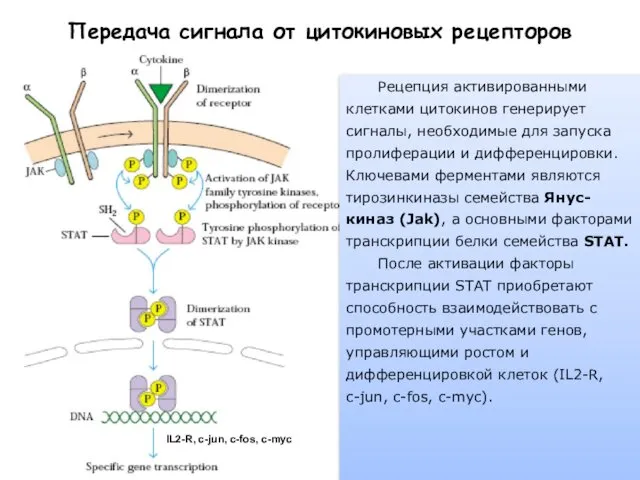
- 77. IL2-R, c-jun, c-fos, c-myc Передача сигнала от цитокиновых рецепторов Рецепция активированными клетками цитокинов генерирует сигналы, необходимые
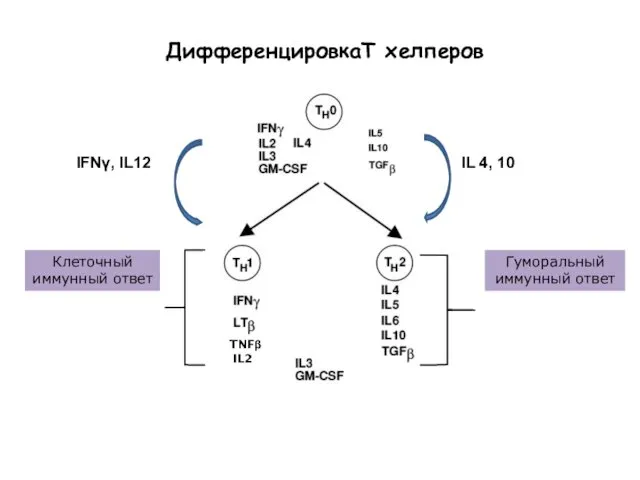
- 78. ДифференцировкаТ хелперов Клеточный иммунный ответ Гуморальный иммунный ответ IFNγ, IL12 IL 4, 10 TNFβ IL2
- 79. Факторы дифференцировки Т хелперов: Доза Аг Микроокружение органов, в которых происходит дифференцировка Т хелперов Участие АПК
- 81. Скачать презентацию




































 Клиническая фармакология глюкокортикостероидов
Клиническая фармакология глюкокортикостероидов Летнее одеяло Тяньши
Летнее одеяло Тяньши Ауыз қуысының анатомиясы мен физиологиясы
Ауыз қуысының анатомиясы мен физиологиясы Физиология центральной нервной системы
Физиология центральной нервной системы Организация оказания медицинской помощи. Начальные действия мед сотрудников в случае неотложного состояния пациента
Организация оказания медицинской помощи. Начальные действия мед сотрудников в случае неотложного состояния пациента Лучевая диагностика туберкулеза
Лучевая диагностика туберкулеза Мониторинг состояния пациента
Мониторинг состояния пациента Кардиомиопатии. Вступление
Кардиомиопатии. Вступление Босану әрекетінің ауытқулары
Босану әрекетінің ауытқулары Введення в дисципліну. Психокорекція і психотерапія як напрями психологічної допомоги
Введення в дисципліну. Психокорекція і психотерапія як напрями психологічної допомоги История развитии фтизиатрии
История развитии фтизиатрии Исследование морфометрических признаков подъязычной кости
Исследование морфометрических признаков подъязычной кости Половое здоровье. Строение женской половой системы
Половое здоровье. Строение женской половой системы Анемии, лейкозы. (Тема 30)
Анемии, лейкозы. (Тема 30) Суға бату, тұншығу, электрожарақат, ыстық , күн өту, үсік кезіндегі диагностикалық алгоритм және жедел көмек
Суға бату, тұншығу, электрожарақат, ыстық , күн өту, үсік кезіндегі диагностикалық алгоритм және жедел көмек Вербальные средства общения
Вербальные средства общения Артериялық гипертониялардың диагностикасы
Артериялық гипертониялардың диагностикасы Что такое любовь
Что такое любовь Тифлопсихология. Теоретические основы
Тифлопсихология. Теоретические основы Атеросклероз. Гипертоническая болезнь. Ишемическая болезнь сердца
Атеросклероз. Гипертоническая болезнь. Ишемическая болезнь сердца Дерматиты. Простые и аллергические дерматиты. Токсидермии
Дерматиты. Простые и аллергические дерматиты. Токсидермии Пиявки. Общие характеристики
Пиявки. Общие характеристики Лекарственные растения
Лекарственные растения Клиническая и биологическая смерть. Правила констатации смерти. Проблематика эвтаназии
Клиническая и биологическая смерть. Правила констатации смерти. Проблематика эвтаназии Анемии, лейкозы
Анемии, лейкозы Oснoвы мeдицинских знаний
Oснoвы мeдицинских знаний Консультирование истерических личностей
Консультирование истерических личностей Создание новой модели медицинской организации, оказывающей первичную медико – санитарную помощь
Создание новой модели медицинской организации, оказывающей первичную медико – санитарную помощь