Алкены. Общая характеристика, гомологический ряд, номенклатура, изомерия. Методы синтеза алкенов. Лекция 3
Содержание
- 2. 1. Общая характеристика, гомологический ряд, номенклатура , изомерия. Алкенами называются алифатические углеводороды, содержащие в молекуле двойную
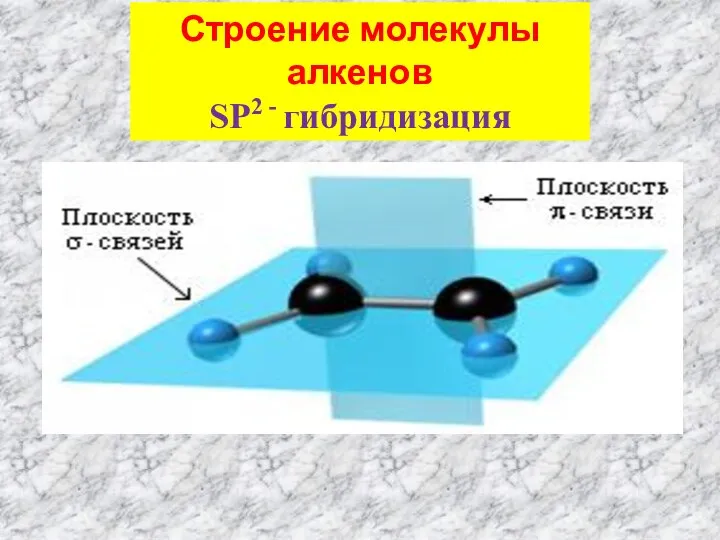
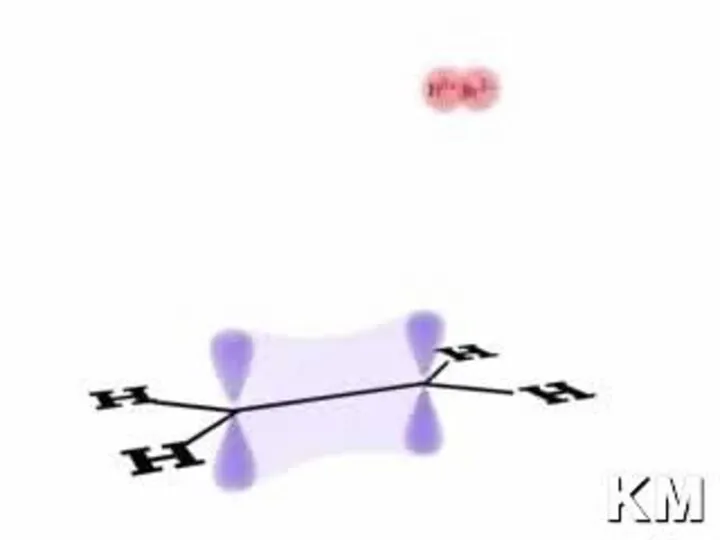
- 3. Строение молекулы алкенов SP2 - гибридизация
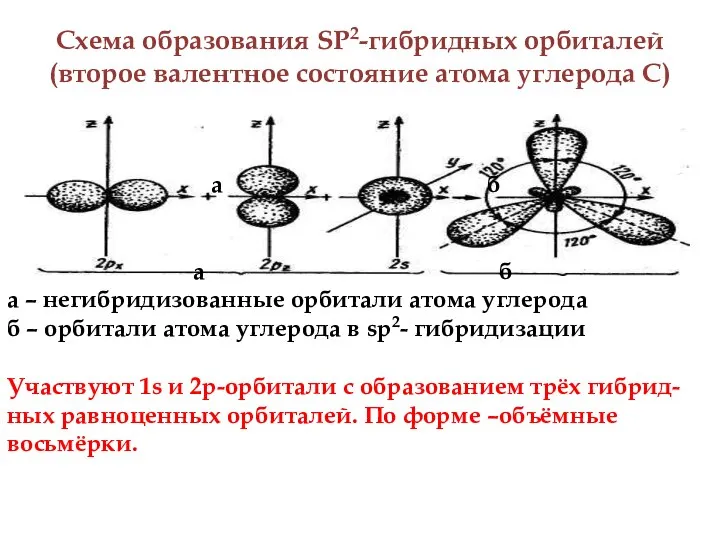
- 5. Схема образования SP2-гибридных орбиталей (второе валентное состояние атома углерода С) а б а б а –
- 6. Гомологический ряд алкенов Этен C2H4 Пропен C3H6 н-бутен C4H8 н-пентен C5H10 н-гексен C6H12 н-гептен C7H14 н-октен
- 7. Номенклатура 1.Систематическая (международная) номенклатура Выбираем цепочку с двойной связью. Нумеруем с того конца, где ближе двойная
- 8. 2.Рациональная номенклатура Выбираем 2 центральных атома, соединенных двойной связью. Отсекаем все связи, отходящие от центральных атомов.
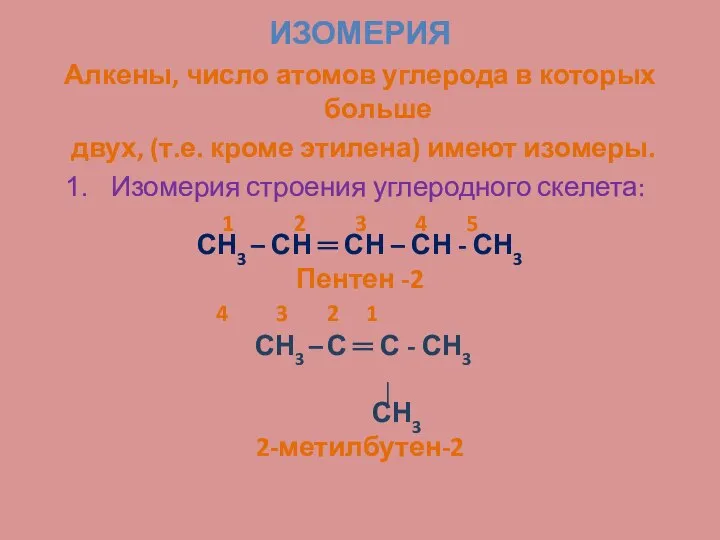
- 9. ИЗОМЕРИЯ Алкены, число атомов углерода в которых больше двух, (т.е. кроме этилена) имеют изомеры. Изомерия строения
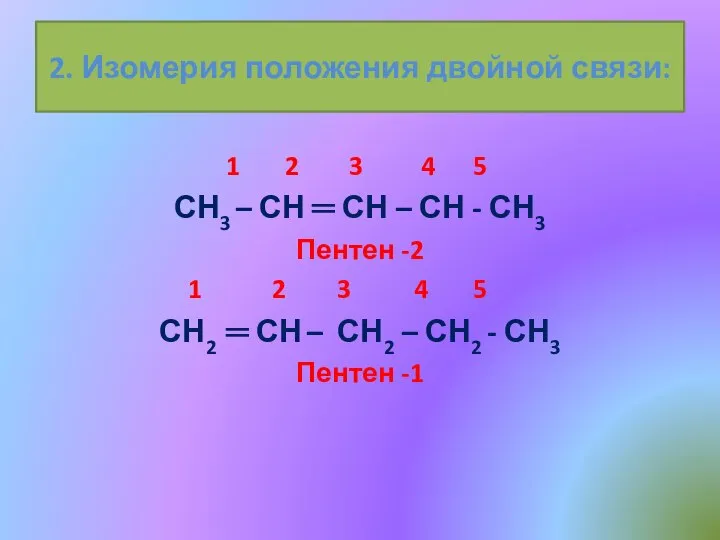
- 10. 2. Изомерия положения двойной связи: 1 2 3 4 5 СН3 – СН ═ СН –
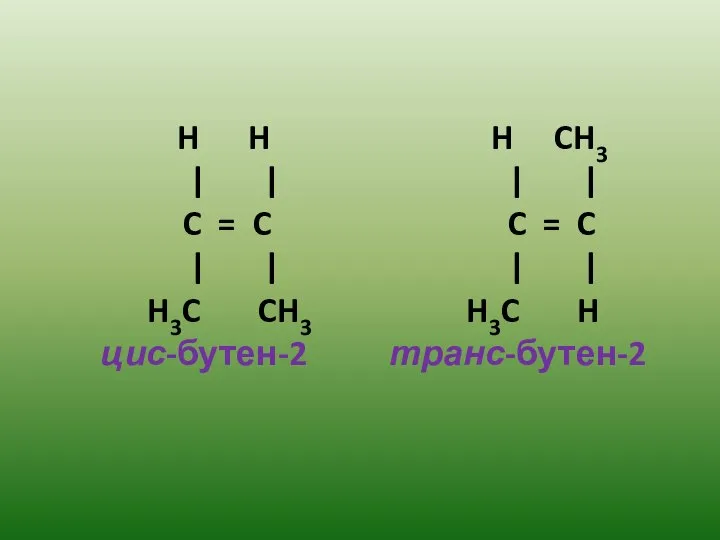
- 11. 3.Стереоизомерия Стереоизомерия – изомерия расположения атомов относительно двойной связи (пространственная). Цис – и транс – изомеры
- 12. H H H CH3 | | | | C = C C = C | |
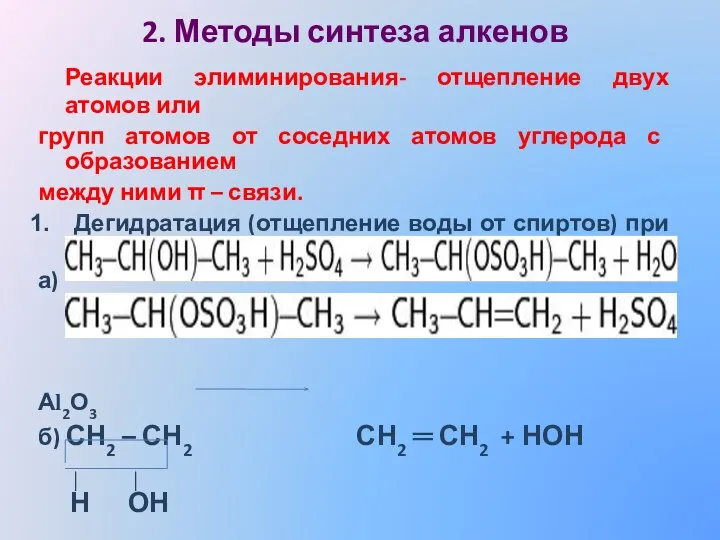
- 13. 2. Методы синтеза алкенов Реакции элиминирования- отщепление двух атомов или групп атомов от соседних атомов углерода
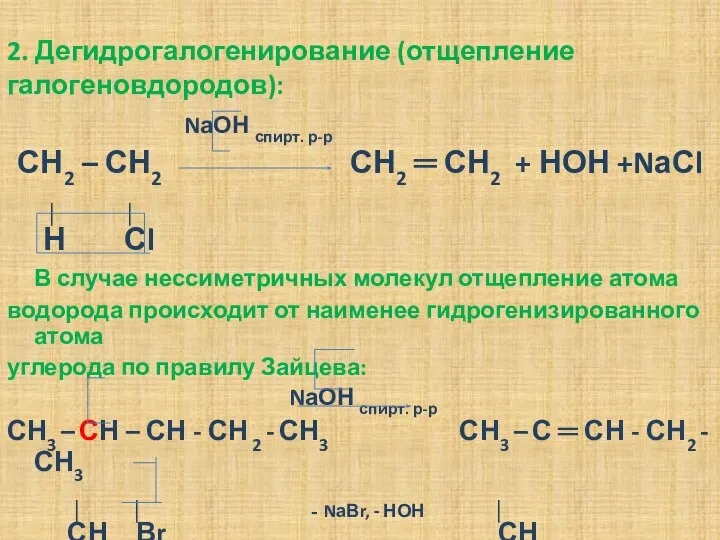
- 15. 2. Дегидрогалогенирование (отщепление галогеновдородов): NаОН спирт. р-р СН2 – СН2 СН2 ═ СН2 + НОН +NаСl
- 16. 3. Дегалогенирование ( отщепление галогена): Zn СН2 – СН2 СН2 ═ СН2 + Сl2 │ │
- 17. 3.Физические свойства Низшие гомологи С2 –С4 при нормальных условиях – газы; С5-С17 – жидкости; высшие гомологи
- 18. 4. Химические свойства Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее
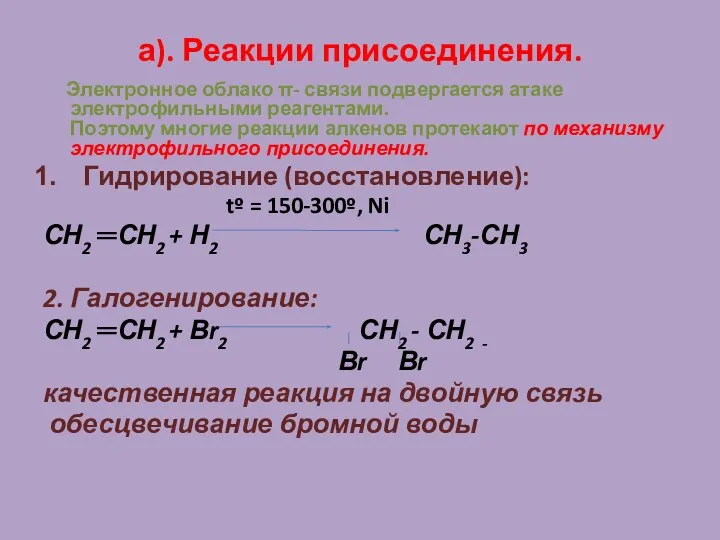
- 19. а). Реакции присоединения. Электронное облако π- связи подвергается атаке электрофильными реагентами. Поэтому многие реакции алкенов протекают
- 20. 3. Гидратация: СН2 ═СН2 + Н2 О Н+ СН3 - СН2 - ОН В реакциях несимметричных
- 21. 4. Гидрогалогенирование: СН2 ═ СН - СН3 + НСl СН2 - СН - СН3 Н Сl
- 23. б). Реакции окисления 1. Окисление алкенов в мягких условиях (щелочная или нейтральная среда, холод, окислитель –
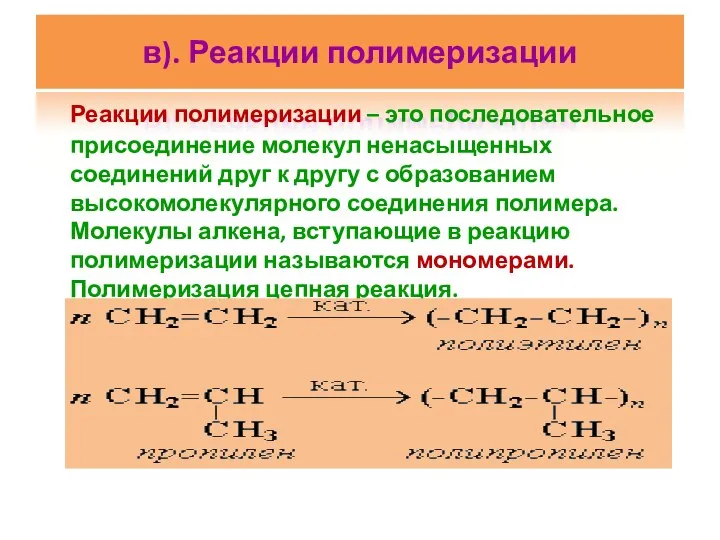
- 26. в). Реакции полимеризации Реакции полимеризации – это последовательное присоединение молекул ненасыщенных соединений друг к другу с
- 27. 5. Отдельные предствители 1.С2Н4 – этилен- газ со слабым чесночным запахом, горит, образуя копоть, мало растворим
- 28. 2.Пропен (пропилен) — вызывает наркоз (сильнее, чем этилен), оказывает общетоксическое и мутагенное действие. 3.Бутен-2 — вызывает
- 29. 4. Полиэтилен – получают полимеризацией этилена. Представляет собой бесцветный материал, имеющий низкую тепло- и электропроводность. Широко
- 31. Скачать презентацию


















 Бионеорганическая химия. Жидкие среды организма. (Лекция 2)
Бионеорганическая химия. Жидкие среды организма. (Лекция 2) Ароматичні речовини
Ароматичні речовини Коллигативные свойства растворов
Коллигативные свойства растворов Метаморфические горные породы
Метаморфические горные породы Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Chimie bioorganique
Chimie bioorganique Современные области применения изотопной продукции
Современные области применения изотопной продукции Дгебуадзе Загра Омардибировна, учитель химии, МОУ «СОШ № 14 г.Зеленокумска» Ставропольский край
Дгебуадзе Загра Омардибировна, учитель химии, МОУ «СОШ № 14 г.Зеленокумска» Ставропольский край  Хроматография. Классификации хроматографических методов
Хроматография. Классификации хроматографических методов Нуклеирующие добавки
Нуклеирующие добавки Газ тәрізді диэлектриктер. Пропан
Газ тәрізді диэлектриктер. Пропан Короткі відомості з історії хімії. Становлення хімії як науки
Короткі відомості з історії хімії. Становлення хімії як науки Массообменные процессы
Массообменные процессы Секреты химии. Проект Радуга
Секреты химии. Проект Радуга Галогены
Галогены Презентация по Химии "Гидролиз солей" - скачать смотреть бесплатно
Презентация по Химии "Гидролиз солей" - скачать смотреть бесплатно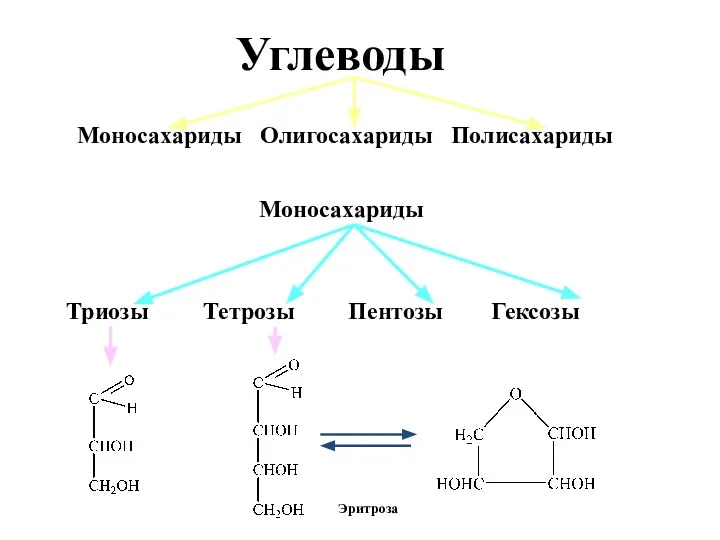 Углеводы. Моносахариды. Олигосахариды. Полисахариды
Углеводы. Моносахариды. Олигосахариды. Полисахариды Химия и сельское хозяйство
Химия и сельское хозяйство Изучение влияния азотсодержащих удобрений на качество продукции по содержанию нитратов
Изучение влияния азотсодержащих удобрений на качество продукции по содержанию нитратов Презентация по Химии "ВЛИЯНИЕ ГАЗИРОВАННЫХ НАПИТКОВ НА ОРГАНИЗМ ЧЕЛОВЕКА" - скачать смотреть
Презентация по Химии "ВЛИЯНИЕ ГАЗИРОВАННЫХ НАПИТКОВ НА ОРГАНИЗМ ЧЕЛОВЕКА" - скачать смотреть  Природные источники углеводородов и их переработка
Природные источники углеводородов и их переработка Уголь активированный
Уголь активированный Гетероциклические соединения
Гетероциклические соединения Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы
Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы Ферменты. Уравнение Михаэлиса-Ментен
Ферменты. Уравнение Михаэлиса-Ментен МЫЛО
МЫЛО Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений
Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений 2_Galogenovodorody
2_Galogenovodorody