Содержание
- 2. Білген сайын келеді біле бергің, біле беру емес пе тілегі елдің
- 3. Осы сабақ арқылы жүзеге асатын оқу мақсаттары - электрондық қабаттар және алғашқы 20 элементтердегі электрондардың орналасуын
- 4. Сабақтың мақсаты: Химия және физика курстарынан алған білімдерін пайдалана отырып , атомдағы электрондардың құрылысымен тереңірек таныстыру,
- 5. Атом-молекулалық ілімінің негізгі қағидалары: Атом-молекулалық ілімін жасаған орыс ғалымы Михаил Васильевич Ломоносов, VIII ғасыр. Барлық заттар
- 6. Элемент атомының қасиеттері: Атом радиусы-ядроның өзегінен сыртқы электронға дейінгі қашықтық. Иондану энергиясы-бейтарап атомнан бір электронды жұлып
- 8. Натрий атомының құрамы Хлор атомының құрамы
- 9. Оқытудың күтілетін нәтижелері Атомдағы электрондардың құрылысымен тереңірек танысады «электрон бұлты », «орбиталь», «энергетикалық деңгей», «энергетикалық деңгейше»,
- 10. Атом құрылысының бірінші кванттық теориясын Нильс Бор 1913 ж. ұсынған,кейіннен XX ғасырдың 20 – жылдарында Л.де
- 11. Атомның химиялық қасиеті – электрондық қабатының құрылысына тәуелді
- 12. Электрондар – микробөлшектер, олардың атомдағы қозғалысын кванттық механика зерттейді.Ол элементар бөлшектердің әрекеттесуі мен тәртібін қарастырады. Электронның
- 13. Электрондық бұлт Атомдағы электрондар қозғалысының траекториясы белгісіз,кванттық механикада ядро маңындағы кеңістікте электрондар болу ықтималдығын – электрондық
- 14. Электрон бұлты болатын кеңістікті орбиталь деп атаймыз. мөлшері жуық орбитальдардан электрондық қабаттар немесе энергетикалық деңгейлер қалыптасады.
- 15. Электрондық қабат деп– бір энергетикалық деңгейдегі электрондардың жиынтығын айтады. Орбитальдар бір- бірінен өздерінің энергиялары, пішіндері және
- 16. Энергетикалық деңгейде орналасқан электрон саны Егер n = 1 болса N = 2 n = 2
- 17. This is known as a 1s sublevel: That contains 1 orbital s orbital electron spinning clockwise
- 18. Energy level 2 s orbital p orbitals 2s sublevel 2p sublevel
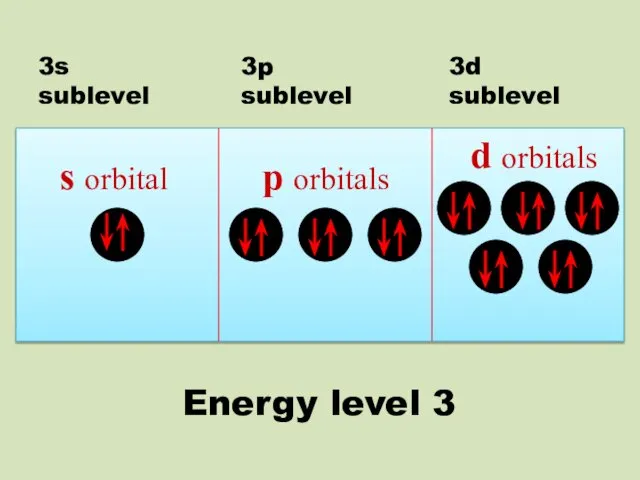
- 19. s orbital p orbitals d orbitals 3s sublevel 3p sublevel 3d sublevel Energy level 3
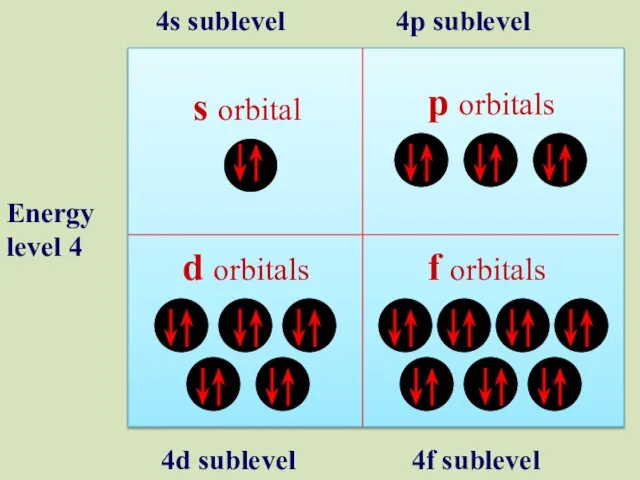
- 20. s orbital p orbitals d orbitals f orbitals Energy level 4 4s sublevel 4p sublevel 4d
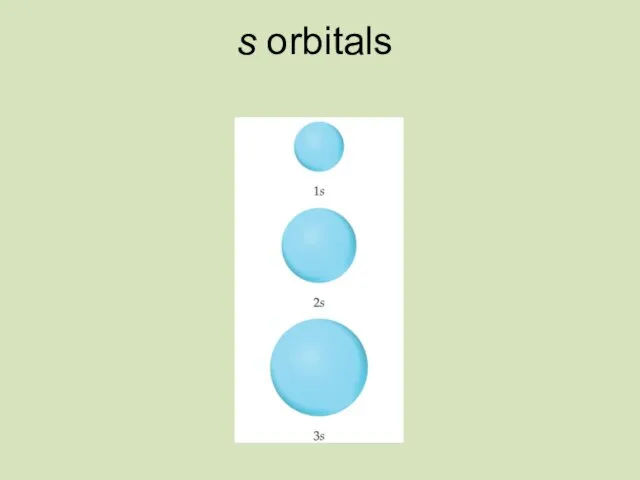
- 21. s orbitals
- 22. p orbitals
- 23. d orbitals
- 25. Электронның күйін 4 квант саны сипаттайды Бас квант саны – n электрондардың жалпы энергия қорын және
- 26. Бас квант сандары 1, 2 , 3, 4, 5, 6, 7; Энергетикалық деңгей K,L,M,N,O, P, Q
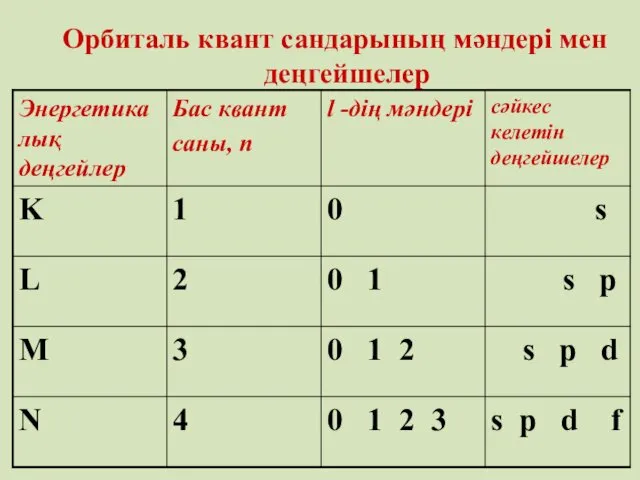
- 27. Орбиталь квант саны – l (қосымша квант саны) электронның энергетикалық күйін және орбитальдардың пішінін көрсетеді Қосымша
- 28. Орбиталь квант сандарының мәндері мен деңгейшелер
- 29. Магнит квант саны - ml пішіндері бірдей орбитальдардың кеңістікте орналасу бағытын көрсетеді. Магниттік квант саны орбиталь
- 30. Магнит квант сандарының мәндері
- 31. Спин квант саны – ms электронның өз осінен қай бағытта қозғалатынын көрсетеді.Электрон өз осінен сағат тілінің
- 32. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Hydrogen Electron Building (1 e -)
- 33. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Helium Electron Building (2 e -)
- 34. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Lithium Electron Building (3 e -)
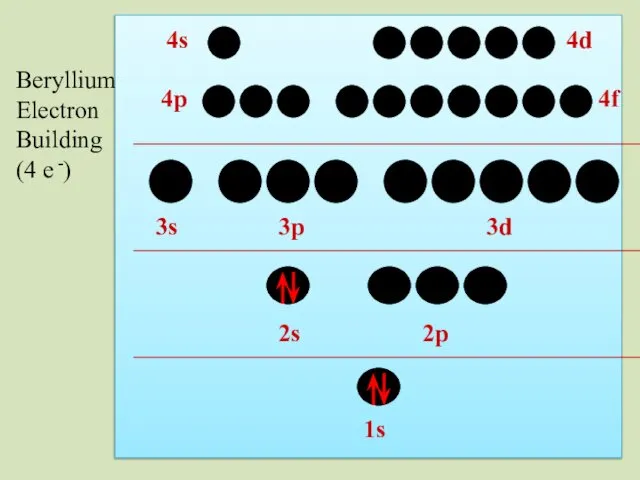
- 35. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Beryllium Electron Building (4 e -)
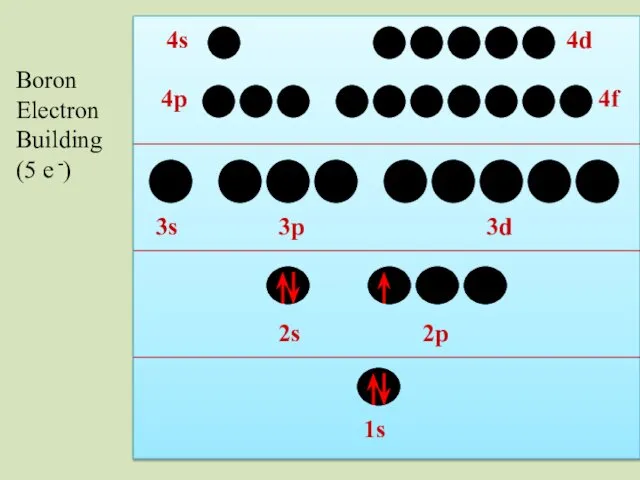
- 36. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Boron Electron Building (5 e -)
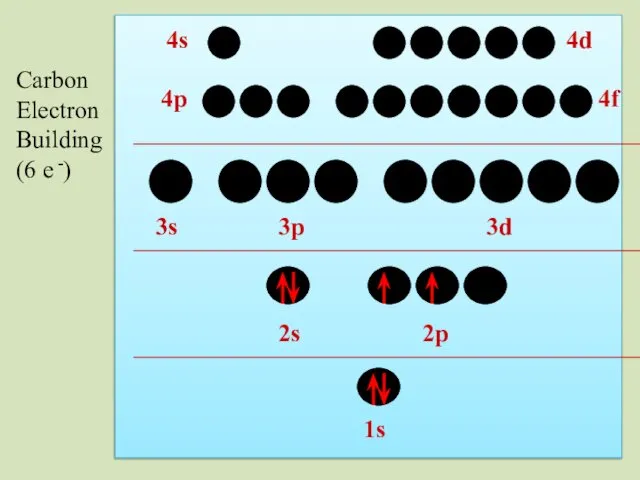
- 37. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Carbon Electron Building (6 e -)
- 38. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Nitrogen Electron Building (7 e -)
- 39. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Oxygen Electron Building (8 e -)
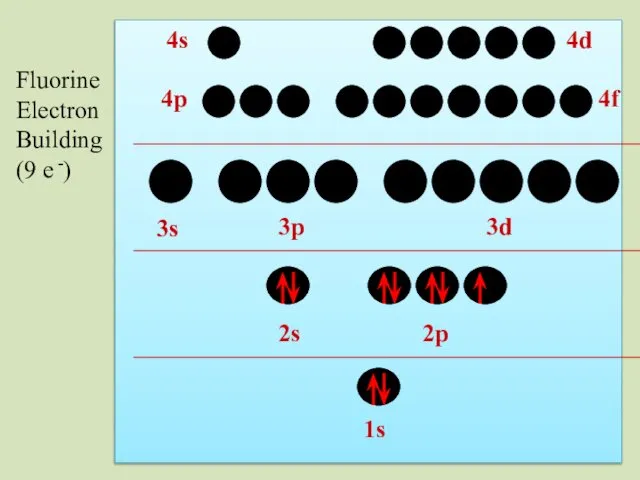
- 40. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Fluorine Electron Building (9 e -)
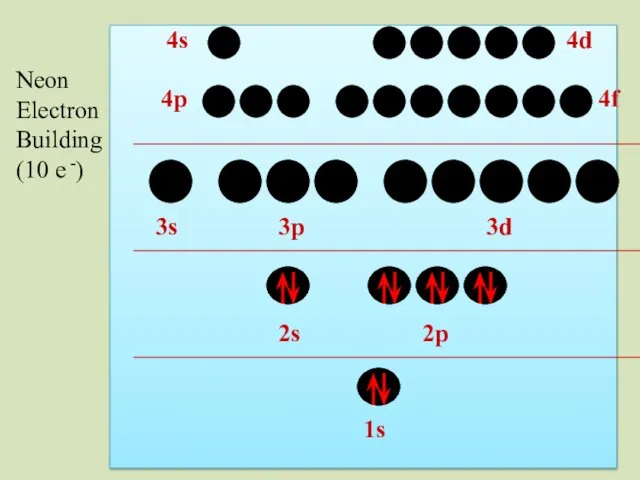
- 41. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Neon Electron Building (10 e -)
- 42. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f ?????? Electron Building (14 e -)
- 43. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Silicon Electron Building (14 e -)
- 44. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f ????? Electron Building (17 e -)
- 45. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f ????? Electron Building (17 e -)
- 46. 2s 1s 2p 3s 3p 3d 4p 4s 4d 4f Chlorine Electron Building (17 e -)
- 47. 1s 2s 2p 3s 3p 3d 4s Draw an electron filling diagram and the electron configuration
- 48. 1s 2s 2p 3s 3p 3d 4s Draw an electron filling diagram and the electron configuration
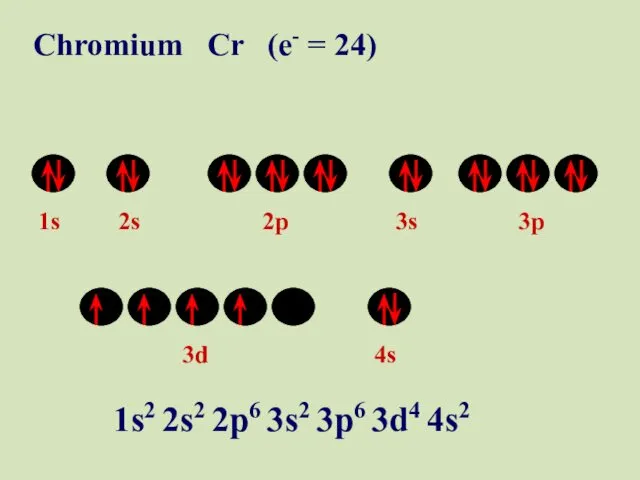
- 49. 1s 2s 2p 3s 3p 3d 4s Chromium Cr (e- = 24) 1s2 2s2 2p6 3s2
- 50. 1s 2s 2p 3s 3p 3d 4s Copper Cu (e- = 29) 1s2 2s2 2p6 3s2
- 51. 1s 2s 2p 3s 3p 3d 4s Copper Cu (e- = 29) 1s2 2s2 2p6 3s2
- 52. 1s 2s 2p Draw an electron filling diagram and the electron configuration for the ion O2-.
- 53. 1s 2s 2p Draw an electron filling diagram and the electron configuration for the ion Na+.
- 54. 1s 2s 2p 3s 3p Draw an electron filling diagram and the electron configuration for the
- 55. 1s 2s 2p 3s 3p 3d 4s Iron Fe (e- = 26) 1s2 2s2 2p6 3s2
- 56. 1s 2s 2p 3s 3p 3d 4s Iron II ion Fe2+ (e- = 24) 1s2 2s2
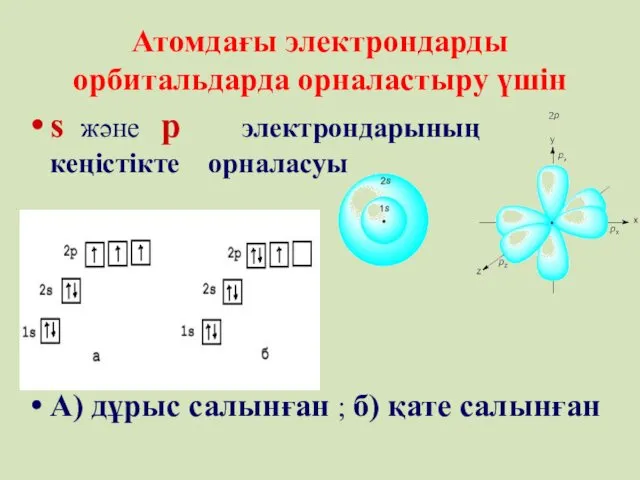
- 57. Атомдағы электрондарды орбитальдарда орналастыру үшін s және p электрондарының кеңістікте орналасуы А) дұрыс салынған ; б)
- 58. 1925ж Швейцария ғалымы В.Паули атомдардың спектрлерін зерттей келіп мынадай ереже немесе принцип ұсынды: атомда төрт квант
- 59. Хунд ережесі Бір деңгейшедегі орналасқан электрондардың спин квант сандарының қосындысы максималь болуы шарт; ол үшін электрондар
- 60. Бір орбитальда спиндері қарама –қарсы бағытталған екі электрон ғана орналасады мысалы: K (n=1) болғанда s (l=0)
- 61. Атомдағы электрондардың энергетикалық деңгейлер мен деңгейшелерде орналасуы Клечковскийдің ережелеріне бағынады
- 62. Атомның электрондары оның деңгейлері мен деңгейшелерінде бас және орбиталь квант сандарының қосындысының (n + l) өсу
- 63. Мысалы: 3d мен 4s орбитальдарындағы электрондар үшін 4s (4+0=4) және 3d (3+2=5) біле отырып, алғашқысының энергиясы
- 68. периодтық кестеде элемент орналасқан период нөмірі электрон орналасатын энергетикалық деңгей нөмірін және валенттілік электрондар орналасқан -
- 69. Атомдағы электрондардың деңгейлер мен деңгейшелер де орналасуы 1s 2s 2p 3s 3p 4s 3d 4p 5s
- 71. Тапсырма №1 Атомның электрондық формуласы берілген ол қай элементке сәйкес келеді: 1s2 2s2 2p6 3s2 3p6
- 72. Тапсырма № 2 Берілген электрондық конфигурацияның қайсысы үшінші периодтың екінші тобының элементіне сәйкес келеді: a) 1s2
- 73. Электрондық конфигурациясы... 3d5 4s1 болатын элемент a) Co; b) V; c) Cr; d)Mn; e)Fe; Мына электрондық
- 74. Октет ережесі - s- және p- элементтердің электрондарды қосып, беріп немесе жұптастыру нәтижесінде сыртқы энергетикалық қабатын
- 75. Үйге тапсырма: l = 0 орбитальдарының кеңістіктегі пішіні қандай және қалай аталады? l=1 орбитальдарының кеңістіктегі пішіні
- 77. Скачать презентацию































































 Термодинамика. Законы термодинамики
Термодинамика. Законы термодинамики Алкадиены. Диеновые углеводороды
Алкадиены. Диеновые углеводороды Растительные источники жиров и жирных масел
Растительные источники жиров и жирных масел Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства
Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства Діагностика за показами газоаналізатора. Типи газоаналізаторів
Діагностика за показами газоаналізатора. Типи газоаналізаторів Презентация по Химии "Сильнодіючі отруйні речовини: поняття та класифікація." - скачать смотреть бесплатно
Презентация по Химии "Сильнодіючі отруйні речовини: поняття та класифікація." - скачать смотреть бесплатно Природный каучук
Природный каучук Гранулирование. Виды грануляции
Гранулирование. Виды грануляции Метаморфогенные месторождения
Метаморфогенные месторождения Legătura chimică
Legătura chimică Total Syntheses of Trichorabdal A and Maoecrystal Z
Total Syntheses of Trichorabdal A and Maoecrystal Z Культивирование растительных и животных клеток
Культивирование растительных и животных клеток Оптические свойства дисперсных систем
Оптические свойства дисперсных систем Принципы создания полимерных конструкционных нанокомпозитов
Принципы создания полимерных конструкционных нанокомпозитов Жиры (9 класс)
Жиры (9 класс) Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс Химик-эколог
Химик-эколог Нафта
Нафта  Рубрифлордилатктон. Стратегия синтеза
Рубрифлордилатктон. Стратегия синтеза Синтез липидов
Синтез липидов Окислительные свойства концентрированной серной кислоты
Окислительные свойства концентрированной серной кислоты Тайна воды которую мы пьём
Тайна воды которую мы пьём Учитель химии МБОУ СОШ №79 г. о. Самара Язрикова Любовь Михайловна
Учитель химии МБОУ СОШ №79 г. о. Самара Язрикова Любовь Михайловна Автомобильные бензины и дизельные топлива. Характеристика и классификация автомобильных топлив
Автомобильные бензины и дизельные топлива. Характеристика и классификация автомобильных топлив Биоорганическая химия
Биоорганическая химия Соляная кислота и её соли
Соляная кислота и её соли Cromatografie de lichide de inalta performanta cuplata cu spectrometrie de masă
Cromatografie de lichide de inalta performanta cuplata cu spectrometrie de masă Полістирол. Визначення, фізичні властивості
Полістирол. Визначення, фізичні властивості