Содержание
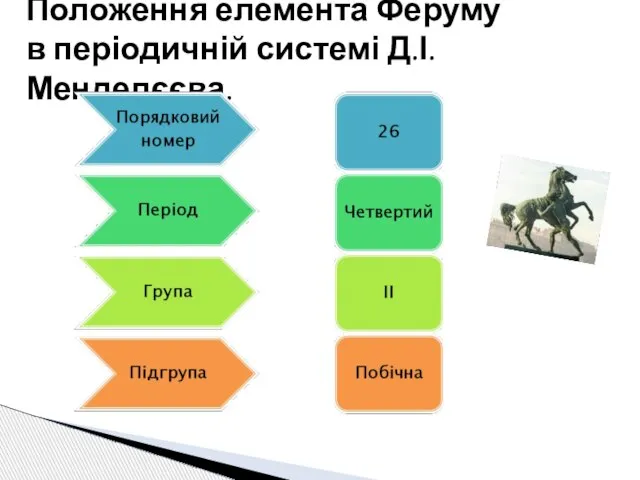
- 2. Положення елемента Феруму в періодичній системі Д.І. Менделєєва.
- 3. Дописати електронну формулу 1s2 2s2 2р6 3s2 3р6…. Будова атома Феруму
- 4. Які електрони для елементів головних підгруп являються валентними? А які електрони для елементів побічних підгруп являються
- 5. Валентні електрони атомів елементів побічних підгруп розприділяються на останньому і передостанньому рівнях. Запам’ятай!
- 6. Для Феруму характерні два основні ступені окиснення: +2, +3. Fe0 –2e = Fe+2 Fe0 –3e =
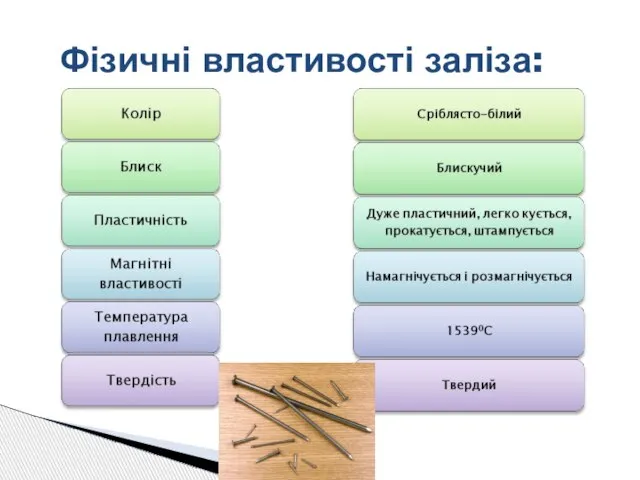
- 7. Фізичні властивості заліза:
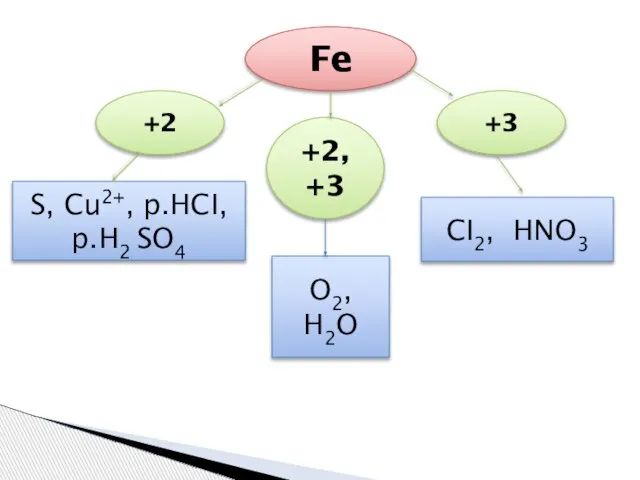
- 8. Fe +3 +2 +2, +3 O2, H2O CI2, HNO3 S, Cu2+, p.HCI, p.H2 SO4
- 9. Fe + CI2 = Fe + S = Fe + HCI = Fe + O2 =
- 10. Взаємодія з простими речовинами -неметалами 1) З киснем. 0 0 +2, +3 -2 +2 -2 +3
- 11. 0 0 +2 -2 Fe + S —>FeS електронний баланс Fe0 – 2e- —> Fe2+ S0
- 12. Хімічні властивості заліза Взаємодія з складними речовинами 1) З водою. +2, +3 3Fe0 + 4H2O —>
- 13. Метали Взаємодіють з кислотами коли: 1. Метал знаходиться в ряду активності металів до водню. 2. Повинні
- 14. 3) З солями. Дослід: здійснити реакцію між порошком заліза і розчином купрум (II) хлориду В якому
- 15. Метали Взаємодіють з розчинами солей коли: 1. Кожний метал витісняє із розчинів солей всі інші метали,
- 16. Сполуки Феруму :
- 17. +2 +2 FeO —>Fe(OH)2 Даний оксид проявляє основний характер. Які реакції підтверджують основний характер оксидів? +3
- 18. 1) 2FeCI2 + CI2 = 2FeCI3 2) FeCI3 + 3NaOH = Fe(OH)3 + 3NaCI 3) 4Fe(OH)2
- 19. На йони Fe2+ +2 +3 +2 FeCl2 + K3[Fe(CN)6] —> KFe[Fe(CN)6]+2KCL червона кровяна сіль синій осад
- 21. Скачать презентацию














![На йони Fe2+ +2 +3 +2 FeCl2 + K3[Fe(CN)6] —> KFe[Fe(CN)6]+2KCL](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/592307/slide-18.jpg)
 Стеклянные товары. Основные сырьевые материалы для производства стекла
Стеклянные товары. Основные сырьевые материалы для производства стекла Известные ученые и их открытия
Известные ученые и их открытия Определение активной реакции воды (рН)
Определение активной реакции воды (рН) Химический состав прямогонных бензинов
Химический состав прямогонных бензинов Physical chemistry of surface phenomena. Basics of adsorptive therapy
Physical chemistry of surface phenomena. Basics of adsorptive therapy Конструкционные материалы. Пластмассы
Конструкционные материалы. Пластмассы Истинная и средняя скорости реакции
Истинная и средняя скорости реакции  Буферные растворы. Буферная емкость
Буферные растворы. Буферная емкость Презентация по Химии "Алюміній" - скачать смотреть бесплатно
Презентация по Химии "Алюміній" - скачать смотреть бесплатно Сердечные гликозиды. Общая характеристика, методы выделения, анализ. (Тема 7)
Сердечные гликозиды. Общая характеристика, методы выделения, анализ. (Тема 7) лекарства Урок-защита проектов Разработала учитель химии МОУ «Гимназия №1» г. Саратова Шишкина И.Ю.
лекарства Урок-защита проектов Разработала учитель химии МОУ «Гимназия №1» г. Саратова Шишкина И.Ю. Круговорот воды в природе
Круговорот воды в природе Циклоалканы (полиметиленовые, циклопарафины, ациклические)
Циклоалканы (полиметиленовые, циклопарафины, ациклические) Количество вещества. Единица измерения вещества моль
Количество вещества. Единица измерения вещества моль Металлы в природе. Общие способы их получения.
Металлы в природе. Общие способы их получения. Введение в органическую химию
Введение в органическую химию Презентация по Химии "Закон збереження маси" - скачать смотреть
Презентация по Химии "Закон збереження маси" - скачать смотреть  Гетерогенный катализ
Гетерогенный катализ Спирты: получение, свойства и применение
Спирты: получение, свойства и применение Кислотность и основность органических соединений
Кислотность и основность органических соединений Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Задачи к экзамену по дисциплине «ИПР и ОП»
Задачи к экзамену по дисциплине «ИПР и ОП» Дисахариды, моносахариды
Дисахариды, моносахариды Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Тағамдық қоспалардың гигиеналық регламенттелуі
Тағамдық қоспалардың гигиеналық регламенттелуі Водородная связь
Водородная связь СЕРА Учитель химии МКОУ СОШ №3 с.Чикола РСО-Алания Кадохова А.Г.
СЕРА Учитель химии МКОУ СОШ №3 с.Чикола РСО-Алания Кадохова А.Г. Теоретические основы биоорганической химии
Теоретические основы биоорганической химии