Содержание
- 2. Вступ Вода - найпоширеніша на Землі речовина Майже 3 / 4 поверхні земної кулі покриті водою,
- 3. Хімічні властивості води Хімічні властивості води залежать від фізичної природи її атомів, а також способів їх
- 4. Фізичні властивості води Є також деякі фізичні властивості води, які йдуть врозріз з принципами таблиці Менделєєва.
- 6. Скачать презентацию
Слайд 2
Вступ
Вода - найпоширеніша на Землі речовина
Майже 3 / 4 поверхні
Вступ
Вода - найпоширеніша на Землі речовина
Майже 3 / 4 поверхні
земної кулі покриті водою, що утворює моря, океани, ріки, озера.
Вода має дуже велике значення у житті рослин, тварин, людини. Згідно з сучасними уявленнями, саме походження життя на пов’язується з морем. У всякому організмі вода є середовищем, в якому відбуваються хімічні процеси, що забезпечують життєдіяльність організму: крім того, вона сама бере участь у ряді біохімічних реакцій.
Вода має дуже велике значення у житті рослин, тварин, людини. Згідно з сучасними уявленнями, саме походження життя на пов’язується з морем. У всякому організмі вода є середовищем, в якому відбуваються хімічні процеси, що забезпечують життєдіяльність організму: крім того, вона сама бере участь у ряді біохімічних реакцій.
Слайд 3
Хімічні властивості води
Хімічні властивості води залежать від фізичної природи її атомів,
Хімічні властивості води
Хімічні властивості води залежать від фізичної природи її атомів,
а також способів їх об’єднання в молекулу і подальшої угруповання утворилися молекул. Так як вона постійно контактує з різними речовинами, вода є розчином з дуже складним складом. Більш того, вона проявляється себе як прекрасний розчинник, оскільки вона здатна розчинити і рідини, і тверді тіла, і гази.
Особливо добре властивості такого розчинника проявляють себе в морській воді, так як вона може розчинити практично всі речовини. Приблизно сімдесят елементів періодичної системи можна виявити в її складі. У морській та океанській воді можна виявити навіть рідкі радіоактивні елементи. Найбільш часто зустрічаються речовини в складі води – це хлор, натрій, сірка, калій, магній, кальцій, стронцій, бром, вуглець і бор.
На сьогоднішній день дослідники розкривають все більш складні і тонкі механізми організації водної маси . Її вважають найбільш важким з’єднанням зі всіх речовин, відомих фізикам і хімікам. За хімічним складом вода може і не відрізнятися, але при цьому вона матиме різний вплив на організм людини, так як формувалася вона в певних умовах.
Хімічні властивості води також залежать про її молекулярної структури. Зокрема, молекула води складається з трьох атомів, які сформовані у вигляді рівнобедреного трикутника. У його вершині знаходиться атом кисню, тоді як в основі лежать два атоми водню. При цьому валентний кут з’єднання НОН дорівнює 104,31 °.
Особливо добре властивості такого розчинника проявляють себе в морській воді, так як вона може розчинити практично всі речовини. Приблизно сімдесят елементів періодичної системи можна виявити в її складі. У морській та океанській воді можна виявити навіть рідкі радіоактивні елементи. Найбільш часто зустрічаються речовини в складі води – це хлор, натрій, сірка, калій, магній, кальцій, стронцій, бром, вуглець і бор.
На сьогоднішній день дослідники розкривають все більш складні і тонкі механізми організації водної маси . Її вважають найбільш важким з’єднанням зі всіх речовин, відомих фізикам і хімікам. За хімічним складом вода може і не відрізнятися, але при цьому вона матиме різний вплив на організм людини, так як формувалася вона в певних умовах.
Хімічні властивості води також залежать про її молекулярної структури. Зокрема, молекула води складається з трьох атомів, які сформовані у вигляді рівнобедреного трикутника. У його вершині знаходиться атом кисню, тоді як в основі лежать два атоми водню. При цьому валентний кут з’єднання НОН дорівнює 104,31 °.
Слайд 4
Фізичні властивості води
Є також деякі фізичні властивості води, які йдуть врозріз
Фізичні властивості води
Є також деякі фізичні властивості води, які йдуть врозріз
з принципами таблиці Менделєєва. Зокрема, найбільш високими характеристиками у води є ті, які по суті своїй мають бути набагато нижче. Це стосується температури замерзання і кипіння, теплоти плавлення і пароутворення.
Температура замерзання і кипіння у гідридних елементів кисневої підгрупи по мірі полегшення з’єднання знижується. Якби така закономірність діяла на воду, то вона закипала б при глибоко негативному температурному значенні, при -70 ° С, а замерзала би при -90 ° С. Це, в свою чергу, спровокувало б відсутність води на Землі, так як вона не змогла б міститися ні в рідкому, ні в твердому стані. Єдино можливий варіант – це газоподібний стан.
Відносно теплоти пароутворення можна сказати, що для випаровування води, нагрітої до 100 ° С, необхідно в 6 разів більше тепла, ніж для нагріву аналогічної маси води до 80 ° С.
З кожною хвилиною мільйон тон води в гідросфері випаровується від сонячного тепла. У результаті такого впливу в атмосфері постійно міститься величезна кількість теплоти, яке еквівалентно тому, що виробили б 40 000 найпотужніших електростанцій.
Температура замерзання і кипіння у гідридних елементів кисневої підгрупи по мірі полегшення з’єднання знижується. Якби така закономірність діяла на воду, то вона закипала б при глибоко негативному температурному значенні, при -70 ° С, а замерзала би при -90 ° С. Це, в свою чергу, спровокувало б відсутність води на Землі, так як вона не змогла б міститися ні в рідкому, ні в твердому стані. Єдино можливий варіант – це газоподібний стан.
Відносно теплоти пароутворення можна сказати, що для випаровування води, нагрітої до 100 ° С, необхідно в 6 разів більше тепла, ніж для нагріву аналогічної маси води до 80 ° С.
З кожною хвилиною мільйон тон води в гідросфері випаровується від сонячного тепла. У результаті такого впливу в атмосфері постійно міститься величезна кількість теплоти, яке еквівалентно тому, що виробили б 40 000 найпотужніших електростанцій.



 Подготовлено ученицей 9 "А" класса Михневской СОШ Темновой Яной.
Подготовлено ученицей 9 "А" класса Михневской СОШ Темновой Яной. Аттестационная работа. Методическая разработка занятия клуба Я – исследователь по теме Волшебное вещество ‒ соль
Аттестационная работа. Методическая разработка занятия клуба Я – исследователь по теме Волшебное вещество ‒ соль Презентация по теме «Полисахариды. Крахмал и целлюлоза» Автор: Пономарева О.Ю. учитель химии МОУ «Куртамышская СОШ № 2» 2009г
Презентация по теме «Полисахариды. Крахмал и целлюлоза» Автор: Пономарева О.Ю. учитель химии МОУ «Куртамышская СОШ № 2» 2009г № 16. Аминокислоты
№ 16. Аминокислоты  <Сера как химический элемент и простое вещество> Цель: сформировать представление о аллотропии серы, её физических и химиче
<Сера как химический элемент и простое вещество> Цель: сформировать представление о аллотропии серы, её физических и химиче Химия актиноидов
Химия актиноидов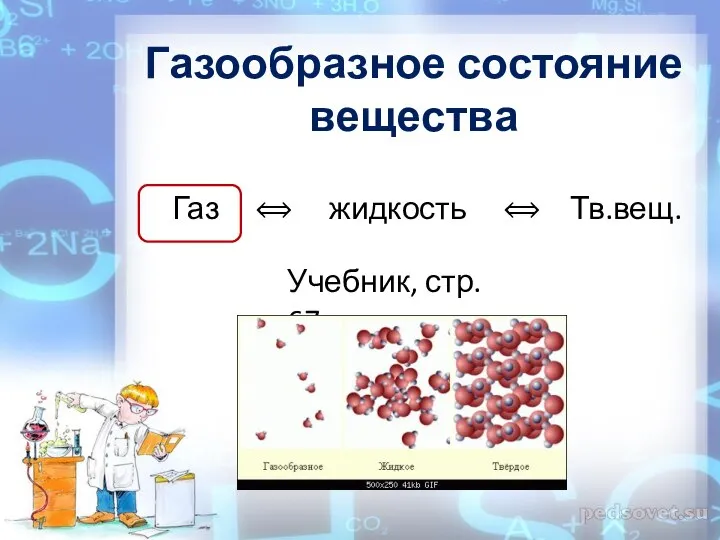 Газообразное состояние вещества
Газообразное состояние вещества Знаки химических элементов. Тренажер
Знаки химических элементов. Тренажер Исследование физико-химических и биологических свойств КФпокрытий, сформированных методом ВЧМР
Исследование физико-химических и биологических свойств КФпокрытий, сформированных методом ВЧМР Контроль процесса эмульсионной сополимеризацин дивинила со стиролом
Контроль процесса эмульсионной сополимеризацин дивинила со стиролом Оксиды и гидроксиды щелочных металлов
Оксиды и гидроксиды щелочных металлов Биополимерлер және олардың құрылымдық құрам бөліктері
Биополимерлер және олардың құрылымдық құрам бөліктері Насыщенные (предельные) углеводороды. Алканы (парафины)
Насыщенные (предельные) углеводороды. Алканы (парафины) Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу
Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу Химические свойства металлов Урок химии в 11 классе
Химические свойства металлов Урок химии в 11 классе Топливо и топливосжигающие устройства. Горение топлива
Топливо и топливосжигающие устройства. Горение топлива Physical chemistry of nanostructured systems.( lecture no. 7)
Physical chemistry of nanostructured systems.( lecture no. 7) Основы химического равновесия
Основы химического равновесия Вода. Физические и химические свойства
Вода. Физические и химические свойства Карбоновые кислоты
Карбоновые кислоты Кремний и его родственники
Кремний и его родственники …Е121…Е123..Е216…Е217…Е240… Пищевые добавки- полезные, вкусные и запрещённые Московских Анастасия 9 А класс МОУ СОШ № 27 города Бело
…Е121…Е123..Е216…Е217…Е240… Пищевые добавки- полезные, вкусные и запрещённые Московских Анастасия 9 А класс МОУ СОШ № 27 города Бело Гидролиз
Гидролиз Презентация по Химии "Скло Будівельний матеріал" - скачать смотреть бесплатно
Презентация по Химии "Скло Будівельний матеріал" - скачать смотреть бесплатно Галогены
Галогены Презентация по Химии "Задания на соответствие" - скачать смотреть
Презентация по Химии "Задания на соответствие" - скачать смотреть  Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии
Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии Химическое равновесие
Химическое равновесие