Содержание
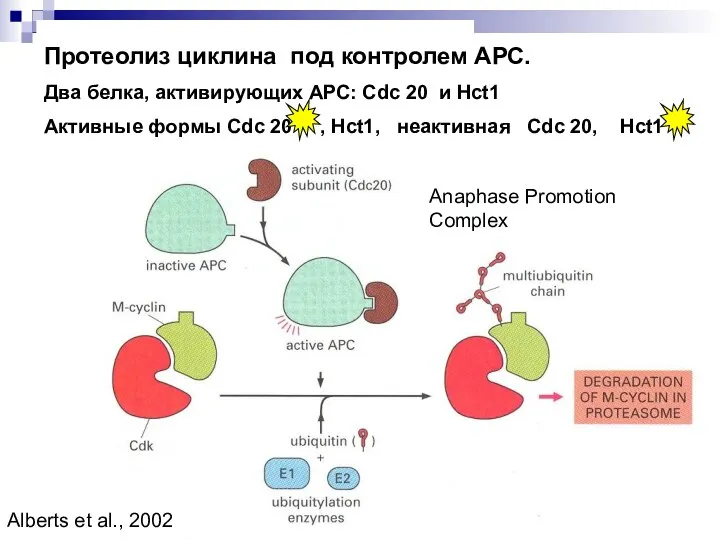
- 2. Протеолиз циклина под контролем АРС. Два белка, активирующих АРС: Cdc 20 и Hct1 Активные формы Cdc
- 3. Cdc20-APC и аналог Hct1-APC – деградация циклина. M-Cdk активирует Cdc20-APC M-Cdk инактивирует Hct1-APC фосфорилированием Hct1-APC активируется
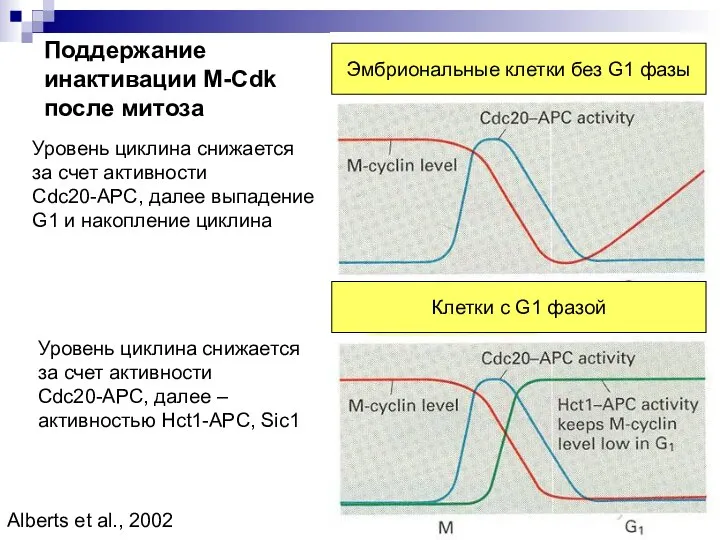
- 4. Поддержание инактивации M-Cdk после митоза Уровень циклина снижается за счет активности Cdc20-APC, далее выпадение G1 и
- 5. Изучение перехода G1-S у S.cerevisia Мутации, связанные с арестом клеточного цикла, получили в реакции на α-фактор
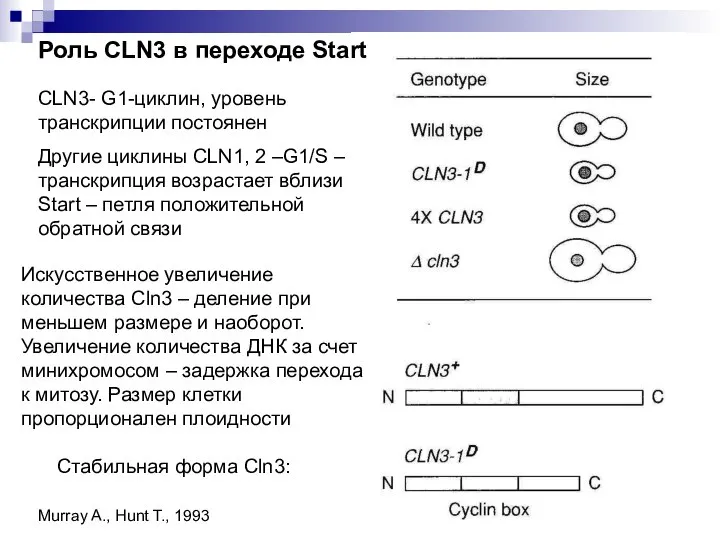
- 6. Роль CLN3 в переходе Start CLN3- G1-циклин, уровень транскрипции постоянен Другие циклины CLN1, 2 –G1/S –
- 7. Гипотетическая модель координации роста клетки и движения по клеточному циклу у дрожжей Белки, cвязывающие Cln3 G1-циклин
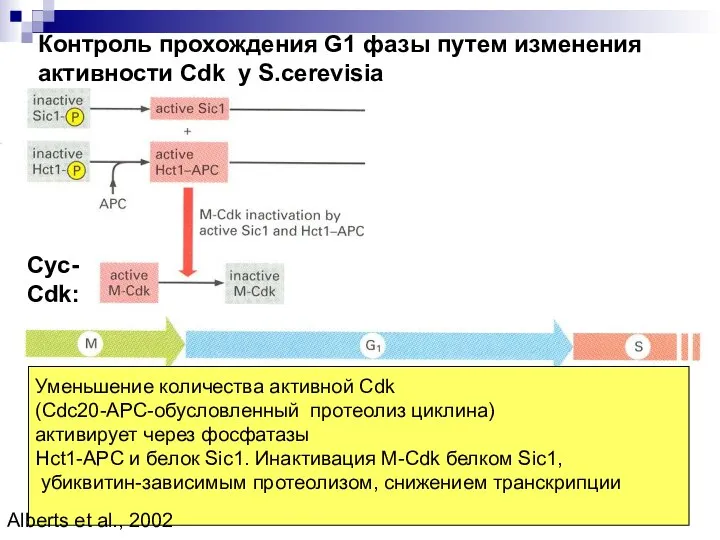
- 8. Контроль прохождения G1 фазы путем изменения активности Cdk у S.cerevisia Уменьшение количества активной Cdk (Cdc20-APC-обусловленный протеолиз
- 9. Контроль прохождения G1 фазы путем изменения активности Cdk у S.cerevisia Аккумуляция G1-циклина (Cln3): на него не
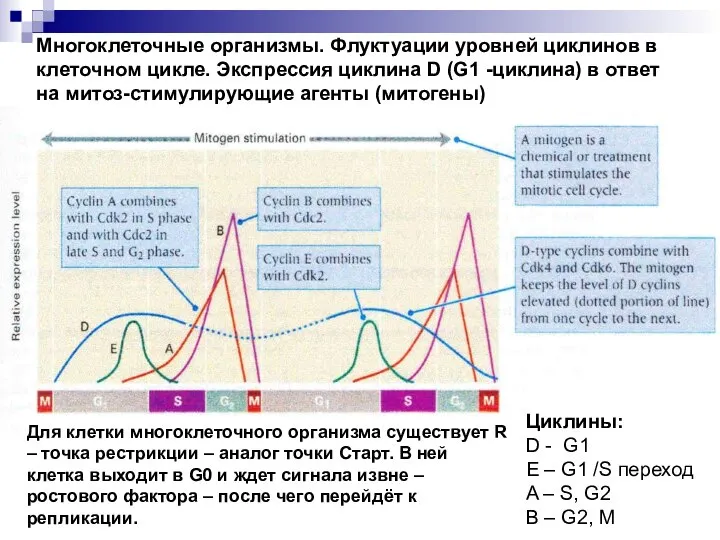
- 10. Многоклеточные организмы. Флуктуации уровней циклинов в клеточном цикле. Экспрессия циклина D (G1 -циклина) в ответ на
- 11. Роль Rb белка в контроле перехода G1-S у многоклеточных Rb -белок ретинобластомы инактивирует фактор транскрипции E2F
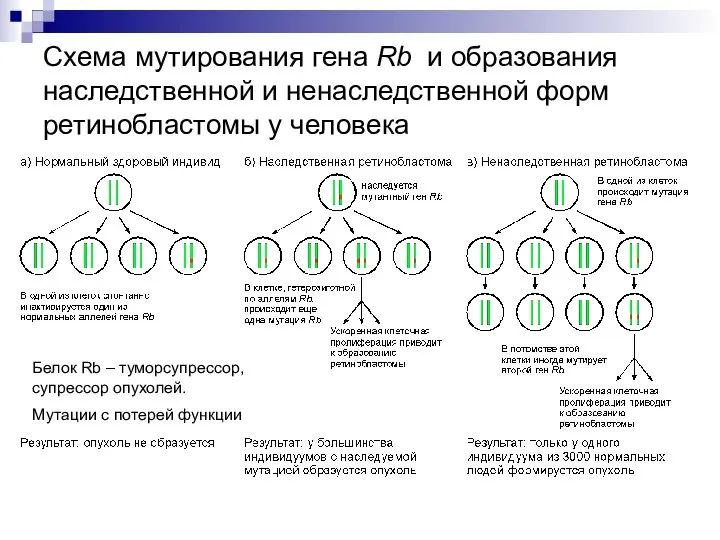
- 12. Схема мутирования гена Rb и образования наследственной и ненаследственной форм ретинобластомы у человека Белок Rb –
- 13. Инициация репликации ДНК у S.cerevisiae Основные участники ОRС-origin recognition complex (6 белков: orc1-orc6)-прикреплен к ori в
- 14. Компоненты организации репликации ORC комплекс из 6 белков Cdc7 CDK Cdc6- нестабилен у дрожжей(Т1/2=5 мин), появляется
- 15. Предотвращение повторной репликации S-Cdk: -запускает репликацию ДНК -фосфорилирует Сdc6, он отделяется от ОRС- предотвращение репликации с
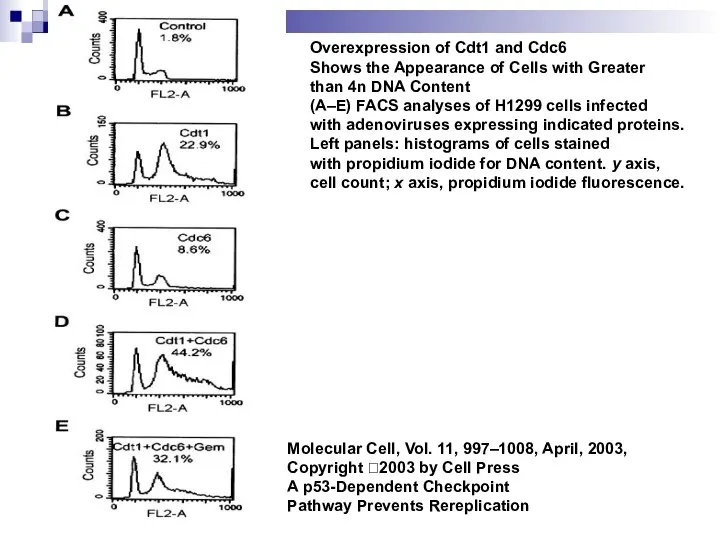
- 16. Molecular Cell, Vol. 11, 997–1008, April, 2003, Copyright 2003 by Cell Press A p53-Dependent Checkpoint Pathway
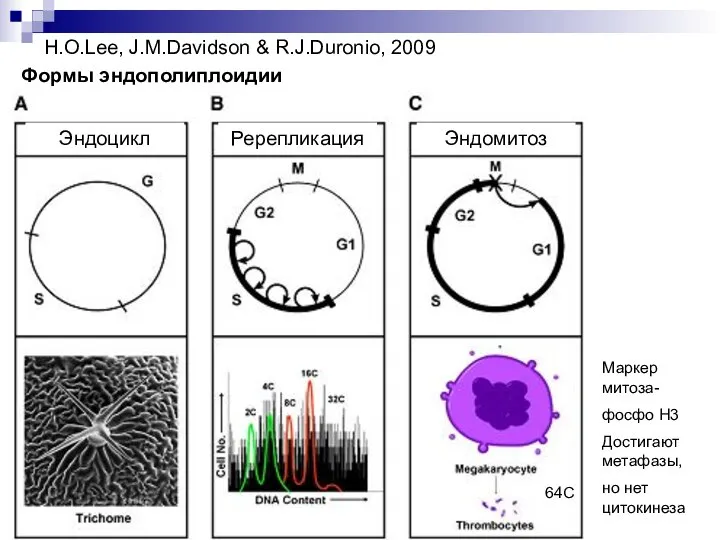
- 17. H.O.Lee, J.M.Davidson & R.J.Duronio, 2009 Формы эндополиплоидии Эндоцикл Ререпликация Эндомитоз 64С Маркер митоза- фосфо Н3 Достигают
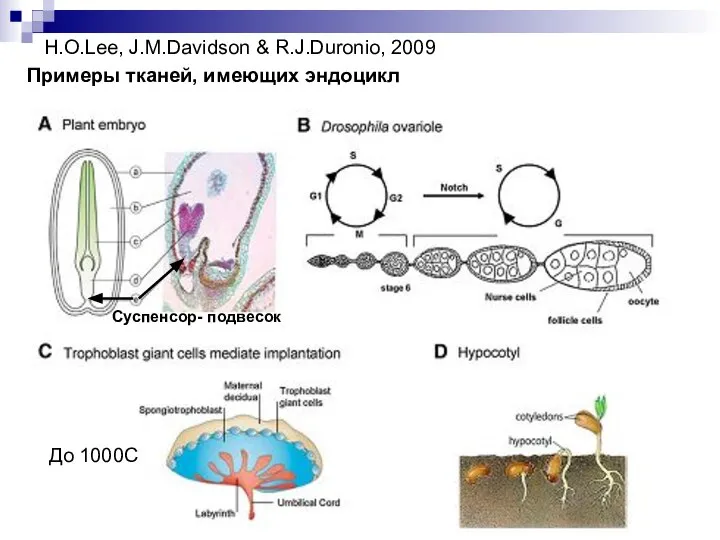
- 18. H.O.Lee, J.M.Davidson & R.J.Duronio, 2009 Примеры тканей, имеющих эндоцикл До 1000С Суспенсор- подвесок
- 19. Фолликулярные клетки, окружающие ооцит: митозы, эндоциклы, амплификация. Полиплоидизируются (до 16 С), потом амплифицируют гены белков хориона:
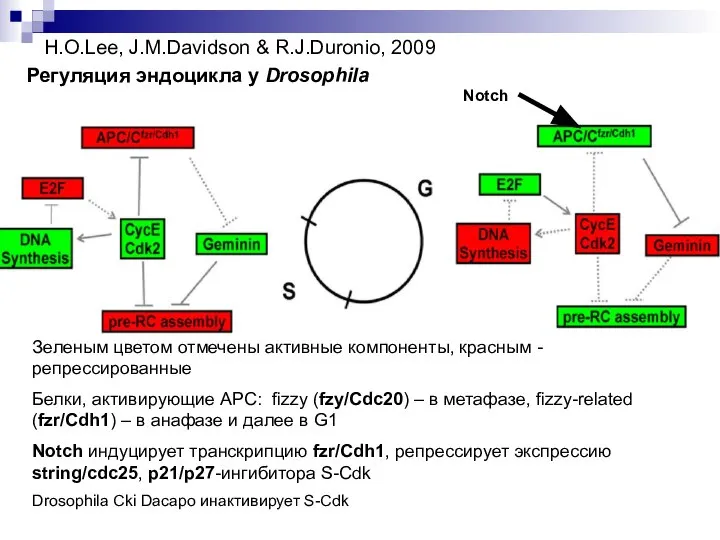
- 20. H.O.Lee, J.M.Davidson & R.J.Duronio, 2009 Регуляция эндоцикла у Drosophila Зеленым цветом отмечены активные компоненты, красным -
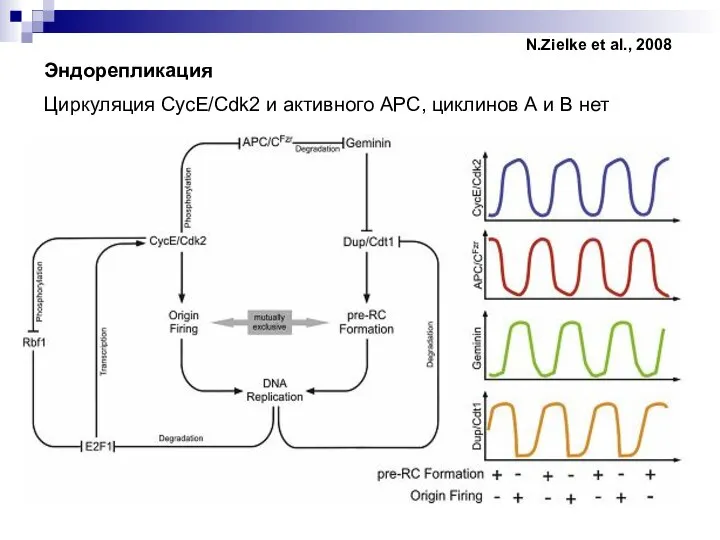
- 21. Эндорепликация Циркуляция CycE/Cdk2 и активного APC, циклинов А и В нет N.Zielke et al., 2008
- 22. S.Y.Park & M.Asano, 2008 Orc1 необходим для пролиферации. A,B,C- включение BdU в нервные ганглии личинок, wt-
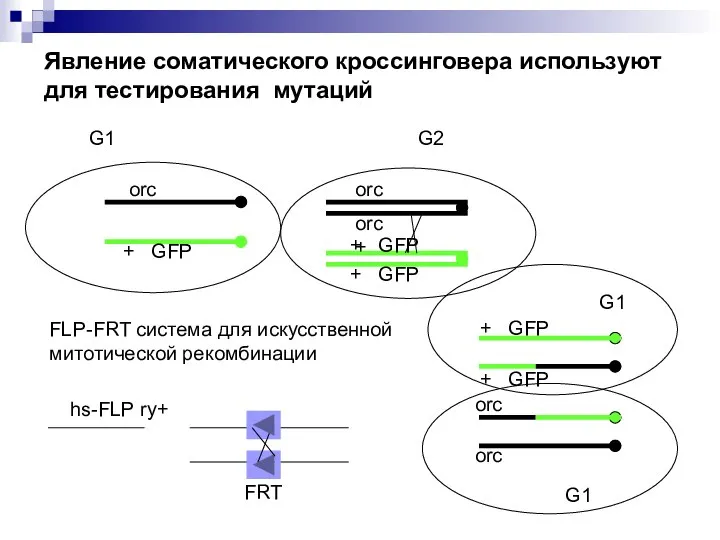
- 23. + GFP orc G1 G2 orc orc + + GFP + GFP G1 G1 Явление соматического
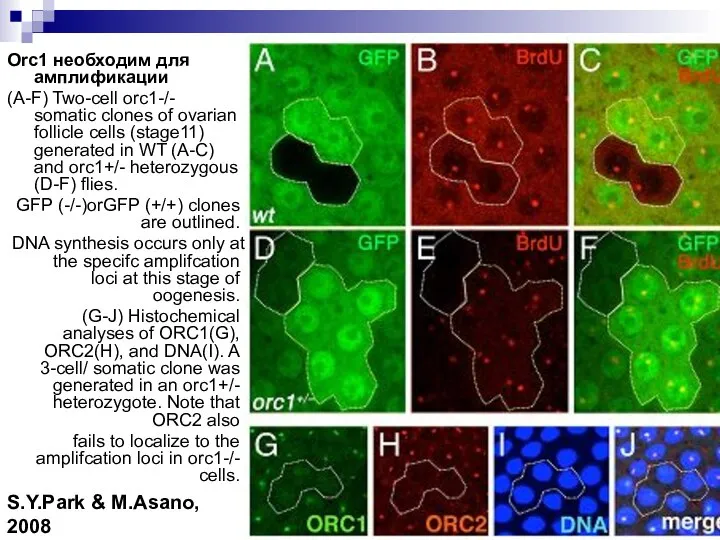
- 24. Orc1 необходим для амплификации (A-F) Two-cell orc1-/- somatic сlones of ovarian follicle cells (stage11) generated in
- 25. S.Y.Park & M.Asano, 2008 Для эндорепликации не нужны белки orc1, 2, вероятно, существуют другие, которые их
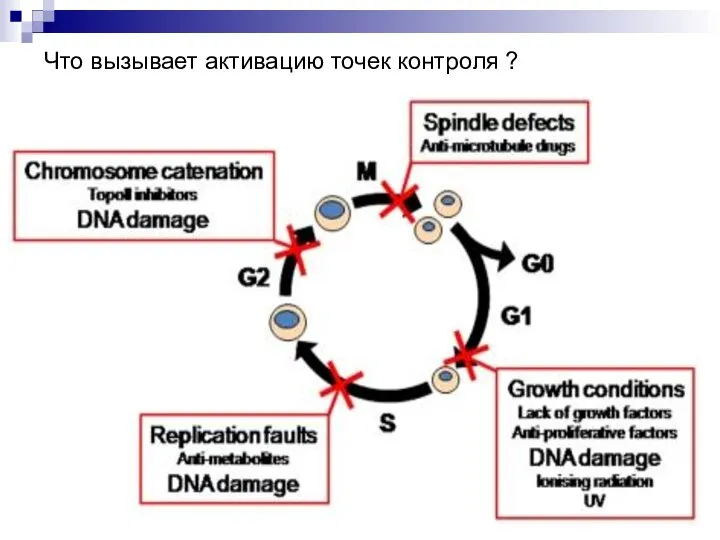
- 27. Что вызывает активацию точек контроля ?
- 28. Какие структуры работают в точах контроля ?
- 29. Изучение точек контроля у дрожжей: Получение условных мутагенчувствительных мутаций Обработка слабой дозой радиации (мутации rad) веществами,
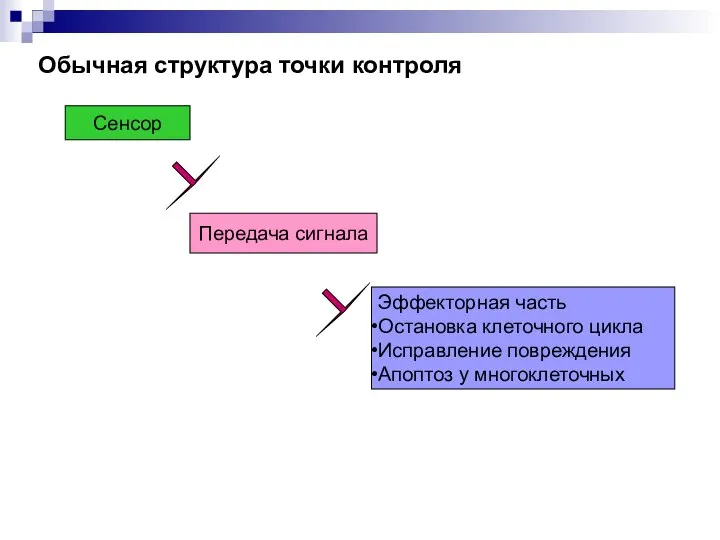
- 30. Обычная структура точки контроля Сенсор Передача сигнала Эффекторная часть Остановка клеточного цикла Исправление повреждения Апоптоз у
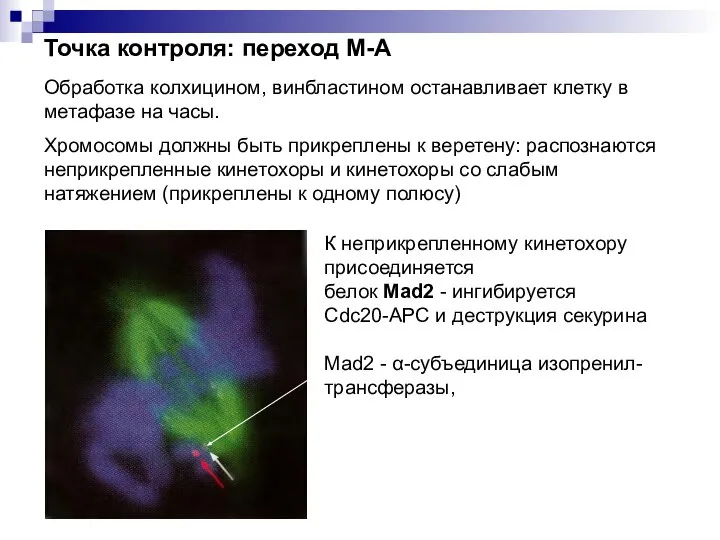
- 31. Обработка колхицином, винбластином останавливает клетку в метафазе на часы. Хромосомы должны быть прикреплены к веретену: распознаются
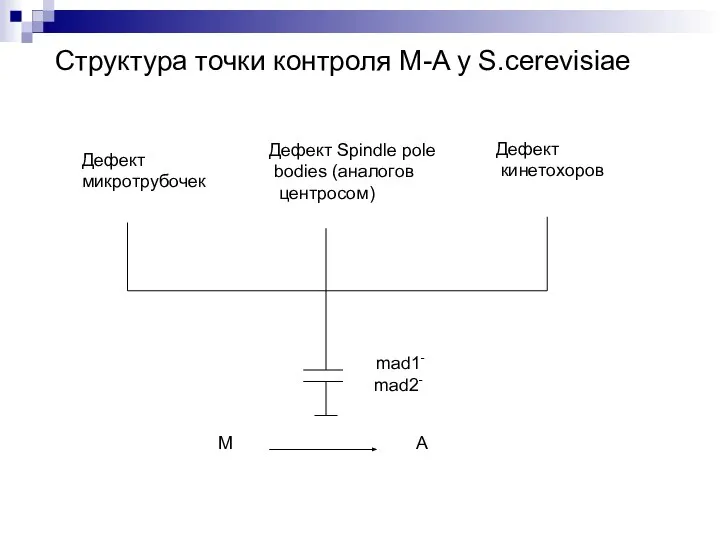
- 32. Точки контроля клеточного цикла. Переход М-А -дефект веретена -дефект полюсов (в т.ч. нереплицированная центросома) -дефект кинетохоров
- 33. Дефект микротрубочек Дефект Spindle pole bodies (аналогов центросом) Дефект кинетохоров М А mad1- mad2- Структура точки
- 34. Участие белков СРС- chromosomal passenger complex в точке контроля М-А Vagnarelli P., Earnshaw W., 2004 Mitotic
- 35. СРС- chromosomal passenger complex INCENP в клетках He LA. Метафазы с нарушением построения хромосом. Яркий сигнал
- 36. Роль СРС в точке контроля веретена Дестабилизация и новое прикрепление кинетохора Сигнализация о нарушении, остановка деления
- 41. СРС- chromosomal passenger complex Survivin – член семейства IAP (Inhibitor of Apoptosis) Присоединяет СРС к кинетохору,
- 42. Точка контроля клеточного цикла. G1 G1 контроль повреждения ДНК. Поврежденная ДНК – активация р53 – CKI
- 43. Точки контроля клеточного цикла у дрожжей. G2 G1-S G2-M или конец S. Контроль завершения репликации. Распознаются
- 44. Структура точки контроля G2-M Murray A., Hunt T., 1993
- 45. Болезнь «атаксия телангиэктазия»- синдром Луи-Бара – дефект одной из протеинкиназ, фосфорилирующих р53 в ответ на облучение
- 46. Cенсоры поврежденной ДНК L.Zou, D.Liu and S.J.Elledge, 2003 Rad9=*PCNA Rad17-RFC Двунитевые разрывы Однонитевые разрывы
- 47. Mdm2 Mdm2 p53 p53 p53 P P ДНК γ-лучи Деградация в протеосоме Стабильный активный р53 ATМ/ATR-киназы
- 48. RPA – ATR - амплификация сигнала ATRIP Передача сигнала: Активация Chk 1, 2 киназ Эффекторная часть:
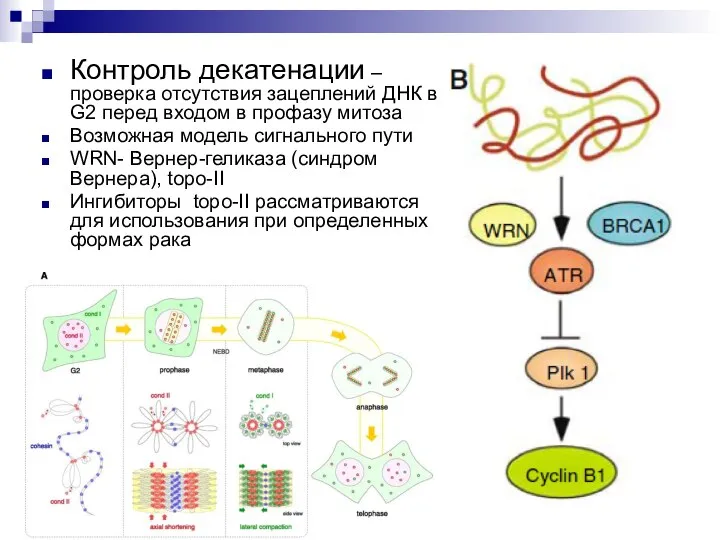
- 49. Контроль декатенации – проверка отсутствия зацеплений ДНК в G2 перед входом в профазу митоза Возможная модель
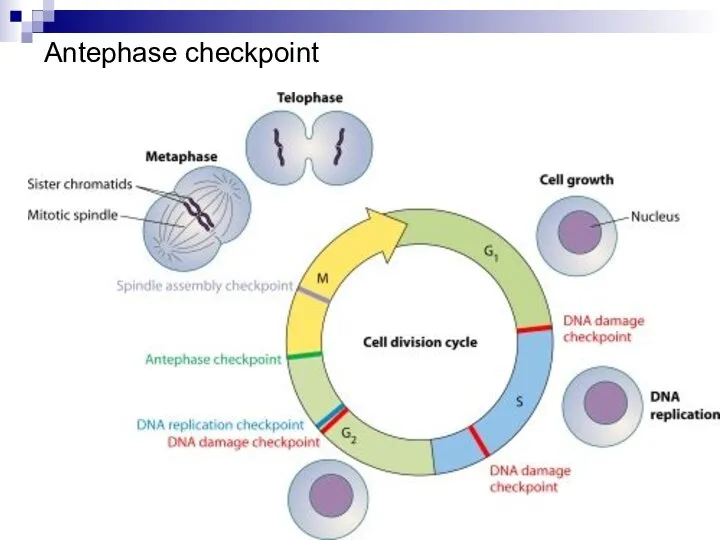
- 50. Antephase checkpoint. Точка контроля в Антефазе отлична от контроля декатенации. Клетки откладывают вступление в профазу митоза
- 51. Antephase checkpoint
- 52. Antephase checkpoint
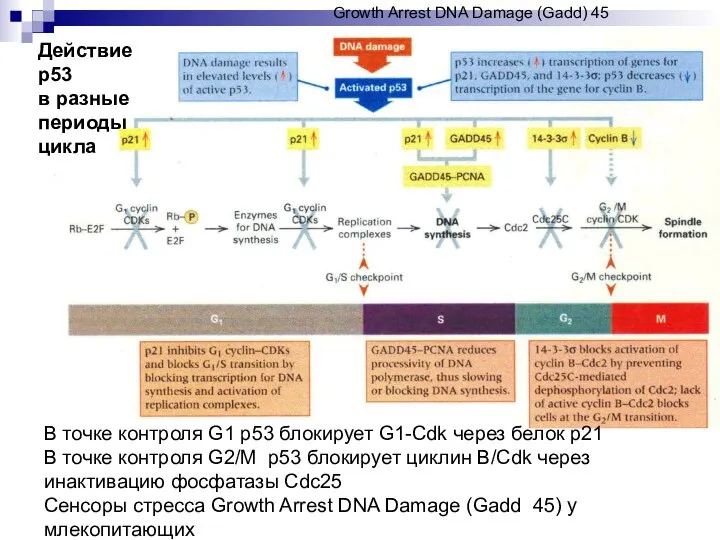
- 53. В точке контроля G1 р53 блокирует G1-Cdk через белок р21 В точке контроля G2/М р53 блокирует
- 54. Белки GADD в ответе клетки на генотоксический стресс IR ионизирующая UV (MMS) радиация метилметан сульфонат P53
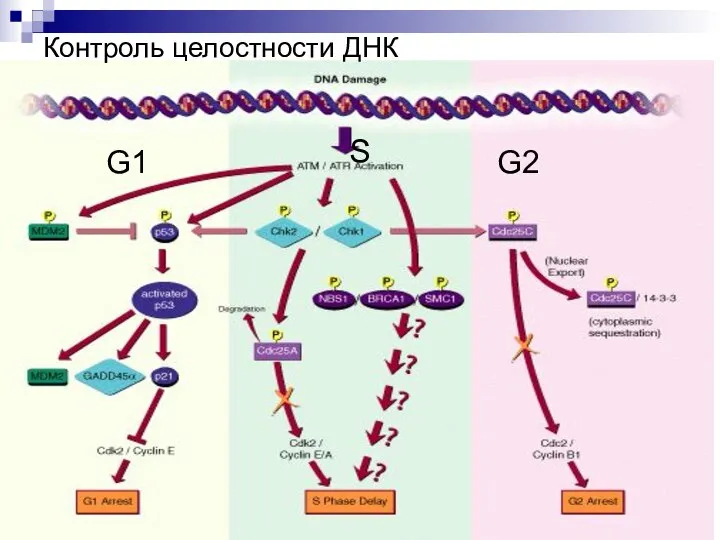
- 55. Контроль целостности ДНК G1 S G2
- 57. Скачать презентацию

































 Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.
Генетика. Лекция 5 Генотип. Геном. Кариотип. Геномные мутации. Генный баланс. Компенсация доз генов. Эволюция генома.  Мыс. Мыс көзі
Мыс. Мыс көзі Какое свойство кожуры апельсина помогает держать его на поверхности воды
Какое свойство кожуры апельсина помогает держать его на поверхности воды Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Порфирины. Производные порфина. (Лекция 14)
Порфирины. Производные порфина. (Лекция 14) Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна
Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна  Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура
Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура Презентация по Химии "Химическая связь" - скачать смотреть бесплатно
Презентация по Химии "Химическая связь" - скачать смотреть бесплатно Хімічні методи підвищення продуктивності свердловини
Хімічні методи підвищення продуктивності свердловини Введение. Теория строения органических соединений А.М.Бутлерова. Лекция 1-2
Введение. Теория строения органических соединений А.М.Бутлерова. Лекция 1-2 Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Простые вещества - металлы
Простые вещества - металлы Дисперсная система
Дисперсная система Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Анодные реакции коррозионного процесса
Анодные реакции коррозионного процесса Химия и биохимия игристых вин
Химия и биохимия игристых вин Истрия развития химии
Истрия развития химии Группа нефелиновых сиенитов-фонолитов
Группа нефелиновых сиенитов-фонолитов Производные пиррозилидина. (Лекция 6)
Производные пиррозилидина. (Лекция 6) Введение в экологическую токсикологию
Введение в экологическую токсикологию Физическая и коллоидная химия
Физическая и коллоидная химия Геология полезных ископаемых
Геология полезных ископаемых Среднее (полное) общее образование. Химия. Изучение химии на профильном уровне
Среднее (полное) общее образование. Химия. Изучение химии на профильном уровне Предельные углеводороды
Предельные углеводороды Гліцерин. Загальні відомості про гліцерин
Гліцерин. Загальні відомості про гліцерин Определение валентности элементов
Определение валентности элементов Лужноземельні елементи. Фізичні та хімічні властивості простих речовин та сполук, що вони утворюють
Лужноземельні елементи. Фізичні та хімічні властивості простих речовин та сполук, що вони утворюють Подготовила воспитанница 11 «А» класса Кулишова Валерия
Подготовила воспитанница 11 «А» класса Кулишова Валерия