Содержание
- 2. СТРОЕНИЕ АТОМА ХИМИЧЕСКАЯ СВЯЗЬ
- 3. Студент должен: Знать: Положения теории химической связи, виды и механизмы ее образования Уметь: Определять виды связей
- 4. Учение о химической связи составляет основу всей теоретической химии. Фундаментальной основой химической связи явилась теория химического
- 5. К основным чертам химической связи можно отнести: а) снижение общей энергии двух- или многоатомной системы по
- 6. Различают четыре типа химических связей: ионную, ковалентную, металлическую и водородную. Правило октета. В результате образования химической
- 7. Ионная химическая связь-это связь, образовавшаяся за счет электростатического притяжения катионов к анионам. Как вы знаете, наиболее
- 8. Атомы, присоединившие «чужие» электроны, превращаются в отрицательные ионы, или анионы. Атомы, отдавшие свои электроны, превращаются в
- 9. → Схема образования ионной связи во фториде натрия:
- 10. Два разноименно заряженных иона, связанные силами притяжения, не теряют способности взаимодействовать с противоположно заряженными ионами, вследствие
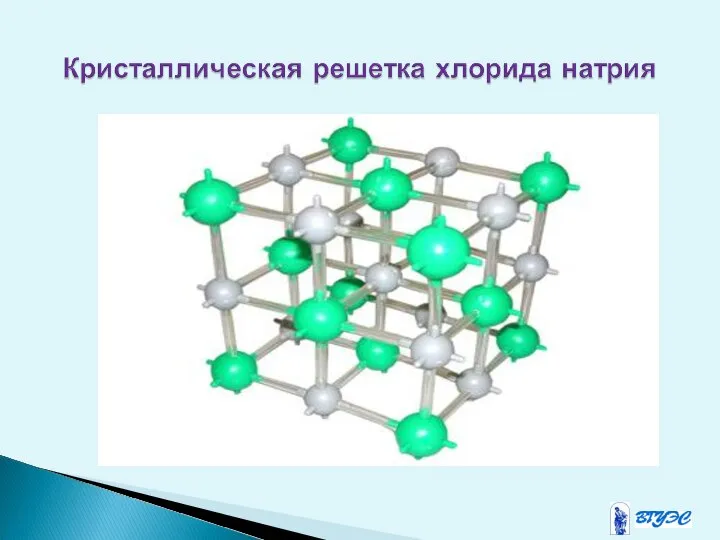
- 11. В ионном соединении ионы представлены как бы в виде электрических зарядов со сферической симметрией электрического поля
- 13. Ионная связь существует также в солях аммония, где нет атомов металлов (их роль играет катион аммония
- 14. Ковалентная химическая связь-это связь, возникающая между атомами за счет образования общих электронных пар. В основе ее
- 15. Обменный механизм действует, когда атомы образуют общие электронные пары за счет объединения неспаренных электронов. Например: 1)
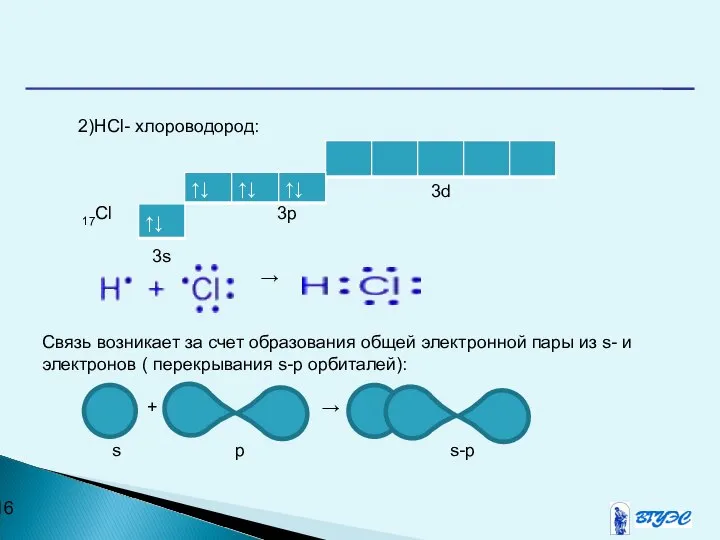
- 16. 2)HCl- хлороводород: 3d 17Cl 3p 3s → Связь возникает за счет образования общей электронной пары из
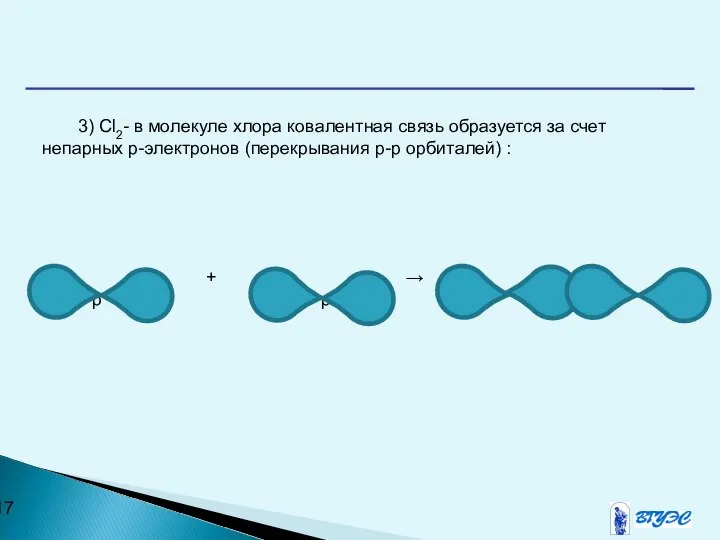
- 17. 3) Cl2- в молекуле хлора ковалентная связь образуется за счет непарных р-электронов (перекрывания р-р орбиталей) :
- 18. 4)N2- в молекуле азота между атомами образуются три общие электронные пары: 7N 2p 2s →
- 19. Донорно-акцепторный механизм образования ковалентной связи рассмотрим на классическом примере образования иона аммония : → Донор имеет
- 20. Ковалентные связи классифицируют не только по механизму образования общих электронных пар, соединяющих атомы, но и по
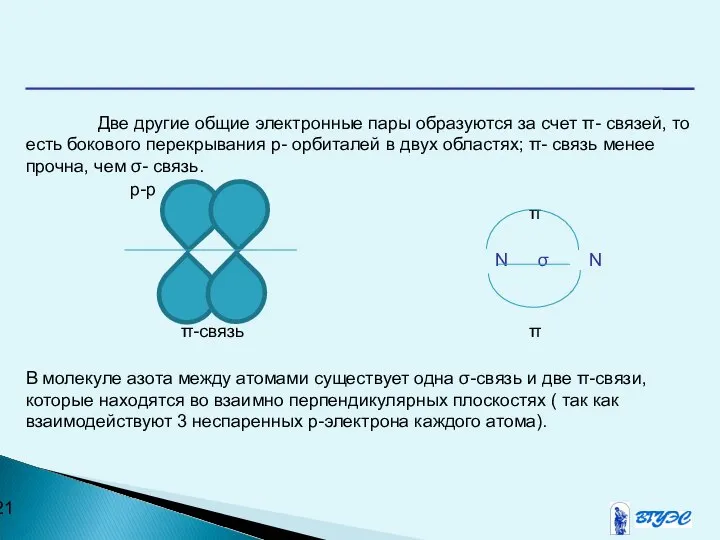
- 21. Две другие общие электронные пары образуются за счет π- связей, то есть бокового перекрывания р- орбиталей
- 22. Следовательно, σ-связи могут образовываться за счет перекрывания электронных орбиталей: s-s (H2) s-p (HCl) p-p (Cl2), а
- 23. 2)двойные: СО2 C2H4 О═С═О H2C═CH2 оксид углерода (IV) этилен По степени смещенности общих электронных пар к
- 24. Например: или N2 то есть посредством ковалентной неполярной связи образованы молекулы простых веществ-неметаллов. Значения относительной электроотрицвтельности
- 25. Азот- более электроотрицательный элемент, чем водород, поэтому общие электронные пары смещаются к его атому. H→ N
- 26. полярными, а молекула не будет полярной, так как имеет линейное строение. Молекула воды Н2О полярна, так
- 27. молекулярной- в обычных условиях это газы, легколетучие жидкости и твердые, но легкоплавкие или возгоняющиеся вещества (Cl2,
- 28. Связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической
- 29. Наличием металлической связи обусловлены физические свойства металлов и сплавов: твердость, электрическая проводимость и теплопроводность, ковкость, пластичность,
- 30. Химическую связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно поляризованными атомами
- 31. При наличии такой связи даже низкомолекулярные вещества могут быть при обычных условиях жидкостями (спирт, вода) или
- 32. При этом действует принцип комплиментарности, то есть эти связи образуются между определенными парами, состоящими из пуринового
- 33. Деление химических связей на типы носит условный характер, так как все они характеризуются определенным единством. Ионную
- 34. В ряду галогеноводородов HF-HCL-HBr-HI-HAt степень полярности связи уменьшается , ибо уменьшается разность в значениях электроотрицательности атомов
- 35. 3)В солях аммония, метиламмония и т.д.-между атомами азота и водорода- ковалентная полярная, а между ионами аммония
- 36. Причиной единства всех типов и видов химических связей служит их одинаковая физическая природа- электронно-ядерное взаимодействие. Образование
- 38. Скачать презентацию































 Изотопы. История открытия. Изотопы водорода
Изотопы. История открытия. Изотопы водорода Кислород и оксиген
Кислород и оксиген Пробоподготовка (HPLC, instrumental analysis)
Пробоподготовка (HPLC, instrumental analysis) Простые вещества. Аллотропия. Классификация простых веществ. Бинарные соединения. Оксиды
Простые вещества. Аллотропия. Классификация простых веществ. Бинарные соединения. Оксиды Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева
Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева Алкадиены. Виды диенов
Алкадиены. Виды диенов Строительное материаловедение. (Лекции 1-2)
Строительное материаловедение. (Лекции 1-2) Презентация по Химии "Алгоритм решения задач" - скачать смотреть
Презентация по Химии "Алгоритм решения задач" - скачать смотреть  Электрохимические методы анализа
Электрохимические методы анализа Теоретическая электрохимия, часть 1
Теоретическая электрохимия, часть 1 Ископаемое сырье органической химии
Ископаемое сырье органической химии Кислотно-основное титрование
Кислотно-основное титрование Стратегия успеха 2 (ЕГЭ). Органическая химия
Стратегия успеха 2 (ЕГЭ). Органическая химия Зависимость свойств химических элементов от положения в ПСХЭ
Зависимость свойств химических элементов от положения в ПСХЭ Дисперсные наполнители. Пневмогидрокомпрессионное формование. Магнитоимпульсное формование
Дисперсные наполнители. Пневмогидрокомпрессионное формование. Магнитоимпульсное формование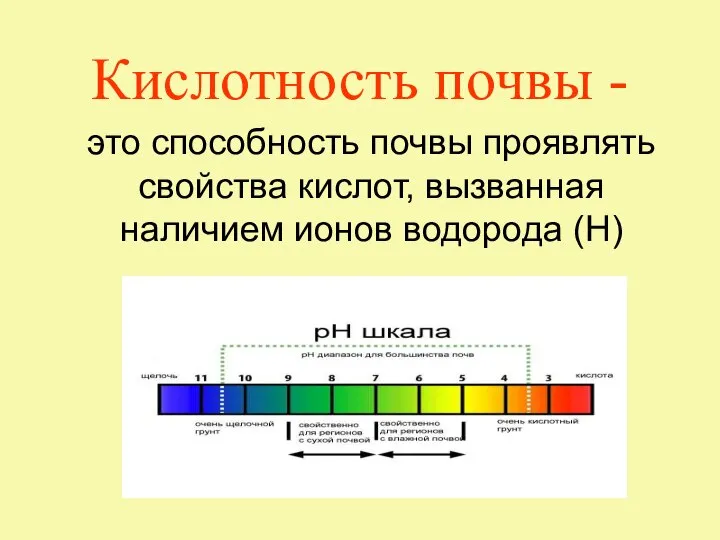 Кислотность почвы
Кислотность почвы Химические свойства, получение и применение крахмала
Химические свойства, получение и применение крахмала Биохимия, как наука
Биохимия, как наука Значение органической химии в жизни человека
Значение органической химии в жизни человека Противоаллергические средства
Противоаллергические средства Презентация по Химии "Викторина для любителей и знатков химии" - скачать смотреть
Презентация по Химии "Викторина для любителей и знатков химии" - скачать смотреть  Светоносный элемент
Светоносный элемент Дмитрий Иванович Менделеев и его периодический закон
Дмитрий Иванович Менделеев и его периодический закон Ионы. Определение кислотности раствора
Ионы. Определение кислотности раствора Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности
Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности Строение и физические свойства металлов
Строение и физические свойства металлов Классификация металлов в соответствии с ионным потенциалом и параметром мягкости
Классификация металлов в соответствии с ионным потенциалом и параметром мягкости Реакции ионного обмена
Реакции ионного обмена