Содержание
- 2. Цели лекции: Обучающая - Сформировать знания о кислотных и основных свойствах органических соединений. Развивающая – Расширить
- 3. Теория электролитической диссоциации Аррениуса (1890г.) Сванте-Август Аррениус Согласно теории Аррениуса кислотами являются электролиты, при диссоциации которых
- 4. Протолитическая (протонная) теория Бренстеда-Лоури Для оценки кислотных и основных свойств органических соединений наибольшее значение имеют две
- 5. Протолитическая (протонная) теория Бренстеда-Лоури I. Кислотность и основность по Бренстеду-Лоури Кислота – химическая частица (молекула, ион),
- 6. Протолитическая (протонная) теория Бренстеда-Лоури Реакцию между кислотой и основанием в общем виде можно представить: Кислота А-Н
- 7. Протолитическая (протонная) теория Бренстеда-Лоури Например: Сильной кислоте HCl будет соответствовать слабое сопряженное основание Cl-, а слабой
- 8. Протолитическая (протонная) теория Бренстеда-Лоури Большинство органических соединений можно рассматривать как потенциальные кислоты, поскольку в них содержатся
- 9. Протолитическая (протонная) теория Бренстеда-Лоури В зависимости от природы кислотного центра различают: OH-кислоты (карбоновые кислоты, фенолы, спирты).
- 10. Протолитическая (протонная) теория Бренстеда-Лоури Количественно сила кислот-протолитов характеризуется вероятностью переноса протона от кислоты к воде как
- 11. Протолитическая (протонная) теория Бренстеда-Лоури Условно кислоты делят на "сильные" pKa
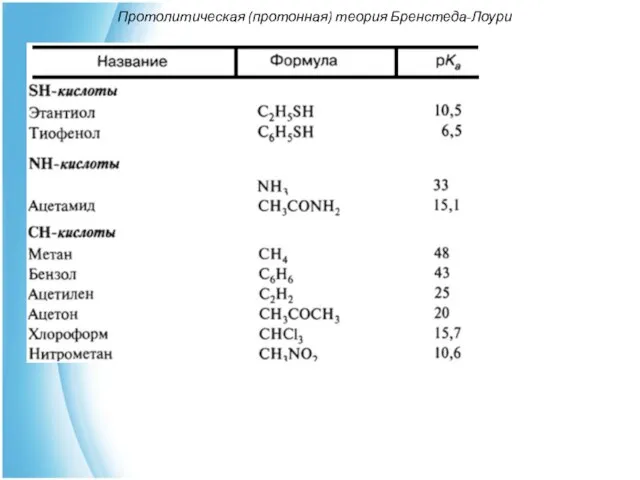
- 12. Протолитическая (протонная) теория Бренстеда-Лоури
- 13. Протолитическая (протонная) теория Бренстеда-Лоури
- 14. Протолитическая (протонная) теория Бренстеда-Лоури
- 15. Протолитическая (протонная) теория Бренстеда-Лоури Факторы, влияющие на кислотность Сила кислоты определяется стабильностью аниона, образовавшегося при диссоциации
- 16. Протолитическая (протонная) теория Бренстеда-Лоури 1)Природа атома в кислотном центре (электроотрицательность и поляризуемость). Чем больше электроотрицательность и
- 17. Протолитическая (протонная) теория Бренстеда-Лоури Электроотрицательность O>N>C, поэтому OH- кислота всегда сильнее, чем NH-кислота, а NH- кислота
- 18. Протолитическая (протонная) теория Бренстеда-Лоури На электроотрицательность атома углерода влияет состояние его гибридизации: С(sp) > С(sp2) >
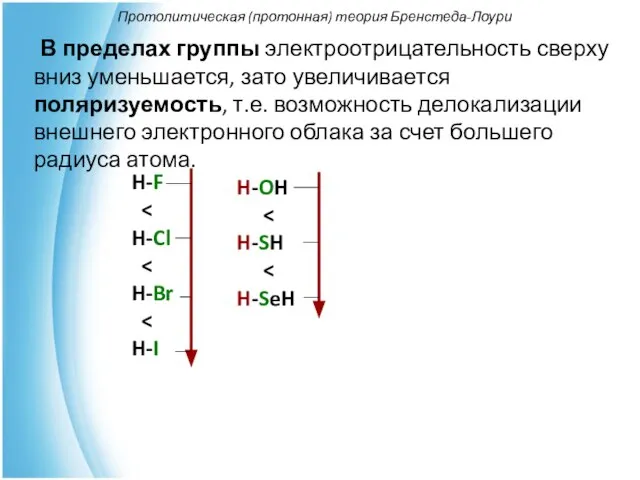
- 19. Протолитическая (протонная) теория Бренстеда-Лоури В пределах группы электроотрицательность сверху вниз уменьшается, зато увеличивается поляризуемость, т.е. возможность
- 20. Протолитическая (протонная) теория Бренстеда-Лоури Сравним, например, кислотность этанола (С2H5OH) и этантиола (С2H5SH). Атом серы S-H кислотного
- 21. Протолитическая (протонная) теория Бренстеда-Лоури Таким образом, в зависимости от природы кислотного центра органические кислоты с одинаковыми
- 22. Протолитическая (протонная) теория Бренстеда-Лоури 2) Стабилизация аниона за счет сопряжения: Сравним, например, кислотность алифатических спиртов, фенолов,
- 23. Протолитическая (протонная) теория Бренстеда-Лоури
- 24. Протолитическая (протонная) теория Бренстеда-Лоури Повышенная по сравнению с фенолами кислотность карбоновых кислот обусловлена стабилизацией ацилат –
- 25. Протолитическая (протонная) теория Бренстеда-Лоури 3) Влияние электронных эффектов заместителей, связанных с кислотным центром. Электроноакцепторные заместители способствуют
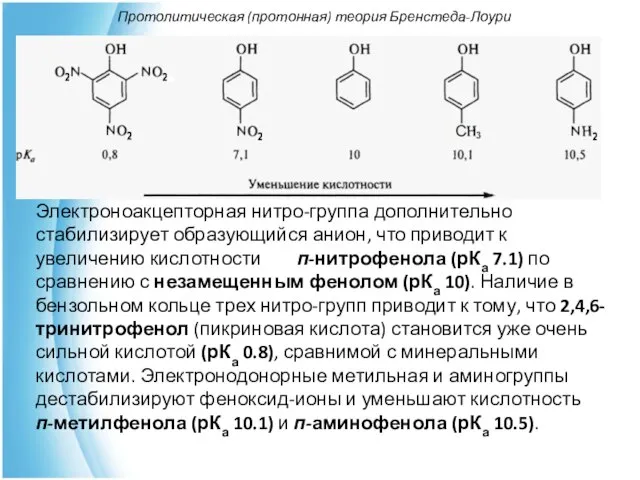
- 26. Протолитическая (протонная) теория Бренстеда-Лоури Электроноакцепторная нитро-группа дополнительно стабилизирует образующийся анион, что приводит к увеличению кислотности п-нитрофенола
- 27. Протолитическая (протонная) теория Бренстеда-Лоури Последовательное введение в молекулу нескольких электроноакцепторных заместителей повышает ее кислотность, например:
- 28. Протолитическая (протонная) теория Бренстеда-Лоури 4) Эффект сольватации. В водных растворах анионы гидратированы, что повышает их стабильность
- 29. Протолитическая (протонная) теория Бренстеда-Лоури Формиат-ион HCOO- за счет малого размера более гидратирован и стабилен по сравнению
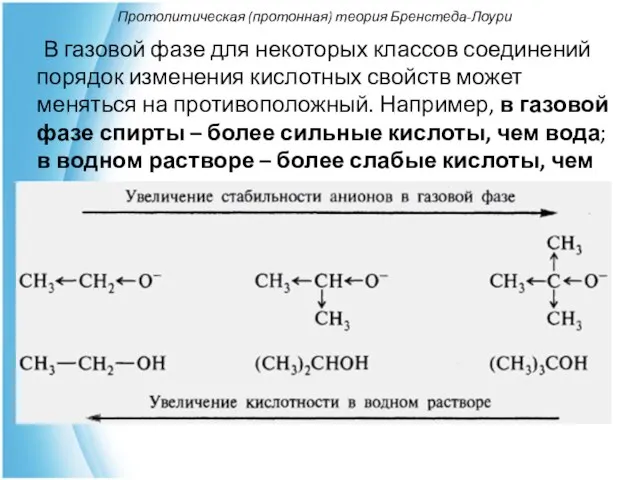
- 30. Протолитическая (протонная) теория Бренстеда-Лоури В газовой фазе для некоторых классов соединений порядок изменения кислотных свойств может
- 31. Протолитическая (протонная) теория Бренстеда-Лоури Основания Бренстеда В роли оснований могут выступать органические соединения, способные принимать протон.
- 32. Протолитическая (протонная) теория Бренстеда-Лоури В процессе взаимодействия протона с π-основаниями происходит частичное перекрывание S-орбитали протона со
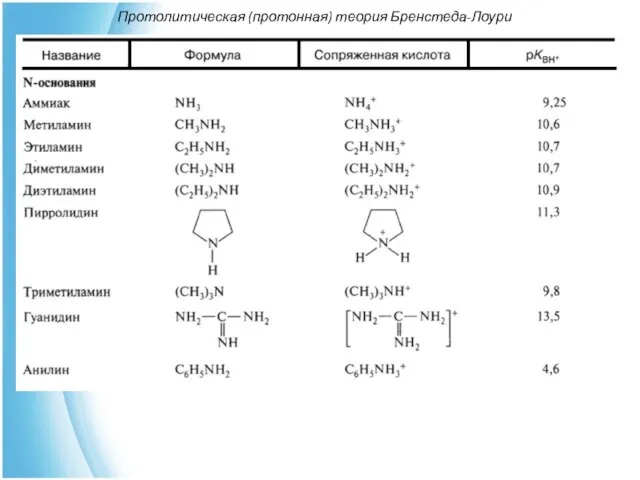
- 33. Протолитическая (протонная) теория Бренстеда-Лоури В n-основаниях центром основности является атом с неподеленной парой электронов, чаще всего
- 34. Протолитическая (протонная) теория Бренстеда-Лоури n-Основания-анионы по основности превосходят нейтральные молекулы. Так, амид-ион NH-2, гидроксид-ион ОН- и
- 35. Протолитическая (протонная) теория Бренстеда-Лоури
- 36. Протолитическая (протонная) теория Бренстеда-Лоури
- 37. Протолитическая (протонная) теория Бренстеда-Лоури По аналогии с кислотами, сила оснований зависит от природы основного центра, электронных
- 38. Протолитическая (протонная) теория Бренстеда-Лоури Еще более слабыми основаниями являются π-основания, в которых пара электронов, присоединяющая протон,
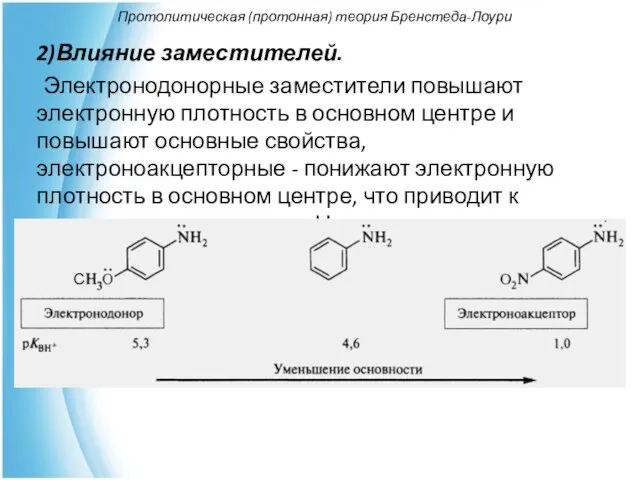
- 39. Протолитическая (протонная) теория Бренстеда-Лоури 2)Влияние заместителей. Электронодонорные заместители повышают электронную плотность в основном центре и повышают
- 40. Протолитическая (протонная) теория Бренстеда-Лоури Алифатические амины, содержащие электронодонорные алкильные группы у атома азота, более сильные основания,
- 41. Протолитическая (протонная) теория Бренстеда-Лоури 3)Влияние растворителя. Сольватация может оказывать сильное воздействие на собственную основность алифатических аминов.
- 42. Протолитическая (протонная) теория Бренстеда-Лоури Амфотерность органических соединений Характерной чертой органических соединений является амфотерность, т.е. способность выступать
- 43. Теория Льюиса II. Теория Льюиса В 1923 году Льюис предложил более общую (электронную) теорию кислот и
- 44. Теория Льюиса Кислоты Льюиса - частицы, имеющие свободные орбитали и способные к присоединению электронной пары, т.е.
- 45. Теория Льюиса Основания Льюиса - частицы, имеющие свободные электронные пары и способные к их отдаче, т.е.
- 46. Теория Льюиса Взаимодействие между кислотой и основанием сводится к донорно-акцепторному характеру, т.е. любое органическое соединение можно
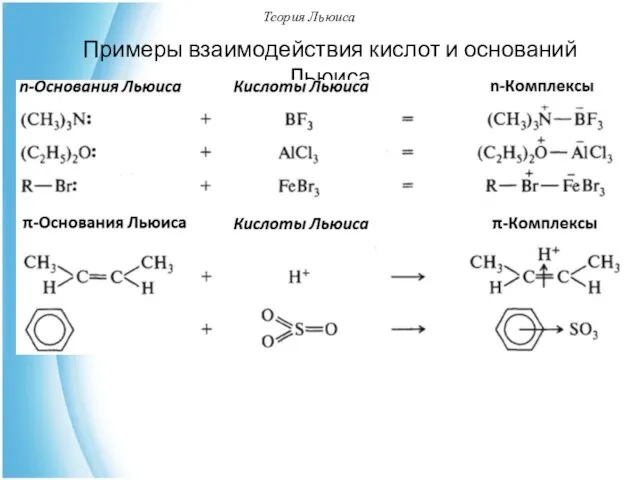
- 47. Теория Льюиса Примеры взаимодействия кислот и оснований Льюиса
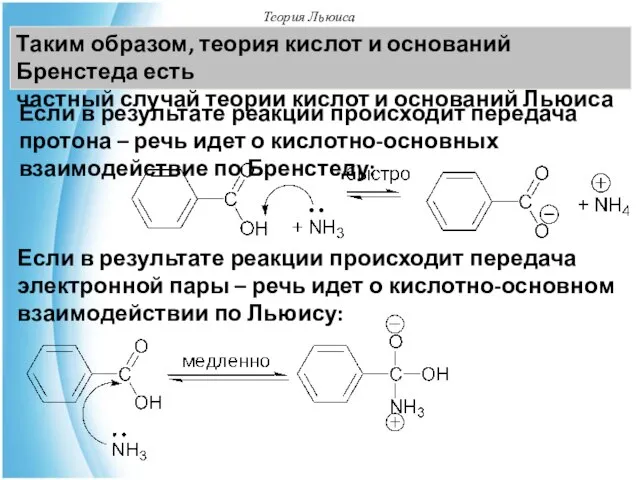
- 48. Теория Льюиса Таким образом, теория кислот и оснований Бренстеда есть частный случай теории кислот и оснований
- 49. Теория Льюиса Жесткие и мягкие кислоты и основания Развитие теории Льюиса привело к созданию принципа жестких
- 50. Теория Льюиса К жестким основаниям относятся донорные частицы, обладающие высокой электроотрицательностью, низкой поляризуемостью, трудно окисляющиеся. К
- 51. Теория Льюиса Жесткие кислоты имеют малые по размеру атомы, тем самым обладают большим положительным зарядом, и
- 52. Теория Льюиса
- 53. Теория Льюиса Жесткие основания преимущественно будут реагировать с жесткими кислотами, а мягкие - с мягкими. Например,
- 55. Скачать презентацию











































 Количество вещества
Количество вещества Драгоценные камни
Драгоценные камни Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Классификация химических элементтов
Классификация химических элементтов Кристаллы и правильные многогранники. 11 класс
Кристаллы и правильные многогранники. 11 класс Кислород. Сера
Кислород. Сера Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна
Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна  Генетика клеточного цикла. Надклеточный контроль клеточного деления, роста и апоптоза. (Глава 5)
Генетика клеточного цикла. Надклеточный контроль клеточного деления, роста и апоптоза. (Глава 5) Амоніак
Амоніак  Atmospheric chemistry
Atmospheric chemistry Презентация по Химии "Презентация Металлы в организме человека" - скачать смотреть
Презентация по Химии "Презентация Металлы в организме человека" - скачать смотреть  ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар
ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар Дисциплина: Химия. Лекция 1. Растворы
Дисциплина: Химия. Лекция 1. Растворы Общие пути обмена аминокислот. (Лекция 11)
Общие пути обмена аминокислот. (Лекция 11) Коллоидные растворы
Коллоидные растворы Введение. Предмет и содержание фармацевтической химии, её связи с другими науками
Введение. Предмет и содержание фармацевтической химии, её связи с другими науками Ионная химическая связь
Ионная химическая связь Углеводы: моносахариды, олиго- и полисахариды
Углеводы: моносахариды, олиго- и полисахариды Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2)
Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2) Металлы: общая характеристика
Металлы: общая характеристика Итоговая консультация. Формульный диктант
Итоговая консультация. Формульный диктант Металлы и их активность
Металлы и их активность Химиялық элемент алюминий
Химиялық элемент алюминий Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Ориентационная вытяжка полимеров
Ориентационная вытяжка полимеров Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В.
Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В. Углеводы. Моносахариды, олигосахариды (дисахариды)
Углеводы. Моносахариды, олигосахариды (дисахариды) Сера. Строение атома, аллотропия, свойства и применение серы
Сера. Строение атома, аллотропия, свойства и применение серы