Содержание
- 2. Проблема «дополнительных валентностей» CuSO4.4NH3 – Андрей Либавий, 1597 г. AgCl.2NH3 – И. Глаубер, 1648 г. CoCl3.6NH3
- 3. Двойная соль или комплексное соединение? KCr(SO4)2∙ 12H2O – хромокалиевые квасцы KCr(SO4)2∙ 12H2O = = K+ +
- 4. Теория Бломстранда - Иёргенсона К. В. Бломстранд (1826-1897), профессор университета в Лунде, 1869 г. «Современная химия»
- 5. Валентность постоянная или переменная? «Соединительная сила» Эдуард Франкланд, 1852 г. «Атомность» «Валентность» Г. Вихельгауз, 1868 г.
- 6. Цепь аммиаков может быть, по-видимому, беспредельна, и, нам кажется, наиболее существенный недостаток такого представления и состоит
- 7. Рождение координационной теории Альфред Вернер «К вопросу о строении неорганических соединений». 1893 г. Главная и побочная
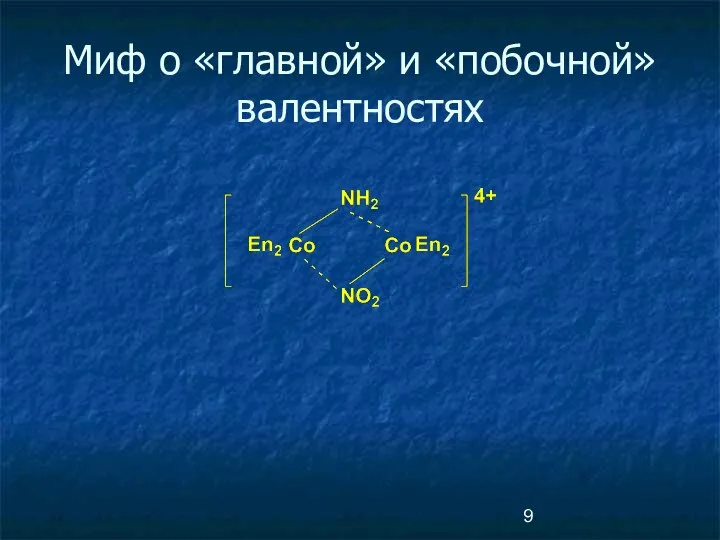
- 8. Главная и побочная валентности PtCl4.2NH3 Pt Cl Cl Cl Cl NH3 NH3 Главная валентность соответствует обычной
- 9. Миф о «главной» и «побочной» валентностях
- 10. Строение комплексного соединения K3 [Fe(CN)6] Ион- Комплексо- образователь Лиганды Координационное число Внутренняя сфера Внешняя сфера [Cu(NH3)4]Cl2
- 11. Рождение стереохимии Якоб Вант-Гофф (1852 — 1912) 1874 г. «Предложение применять в пространстве современные структурно-химические формулы
- 12. Строение комплексного соединения K3 [Fe(CN)6] [Cu(NH3)4]Cl2 [Zn(NH3)4]Cl2
- 13. Номенклатура комплексных соединений K3 [Fe(CN)6] Гексацианоферрат(III) калия [Cu(NH3)4]Cl2 Хлорид тетраамминмеди(II) +3 +2 Порядок перечисления лиганд: Анионные:
- 14. Упражнение 1 Первое основание Рейзе [Pt(NH3)4](OH)2 Соль Чугаева [PtCl(NH3)5]Cl3 Соль Цейзе K[PtCl3C2H4] Пурпуреосоль [CoCl(NH3)5]Cl2 Кроцеосоль [Co(NO2)2(NH3)4]Cl
- 15. Упражнение 2 Гексанитрокобальтат(III) натрия Na3[Co(NO2)6] Гидроксид диамминсеребра(I) [Ag(NH3)2]OH реактив Толленса Тетраиодомеркурат(II) калия K2[HgI4] реактив Несслера Тетрароданомеркурат(II)
- 17. Вернер подтверждает Вернера 1893-4 гг. не были периодом утверждения теории. Вернер 20 лет не оставлял лаборатории
- 18. Ряды Вернера - Миолати 1 [Pt(NH3)6]Cl4 2 [Pt(NH3)5Cl]Cl3 3 [Pt(NH3)4Cl2]Cl2 4 [Pt(NH3)3Cl3]Cl 5 [Pt(NH3)2Cl4] 6 K[Pt(NH3)Cl5]
- 19. Изомерия комплексов PtCl2.2NH3 Pt Pt Cl Cl Cl Cl NH3 NH3 NH3 NH3 Соль Пейроне Хлорид
- 20. Сольватная изомерия
- 21. Механизм образования комплексного иона [Al(OH)4]-
- 22. Комплексные соединения в растворах Первичная диссоциация комплексных соединений K3[Fe(CN)6] = 3K+ + [Fe(CN)6]3- [Cu(NH3)4]SO4 = [Cu(NH3)4]2+
- 23. Вторичная диссоциация комплексов [Ag(NH3)2]+ [Ag(NH3)]+ + NH3 [Ag(NH3)]+ Ag+ + NH3 [Ag+] [NH3]2 KH = =
- 24. Константы нестойкости некоторых комплексов
- 25. Что же такое комплексы? Комплексные соединения – вещества, существующие как в кристаллическом состоянии, так и в
- 26. Полидентатные лиганды ЭДТА Этилендиамин En
- 27. Хелатные комплексные соединения Термин «хелат» 1920 г. Морган и Дрю
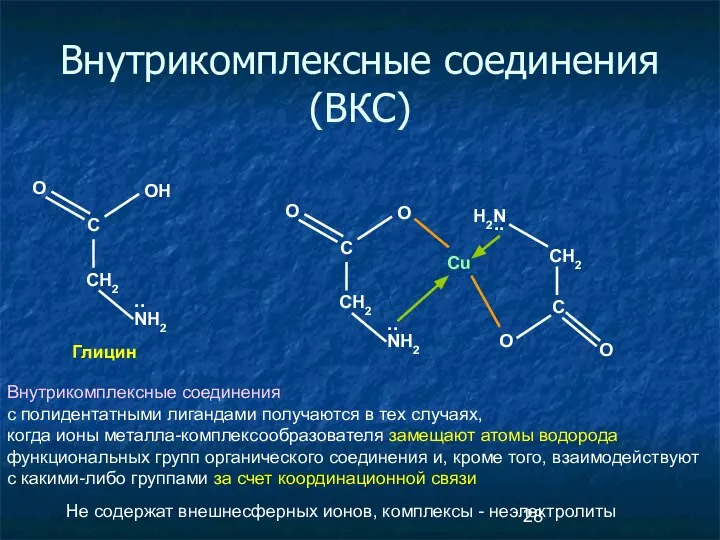
- 28. Внутрикомплексные соединения (ВКС) CH2 С OH NH2 .. Глицин O Cu CH2 С O NH2 ..
- 29. Качественная реакция на Ni2+ c диметилглиоксимом Реактив Чугаева Лев Александрович Чугаев (1873-1922)
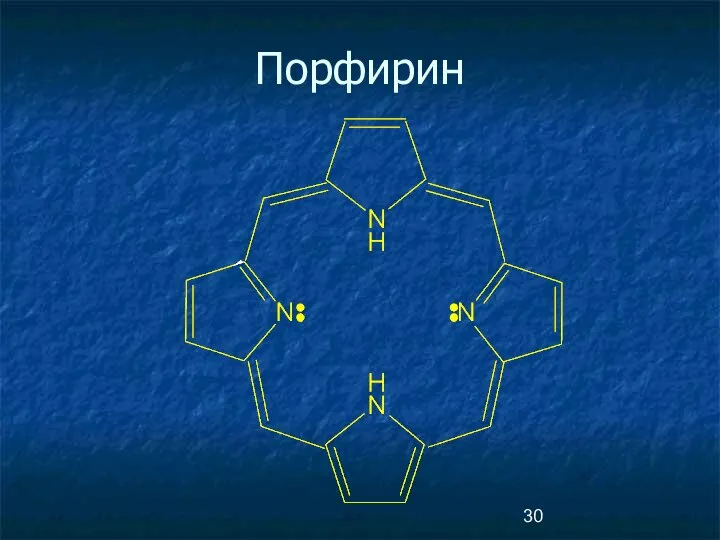
- 30. Порфирин
- 31. Хлорофилл
- 32. Гемоглобин
- 33. B12 1964 г. – Дороти Ходжкин
- 34. Альфред Вернер 1866-1919 1866 г. – родился в Мюлузе (Эльзас)
- 35. 1891 г. – конкурсная работа на звание приват-доцента «К теории сродства и валентности» 1891 г –
- 36. Альфред Вернер 1866-1919 В 1913 г. шведский король Густав V вручил Альфреду Вернеру золотую медаль лауреата
- 37. Спасибо за внимание!
- 39. Скачать презентацию







![Строение комплексного соединения K3 [Fe(CN)6] Ион- Комплексо- образователь Лиганды Координационное число](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-9.jpg)

![Строение комплексного соединения K3 [Fe(CN)6] [Cu(NH3)4]Cl2 [Zn(NH3)4]Cl2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-11.jpg)
![Номенклатура комплексных соединений K3 [Fe(CN)6] Гексацианоферрат(III) калия [Cu(NH3)4]Cl2 Хлорид тетраамминмеди(II) +3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-12.jpg)
2 Соль Чугаева [PtCl(NH3)5]Cl3 Соль Цейзе](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-13.jpg)
![Упражнение 2 Гексанитрокобальтат(III) натрия Na3[Co(NO2)6] Гидроксид диамминсеребра(I) [Ag(NH3)2]OH реактив Толленса Тетраиодомеркурат(II)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-14.jpg)


![Ряды Вернера - Миолати 1 [Pt(NH3)6]Cl4 2 [Pt(NH3)5Cl]Cl3 3 [Pt(NH3)4Cl2]Cl2 4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-17.jpg)


![Механизм образования комплексного иона [Al(OH)4]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-20.jpg)
![Комплексные соединения в растворах Первичная диссоциация комплексных соединений K3[Fe(CN)6] = 3K+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-21.jpg)
![Вторичная диссоциация комплексов [Ag(NH3)2]+ [Ag(NH3)]+ + NH3 [Ag(NH3)]+ Ag+ + NH3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/754372/slide-22.jpg)











 Термодинамика. Законы термодинамики
Термодинамика. Законы термодинамики Алкадиены. Диеновые углеводороды
Алкадиены. Диеновые углеводороды Растительные источники жиров и жирных масел
Растительные источники жиров и жирных масел Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства
Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства Діагностика за показами газоаналізатора. Типи газоаналізаторів
Діагностика за показами газоаналізатора. Типи газоаналізаторів Презентация по Химии "Сильнодіючі отруйні речовини: поняття та класифікація." - скачать смотреть бесплатно
Презентация по Химии "Сильнодіючі отруйні речовини: поняття та класифікація." - скачать смотреть бесплатно Природный каучук
Природный каучук Гранулирование. Виды грануляции
Гранулирование. Виды грануляции Метаморфогенные месторождения
Метаморфогенные месторождения Legătura chimică
Legătura chimică Total Syntheses of Trichorabdal A and Maoecrystal Z
Total Syntheses of Trichorabdal A and Maoecrystal Z Культивирование растительных и животных клеток
Культивирование растительных и животных клеток Оптические свойства дисперсных систем
Оптические свойства дисперсных систем Принципы создания полимерных конструкционных нанокомпозитов
Принципы создания полимерных конструкционных нанокомпозитов Жиры (9 класс)
Жиры (9 класс) Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс Химик-эколог
Химик-эколог Нафта
Нафта  Рубрифлордилатктон. Стратегия синтеза
Рубрифлордилатктон. Стратегия синтеза Синтез липидов
Синтез липидов Окислительные свойства концентрированной серной кислоты
Окислительные свойства концентрированной серной кислоты Тайна воды которую мы пьём
Тайна воды которую мы пьём Учитель химии МБОУ СОШ №79 г. о. Самара Язрикова Любовь Михайловна
Учитель химии МБОУ СОШ №79 г. о. Самара Язрикова Любовь Михайловна Автомобильные бензины и дизельные топлива. Характеристика и классификация автомобильных топлив
Автомобильные бензины и дизельные топлива. Характеристика и классификация автомобильных топлив Биоорганическая химия
Биоорганическая химия Соляная кислота и её соли
Соляная кислота и её соли Cromatografie de lichide de inalta performanta cuplata cu spectrometrie de masă
Cromatografie de lichide de inalta performanta cuplata cu spectrometrie de masă Полістирол. Визначення, фізичні властивості
Полістирол. Визначення, фізичні властивості