Содержание
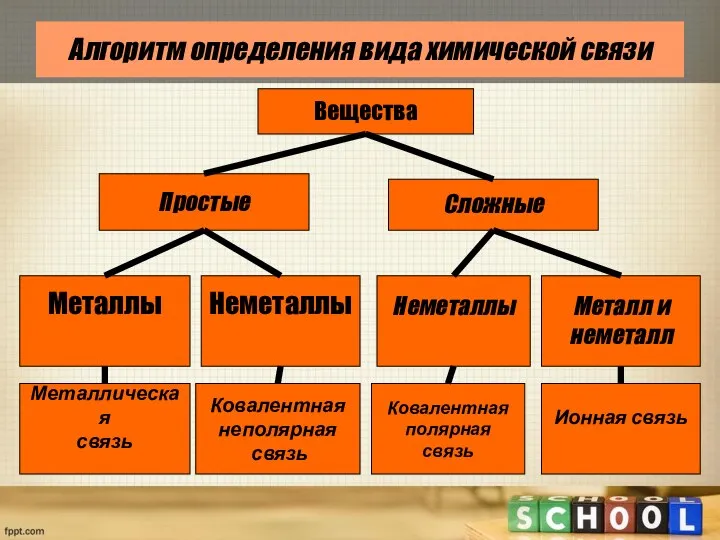
- 2. Алгоритм определения вида химической связи Вещества Простые Сложные Ковалентная неполярная связь Металлическая связь Ковалентная полярная связь
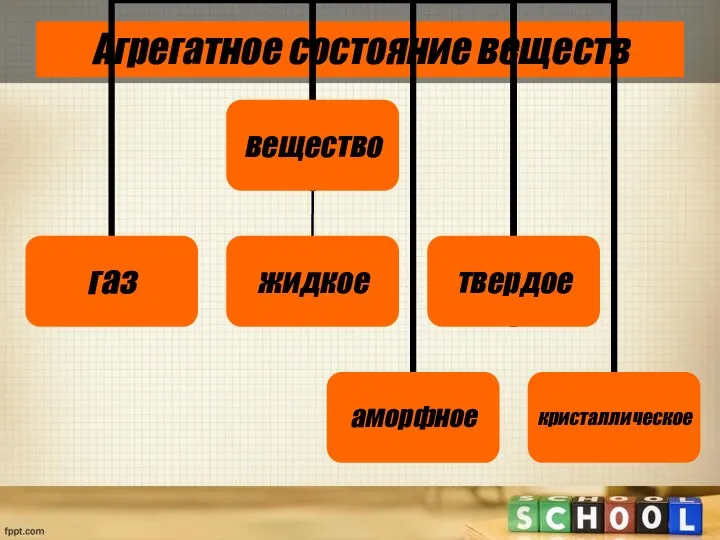
- 3. Агрегатное состояние веществ
- 4. Вещества в твердом состоянии, как правило, имеют кристаллическое строение, для которого характерно определенное расположение частиц в
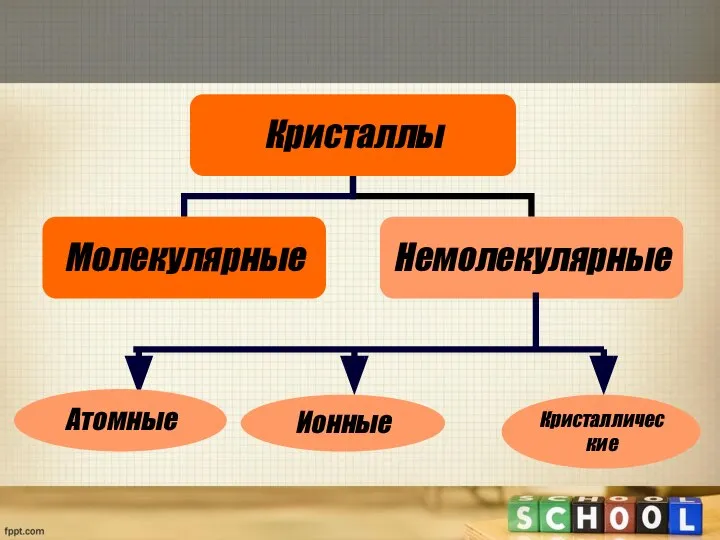
- 5. Кристаллы – твердые вещества, частицы которых образуют периодически повторяющуюся в пространстве структуру – кристаллическую решетку. Кристаллические
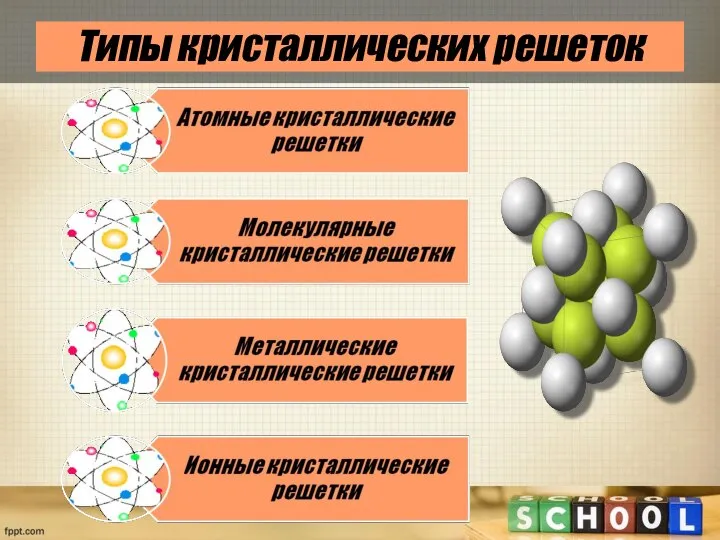
- 6. Типы кристаллических решеток
- 7. Атомные Ионные Кристаллические
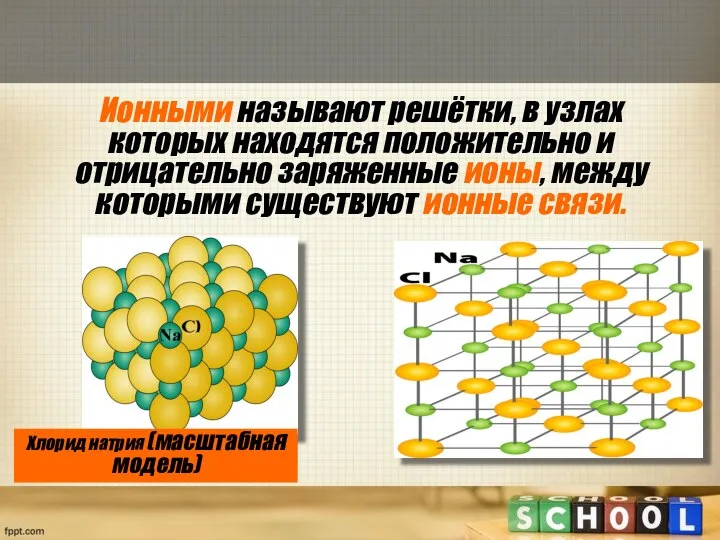
- 8. Ионными называют решётки, в узлах которых находятся положительно и отрицательно заряженные ионы, между которыми существуют ионные
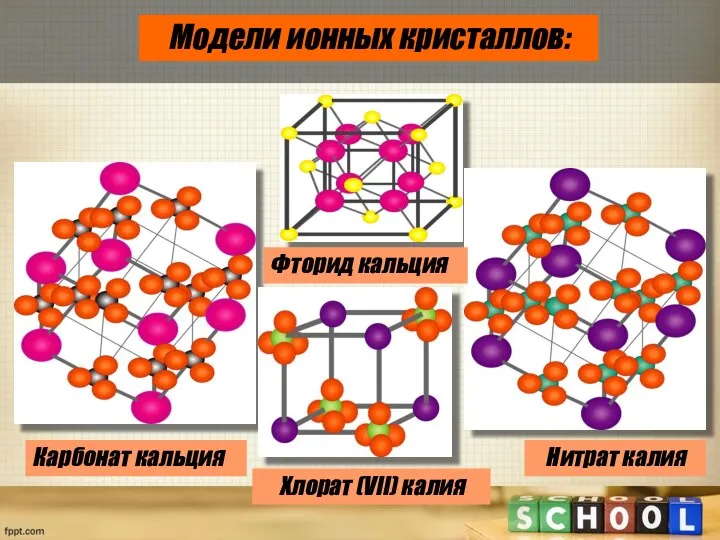
- 9. Модели ионных кристаллов: Карбонат кальция Фторид кальция Хлорат (VII) калия Нитрат калия
- 10. Ионные кристаллы с ионной связью (большинство солей) обладают высокой твёрдостью, и тугоплавкостью, малолетучи, растворимы только в
- 11. Вещества с ионной кристаллической решеткой Мел Каменная соль Малахит Поташ
- 12. Атомные кристаллические решетки Атомной называется решётка, в узлах которой находятся отдельные атомы, соединённые между собой прочными
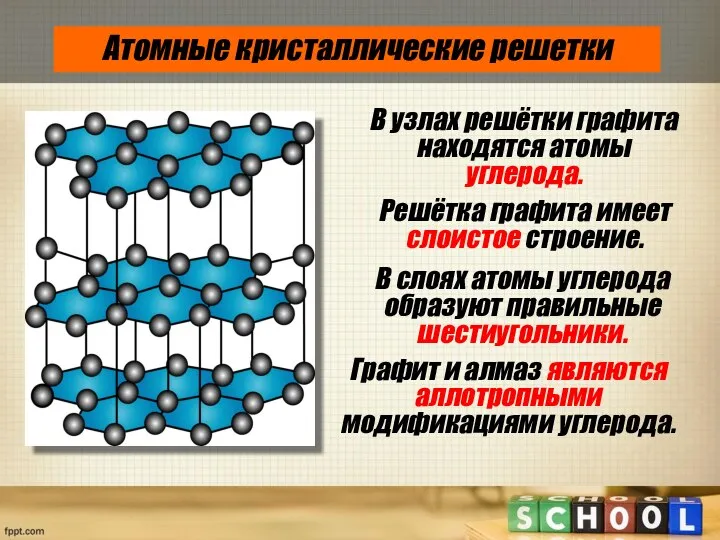
- 13. Атомные кристаллические решетки Графит и алмаз являются аллотропными модификациями углерода. В слоях атомы углерода образуют правильные
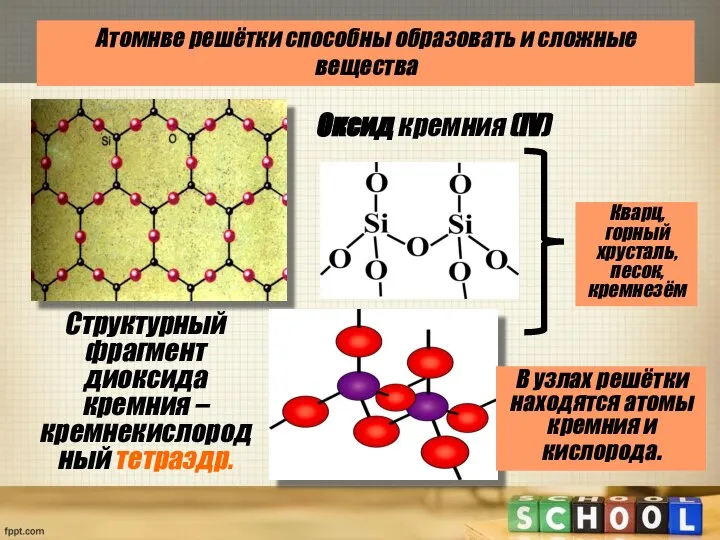
- 14. Атомнве решётки способны образовать и сложные вещества Кварц, горный хрусталь, песок, кремнезём Оксид кремния (IV) В
- 15. Физические свойства атомных кристаллических решеток Атомные кристаллы (алмаз, кремний, германий, бор, оксид и карбид кремния) обладают
- 16. Вещества с атомной кристаллической решеткой Простые: Сложные: Кремний Карборунд SiC Кварц SiO2 Графит Алмаз
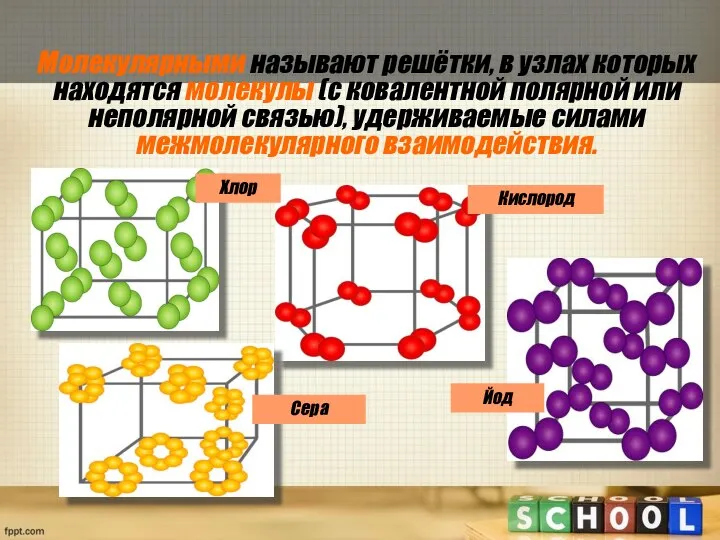
- 17. Молекулярными называют решётки, в узлах которых находятся молекулы (с ковалентной полярной или неполярной связью), удерживаемые силами
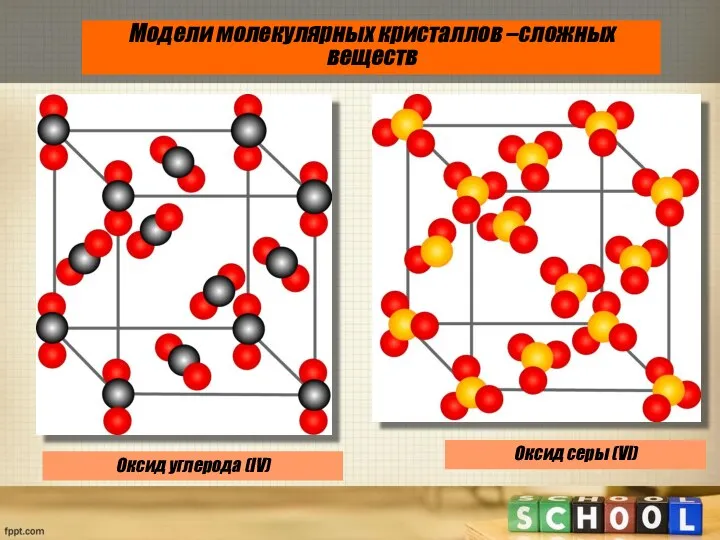
- 18. Модели молекулярных кристаллов –сложных веществ Оксид углерода (IV) Оксид cеры (VI)
- 19. Физические свойства молекулярных кристаллических решеток Молекулярные кристаллы с неполярной связью (водород, сера, фосфор и др.) обладают
- 20. Вещества с молекулярной кристаллической решеткой Простые: Сложные: Неорганические: Органические: Йод Бром Вода Сахароза
- 21. Металлическими называют решётки, в узлах которых находятся отдельные атомы или ионы металлов, которые связаны между собой
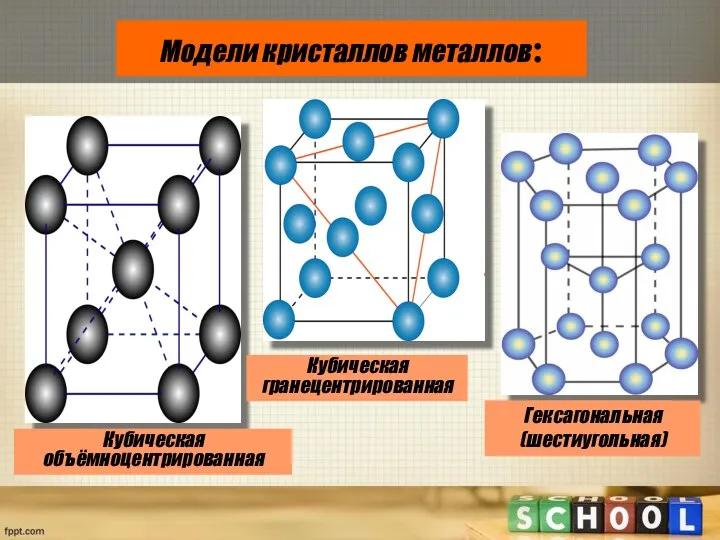
- 22. Модели кристаллов металлов: Кубическая объёмноцентрированная Кубическая гранецентрированная Гексагональная (шестиугольная)
- 23. Вещества с металлической кристаллической решеткой Магний Алюминий Золото Медь
- 24. Обратите внимание Тип химической связи Ионная (NaCI, K2S, CaO…) Ковалентная а) неполярная (алмаз, SiC.., H2, F2,
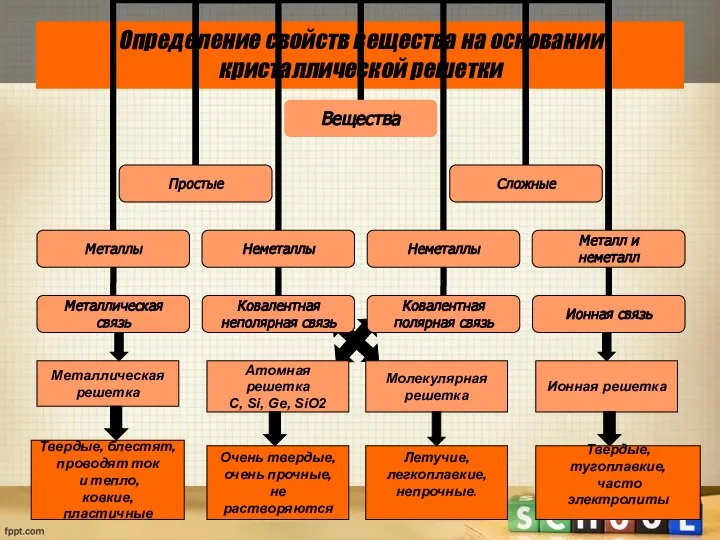
- 25. Определение свойств вещества на основании кристаллической решетки Металлическая решетка Твердые, блестят, проводят ток и тепло, ковкие,
- 26. Типы кристаллических решёток простых веществ
- 28. Скачать презентацию













 Biochemistry of thyroid hormones
Biochemistry of thyroid hormones Біохімічний рівень організації
Біохімічний рівень організації Октановое и цетановое числа
Октановое и цетановое числа ГИДРОЛИЗ СОЛЕЙ 9 класс Учитель биологии и химии Шапошникова Т.С.
ГИДРОЛИЗ СОЛЕЙ 9 класс Учитель биологии и химии Шапошникова Т.С.  Современная химия. (Лекция 6)
Современная химия. (Лекция 6) Углеводы. 10 класс
Углеводы. 10 класс Нуклеїнові кислоти
Нуклеїнові кислоти Дисперсные системы. Коллоидные растворы
Дисперсные системы. Коллоидные растворы Металлы. Урок – обобщения
Металлы. Урок – обобщения Агрегатные состояния вещества. Плавление и отвердевание кристаллических тел
Агрегатные состояния вещества. Плавление и отвердевание кристаллических тел Периодическая Система Д. И. Менделеева в свете учения о строении атома
Периодическая Система Д. И. Менделеева в свете учения о строении атома Кислород. История открытия. Применение кислорода
Кислород. История открытия. Применение кислорода Курс химии (Литвиновой Татьяны Николаевны)
Курс химии (Литвиновой Татьяны Николаевны) Презентация по химии Химия
Презентация по химии Химия Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия
Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия  Химическая связь. (Лекция 3)
Химическая связь. (Лекция 3) Жалпы химиялық технология
Жалпы химиялық технология Физическая и коллоидная химия
Физическая и коллоидная химия Занимательные опыты в качественном анализе
Занимательные опыты в качественном анализе Алкан және алкендер негізінде БАЗ-дарды синтездеу
Алкан және алкендер негізінде БАЗ-дарды синтездеу Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине Предмет химии. Вещества
Предмет химии. Вещества Строение атома пз и пс Д.И. Менделеева в свете квантовомеханической теории строения атома
Строение атома пз и пс Д.И. Менделеева в свете квантовомеханической теории строения атома Алюминий. Природные соединения алюминия
Алюминий. Природные соединения алюминия Изучение химического состава и лечебных свойств воды и грязи озера Дус-Холь
Изучение химического состава и лечебных свойств воды и грязи озера Дус-Холь Биохимия. Разделы биохимии. Становление биохимии как науки
Биохимия. Разделы биохимии. Становление биохимии как науки Роль спиртов в жизни человека
Роль спиртов в жизни человека Структурные превращения стали 15Х5М при различных режимах термической обработки
Структурные превращения стали 15Х5М при различных режимах термической обработки