Содержание
- 3. Степень окисления простых веществ равна нулю: Н20, Cl20, S0, Са0 Степень окисления Ион водорода H в
- 4. Кислород О–2 чаще всего –2 (кроме H2O2, здесь кислород –1) Постоянную степень окисления имеют: атомы щелочных
- 5. K+1N+ХO +1+Х + (–2)3 = 0 Х = +5 (N+ХO )– +Х + (–2)3 = –1
- 6. не ОВР HCl + KOH = KCl + H2O ОВР S4+O2 + N4+O2 = S6+O3 +
- 7. Окисление – процесс отдачи электронов реагирующей частицей (молекула, атом, ион), при которой степень окисления элемента повышается.
- 8. Процесс окисления: Восстановитель N0 – 3e → N+3 Процесс восстановления: Окислитель N0 + 3e → N3–
- 9. Типы ОВР 1. Межмолекулярная ОВР Mn4+O2+4HBr1– = Mn2+Br2+Br20+2H2O ок-ль в-ль Окислитель и восстановитель входят в состав
- 10. 2. Внутримолекулярная ОВР 2KCl5+O = 2KCl1– + 3O ок-ль в-ль Окислитель и восстановитель – разные элементы,
- 11. 3. Реакция диспропорционирования (самоокисления-самовосстановления) 2N4+O2 + H2O → HN3+O2 + HN5+O3 N4+ + 1 = N3+
- 12. FeSO4 + KClO3 + H2SO4 = = Fe2(SO4)3 + KCl + 3H2O Метод электронного баланса 1.
- 13. 2. Составляем электронный баланс. Fe2+ – 1e = Fe3+ 6 Cl5+ + 6e = Cl– 1
- 14. Влияние среды на ОВР Перманганат калия KMnO4 1. Среда кислая 2KMn7+O4 + 5KN3+O2 + 3H2SO4 =
- 15. 2. Среда нейтральная 2KMn7+O4 + 3KN3+O2 + H2O = = 2Mn4+O2↓ + 3KN5+O3 + 2KOH Mn7+
- 16. 3. Среда щелочная 2KMn7+O4 + KN3+O2 + 2KOH = = 2K2Mn6+O4 + KN5+O3 + H2O Mn7+
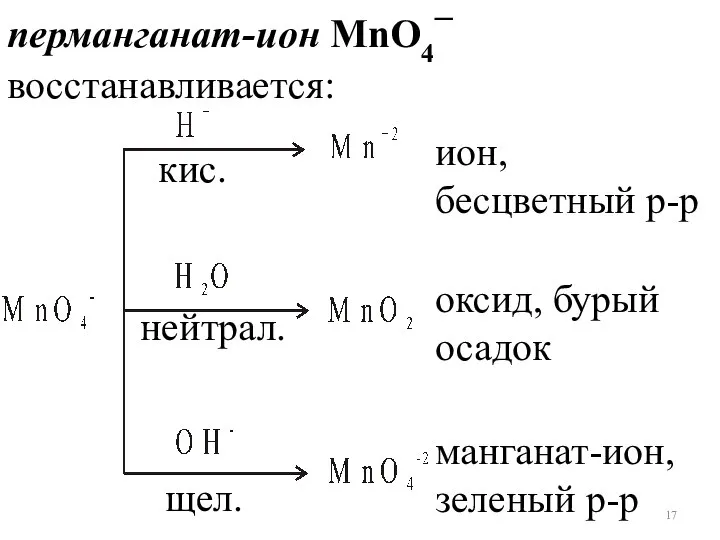
- 17. ион, бесцветный р-р оксид, бурый осадок манганат-ион, зеленый р-р перманганат-ион MnO4– восстанавливается: кис. нейтрал. щел.
- 18. Влияние концентрации кислоты на ОВР Азотная кислота HNO3 Pb0 + 4HN5+O3(конц) = = Pb2+(NO3)2 + 2N4+O2↑
- 19. N5+ + 3e = N2+ 2 Pb0 – 2e = Pb2+ 3 ок-ль в-ль ок-е вос-е
- 21. Серная кислота H2SO4 Разбавленная серная кислота Mg + H2SO4 → MgSO4 + H2
- 23. Скачать презентацию



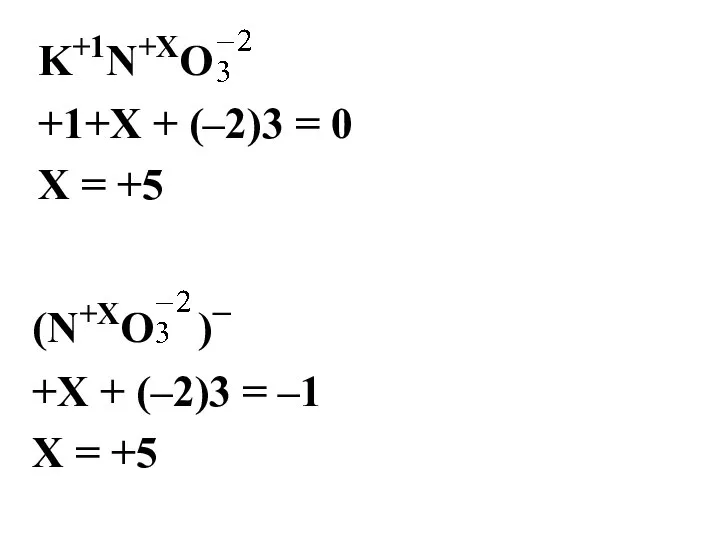
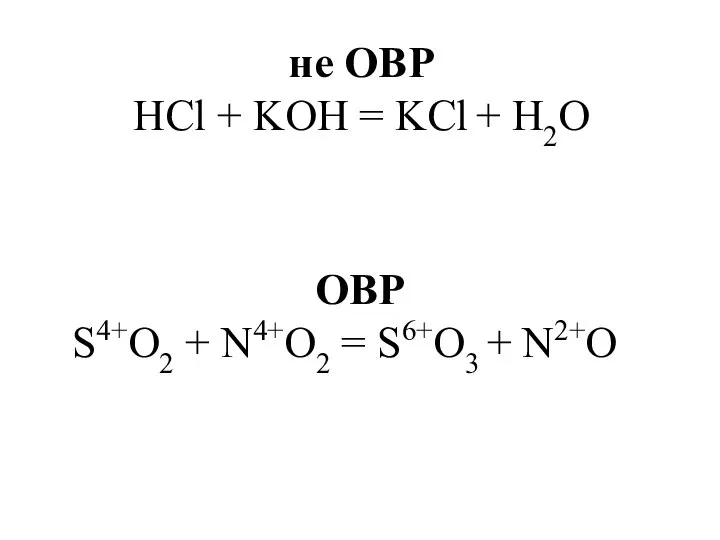














 Полимеры. Классификация полимеров
Полимеры. Классификация полимеров Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Подготовка учащихся к практическим турам олимпиад по химии
Подготовка учащихся к практическим турам олимпиад по химии Мягкие лекарственные формы. Мази, капсулы, суппозитории, пластыри
Мягкие лекарственные формы. Мази, капсулы, суппозитории, пластыри Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Выполнил: ученики 9 класса Проверил: учитель химии Санеева Л.П.
Выполнил: ученики 9 класса Проверил: учитель химии Санеева Л.П. Водород. Растворы. 8 класс
Водород. Растворы. 8 класс Оптическая литография
Оптическая литография Поняття про хімічні засоби захисту рослин (11 клас)
Поняття про хімічні засоби захисту рослин (11 клас) Предмет органической химии. Тест 18
Предмет органической химии. Тест 18 Материалы космической техники
Материалы космической техники Химические элементы O2 и N2
Химические элементы O2 и N2 Загальні способи добування солей. Класифікація неорганічних речовин
Загальні способи добування солей. Класифікація неорганічних речовин Презентация по Химии "Соединения алюминия" - скачать смотреть бесплатно
Презентация по Химии "Соединения алюминия" - скачать смотреть бесплатно Описание основных типов магматических горных пород
Описание основных типов магматических горных пород Смог и его виды
Смог и его виды Природні сполуки алюмінію і методи одержання
Природні сполуки алюмінію і методи одержання Каталитический риформинг
Каталитический риформинг Химия и пища
Химия и пища Дисперсные системы. Поверхностная энергия
Дисперсные системы. Поверхностная энергия Электрохимические методы анализа
Электрохимические методы анализа Chemical kinetics
Chemical kinetics Ядро атома (тест)
Ядро атома (тест) Эндогенная серия. Вулканогенно-осадочная группа
Эндогенная серия. Вулканогенно-осадочная группа Углеводороды. Алканы
Углеводороды. Алканы Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность
Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность Псевдогалогены и их соединения
Псевдогалогены и их соединения Массообменные процессы
Массообменные процессы