Содержание
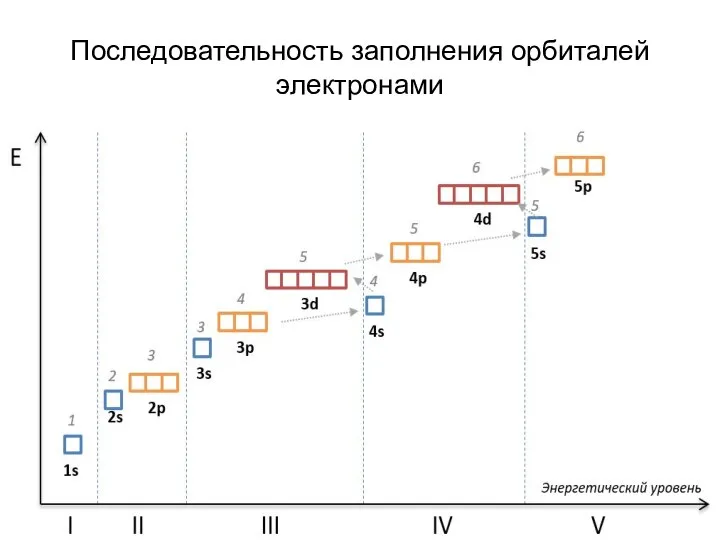
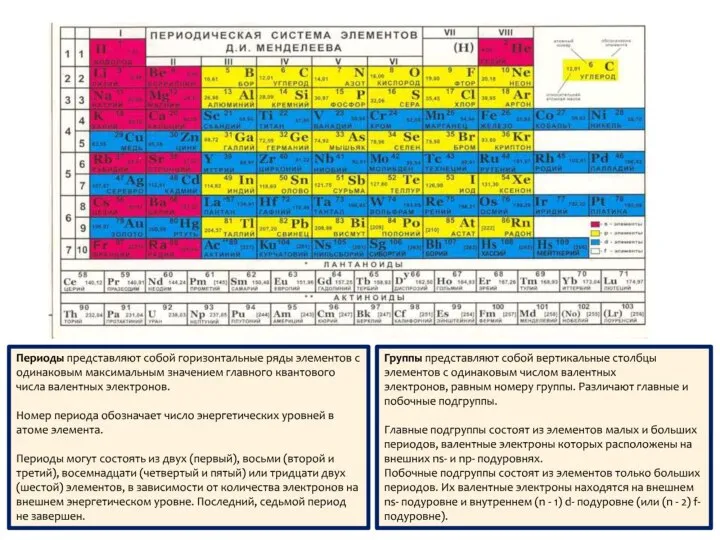
- 13. Последовательность заполнения орбиталей электронами
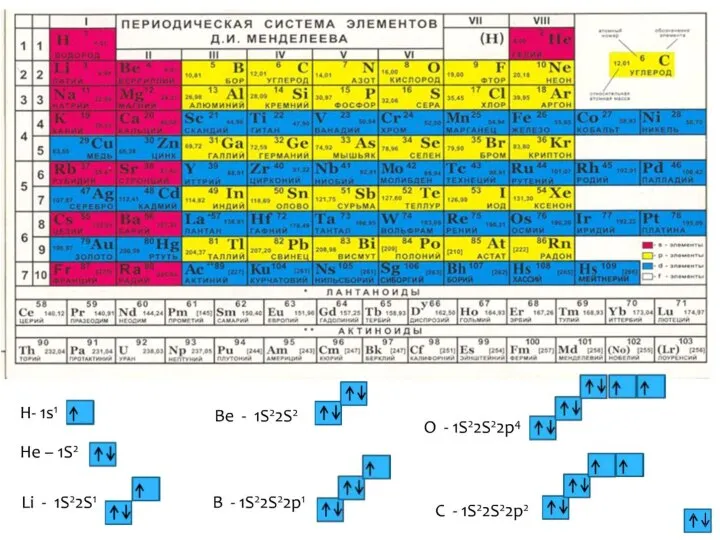
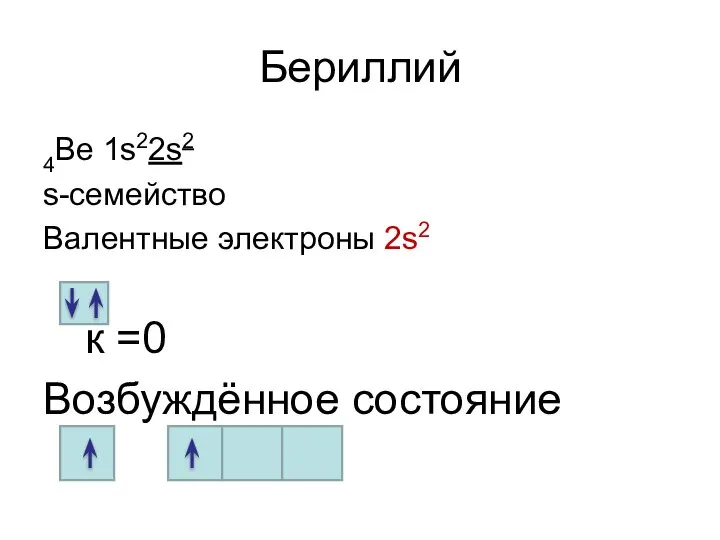
- 16. Бериллий 4Ве 1s22s2 s-семейство Валентные электроны 2s2 к =0 Возбуждённое состояние к= 2
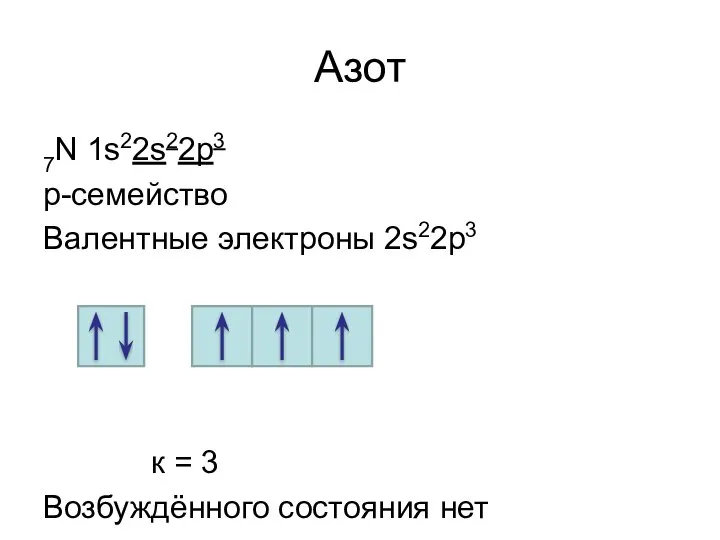
- 17. Азот 7N 1s22s22р3 р-семейство Валентные электроны 2s22р3 к = 3 Возбуждённого состояния нет
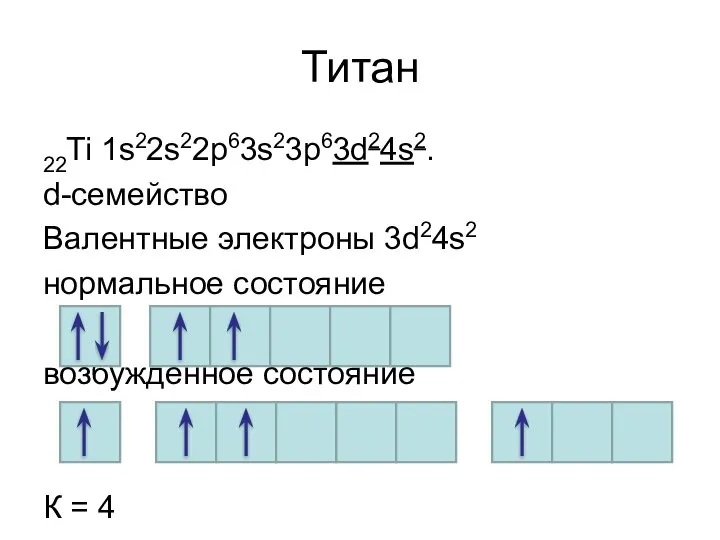
- 18. Титан 22Ti 1s22s22р63s23р63d24s2. d-семейство Валентные электроны 3d24s2 нормальное состояние к = 2 возбужденное состояние К =
- 19. «Проскок» электрона Переход электронов с s-подуровня внешнего энергетического уровня ns на d-подуровень предвнешнего уровня (n –
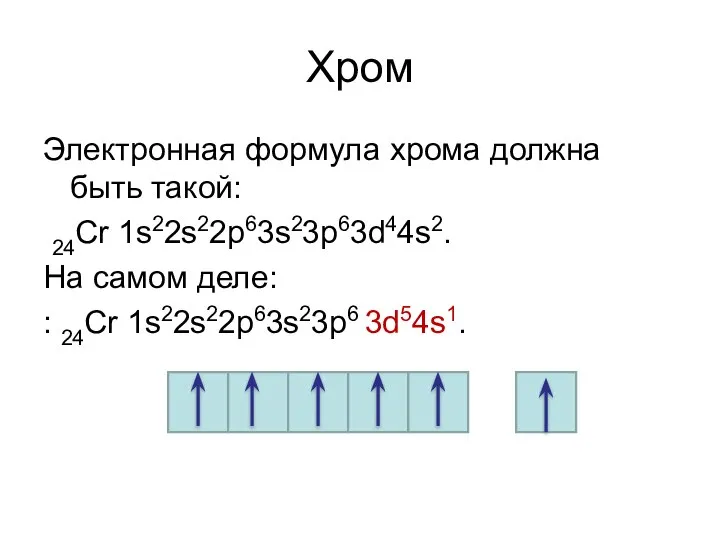
- 20. Хром Электронная формула хрома должна быть такой: 24Cr 1s22s22p63s23p63d44s2. На самом деле: : 24Cr 1s22s22p63s23p6 3d54s1.
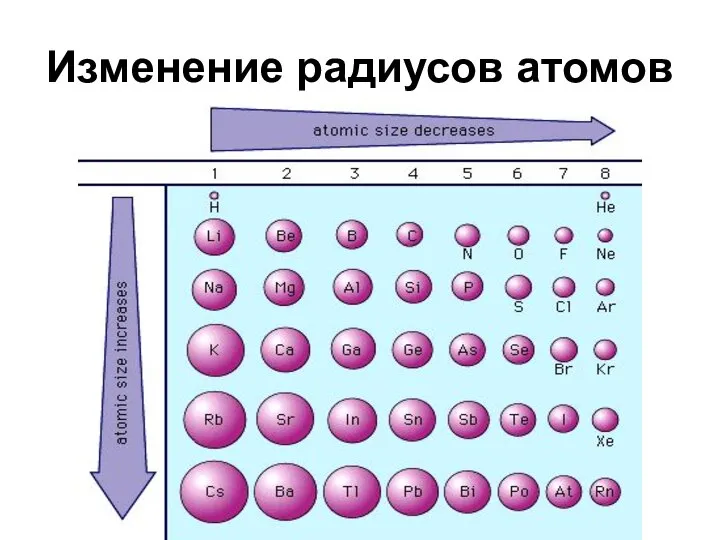
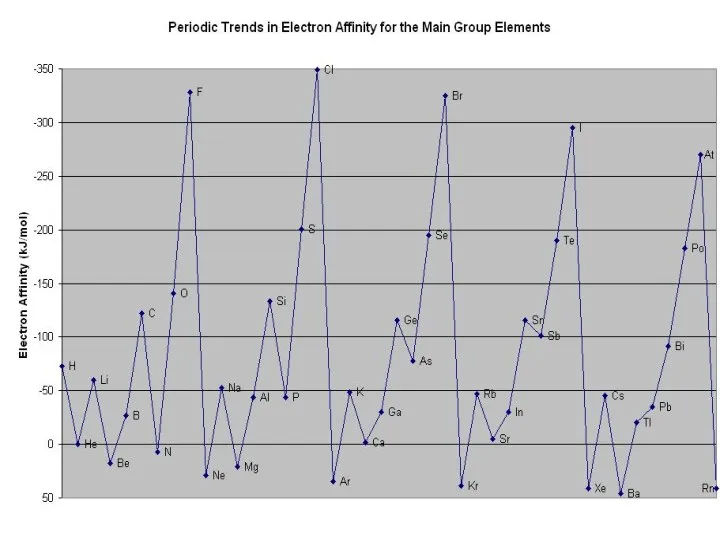
- 25. Изменение радиусов атомов
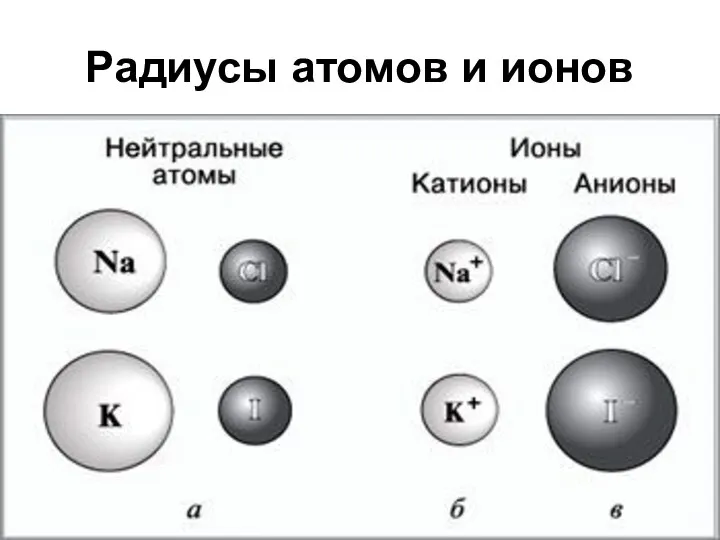
- 26. Радиусы атомов и ионов
- 27. Лантаноидное сжатие
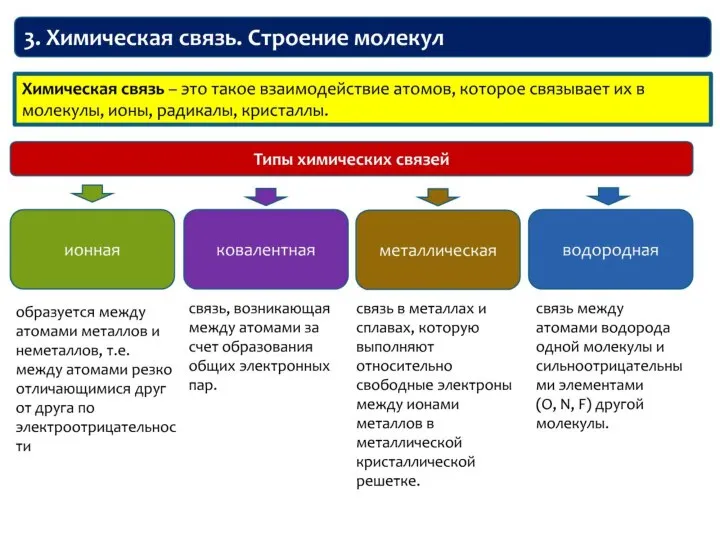
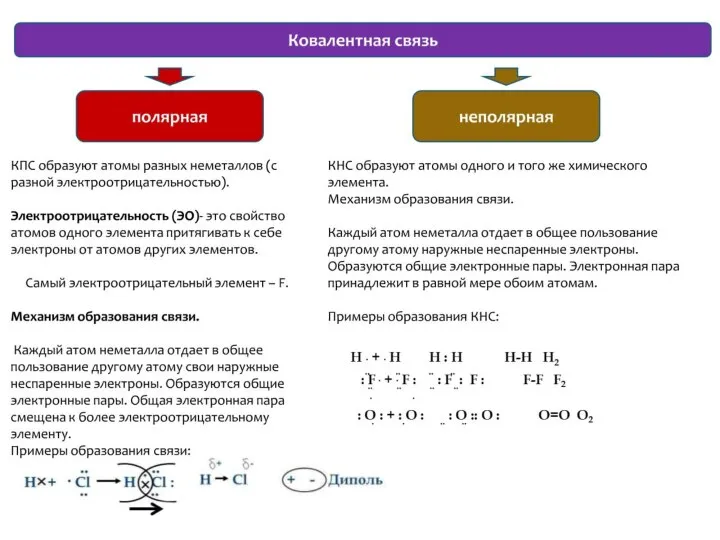
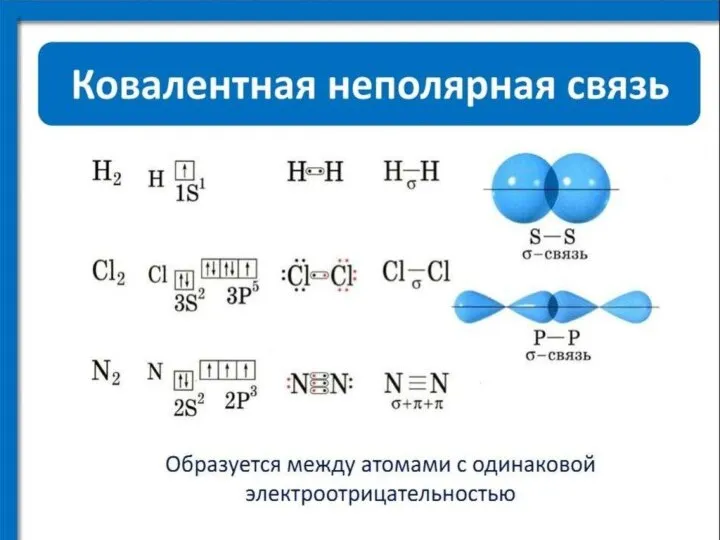
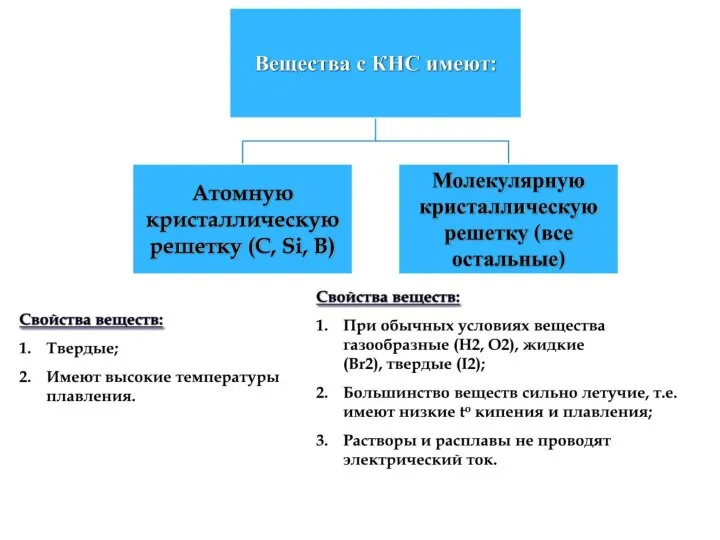
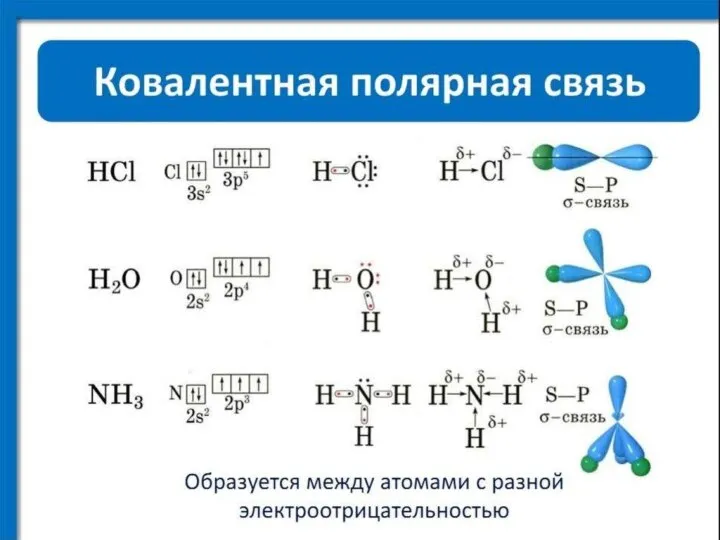
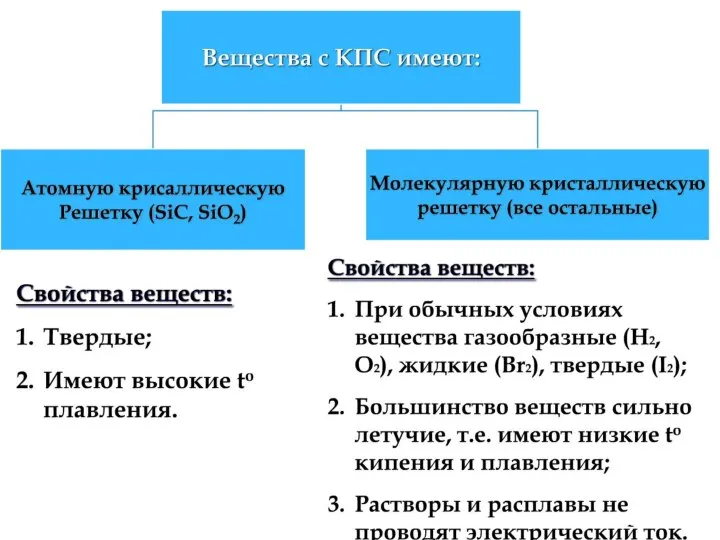
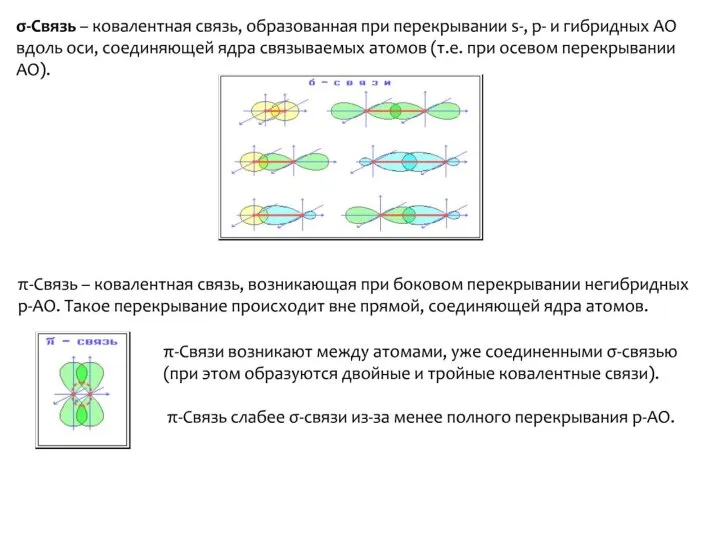
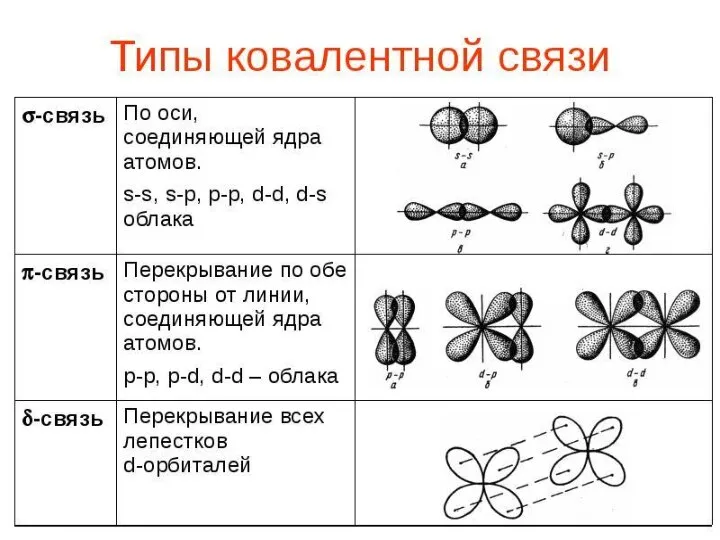
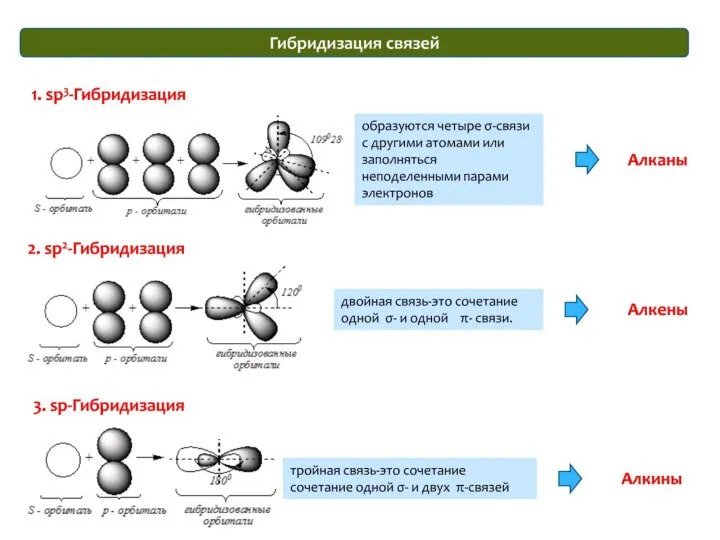
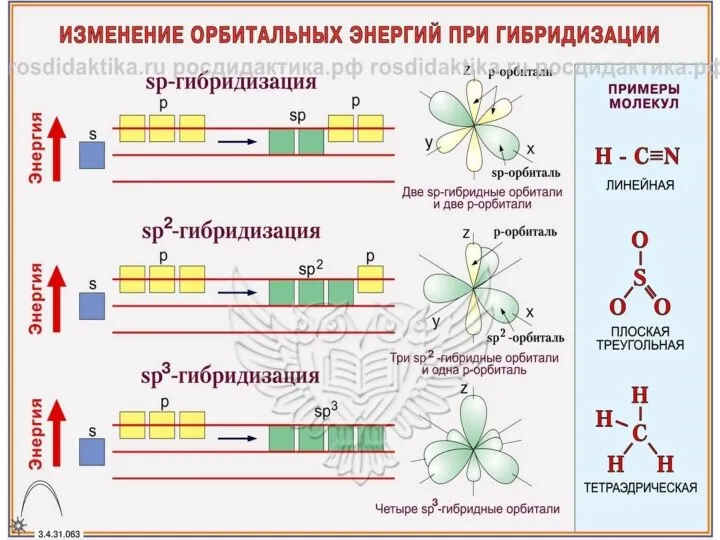
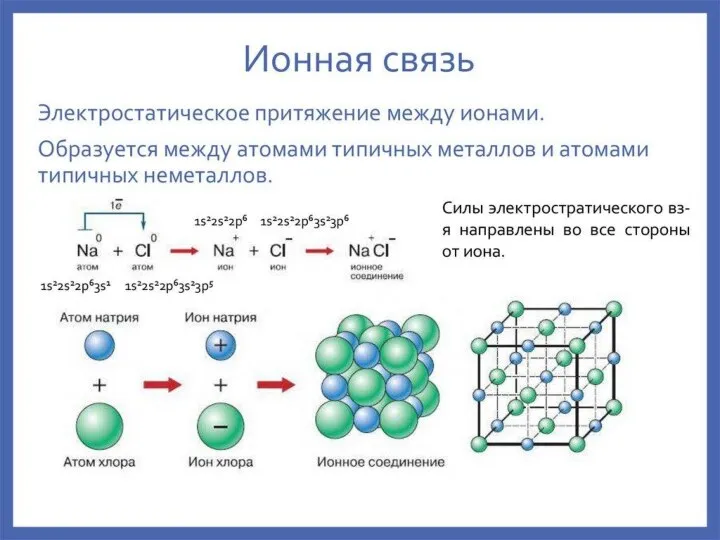
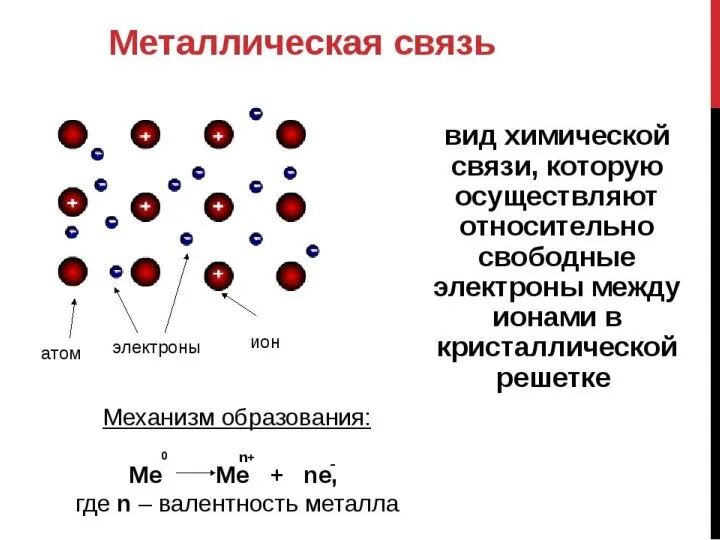
- 35. Лекция 3 ХИМИЧЕСКАЯ СВЯЗЬ. СТРОЕНИЕ МОЛЕКУЛ
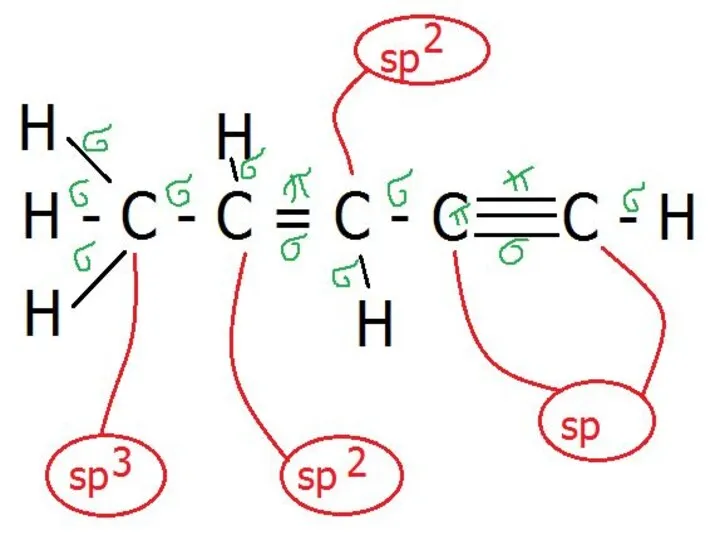
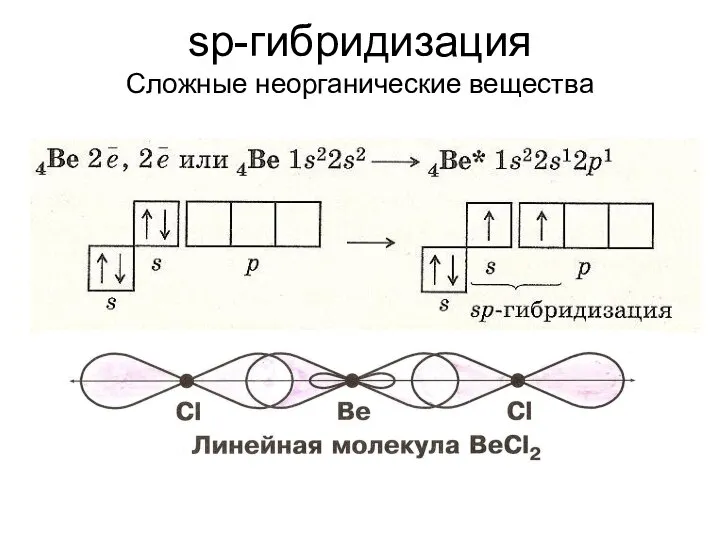
- 49. sp-гибридизация Сложные неорганические вещества
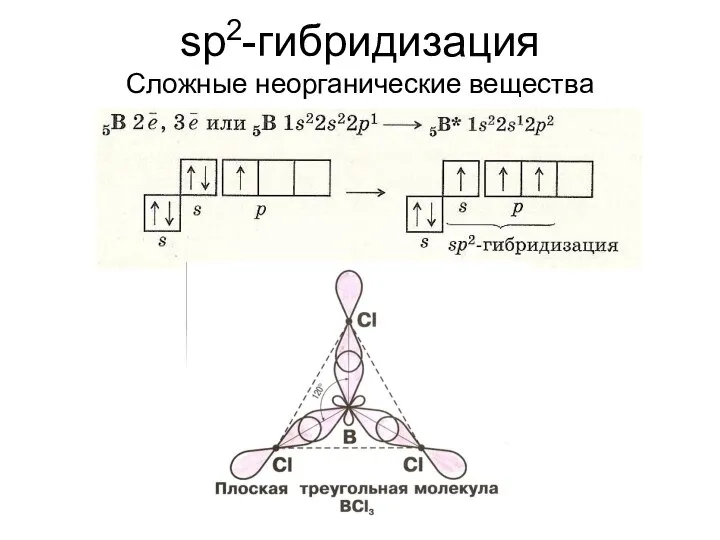
- 50. sp2-гибридизация Сложные неорганические вещества
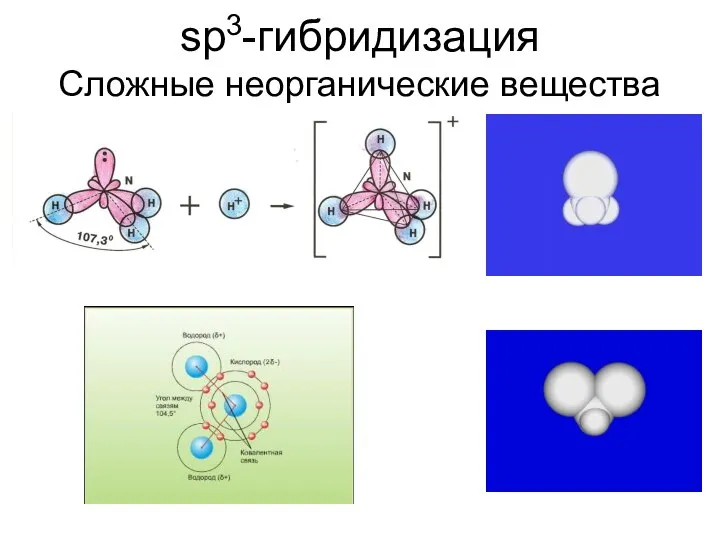
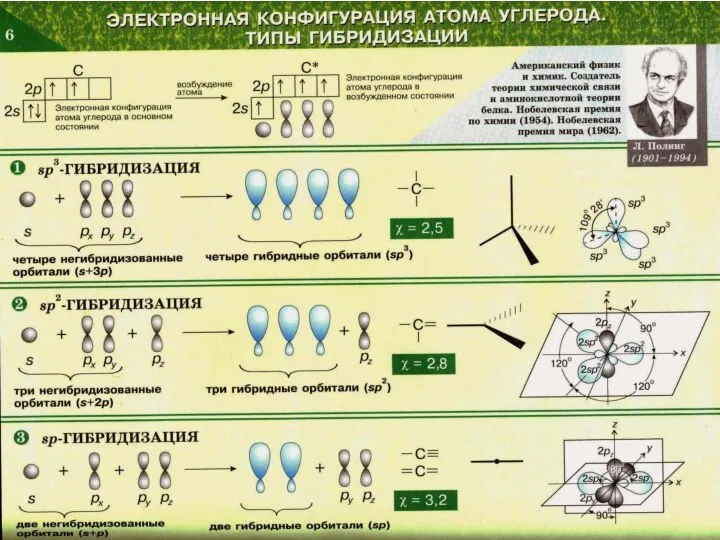
- 51. sp3-гибридизация Сложные неорганические вещества
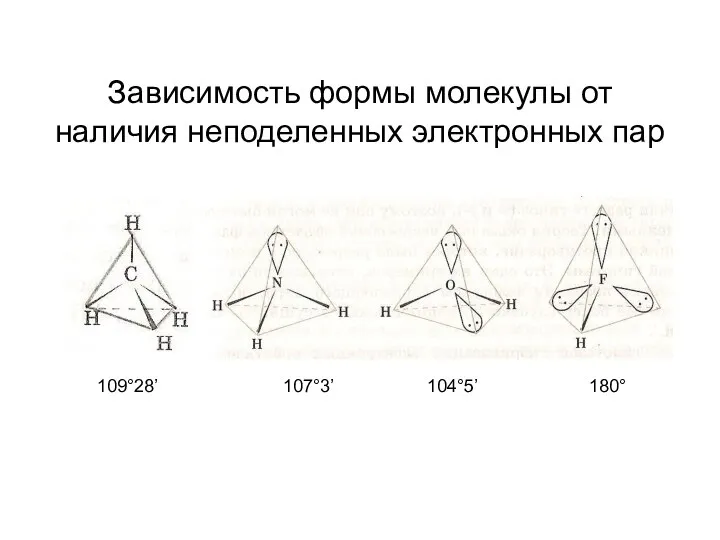
- 52. Зависимость формы молекулы от наличия неподеленных электронных пар 109°28’ 107°3’ 104°5’ 180°
- 68. Скачать презентацию



























 Предмет термодинамики
Предмет термодинамики Задачи по химии
Задачи по химии Решение задач по химической формуле 9 класс
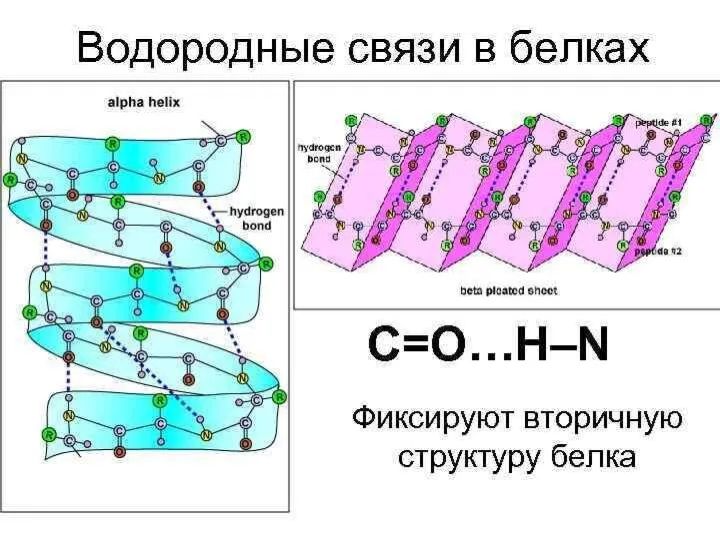
Решение задач по химической формуле 9 класс Белки простые и сложные
Белки простые и сложные Классификация моторных масел по стандартам API
Классификация моторных масел по стандартам API Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Цветные сплавы
Цветные сплавы Реакции окисления и восстановления биоорганических соединений. (Лекция 5)
Реакции окисления и восстановления биоорганических соединений. (Лекция 5) Азот и фосфор
Азот и фосфор Презентация по химии «Гормоны» Подготовила: ученица 10а класса МОУ СОШ №3 г. Светлого Калининградской области Иванова Д
Презентация по химии «Гормоны» Подготовила: ученица 10а класса МОУ СОШ №3 г. Светлого Калининградской области Иванова Д Цель и задачи дисциплины. Значение биохимии. (Тема 1)
Цель и задачи дисциплины. Значение биохимии. (Тема 1) Азот и фосфор
Азот и фосфор Таблица Менделеева
Таблица Менделеева Электрохимические методы. Потенциометрический анализ объектов окружающей среды
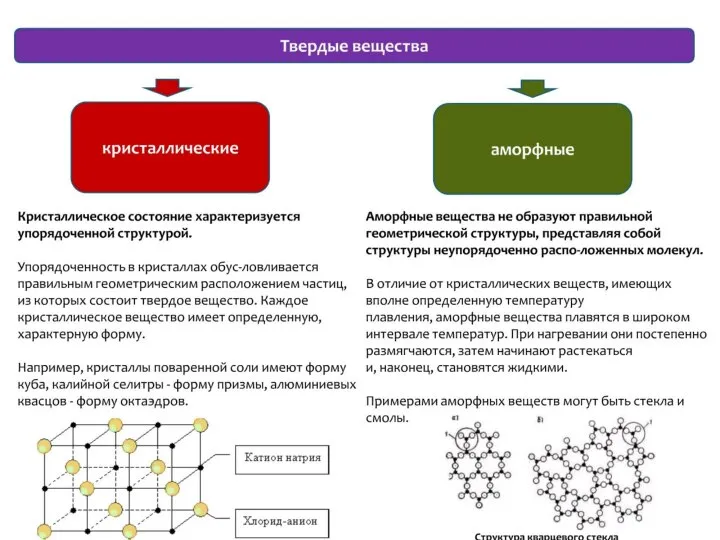
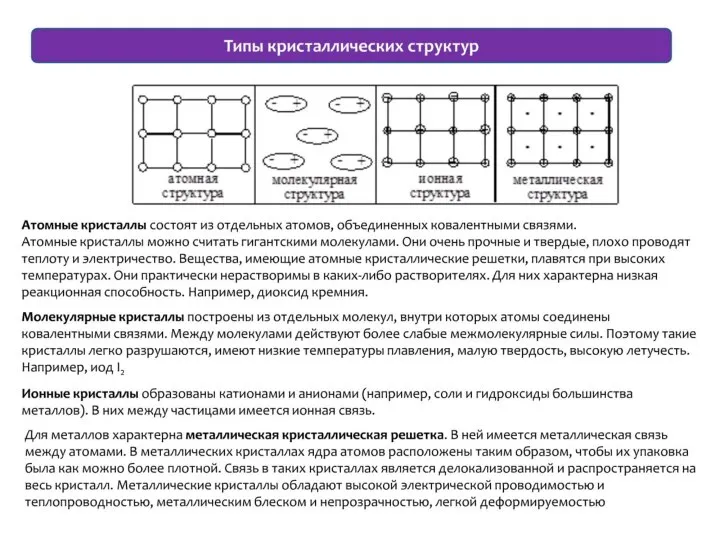
Электрохимические методы. Потенциометрический анализ объектов окружающей среды Презентация по Химии "Презентация Кристаллическая решетка" - скачать смотреть
Презентация по Химии "Презентация Кристаллическая решетка" - скачать смотреть  Лекция 7.04 - к
Лекция 7.04 - к Роль хімії у повсякденному житті
Роль хімії у повсякденному житті  Кристалічні тіла
Кристалічні тіла Электрохимия. Понятие о двойном электрическом слое (ДЭС)
Электрохимия. Понятие о двойном электрическом слое (ДЭС) Полісахариди харчових продуктів і їх властивості. Лекція 4
Полісахариди харчових продуктів і їх властивості. Лекція 4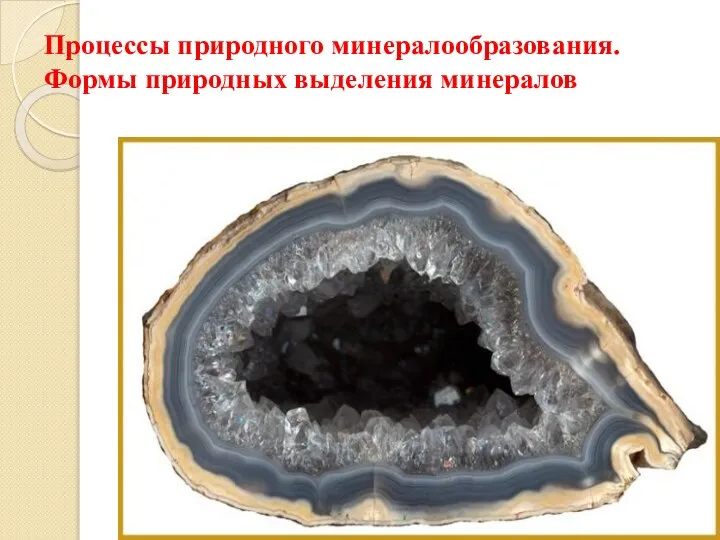 Процессы природного минералообразования. Формы природных выделений минералов
Процессы природного минералообразования. Формы природных выделений минералов Бензол. Получение бензола. Химические свойства бензола. Применение бензола на основе его свойств
Бензол. Получение бензола. Химические свойства бензола. Применение бензола на основе его свойств Урок в 8 классе
Урок в 8 классе Задача №7. По щам! Команда Карбораны
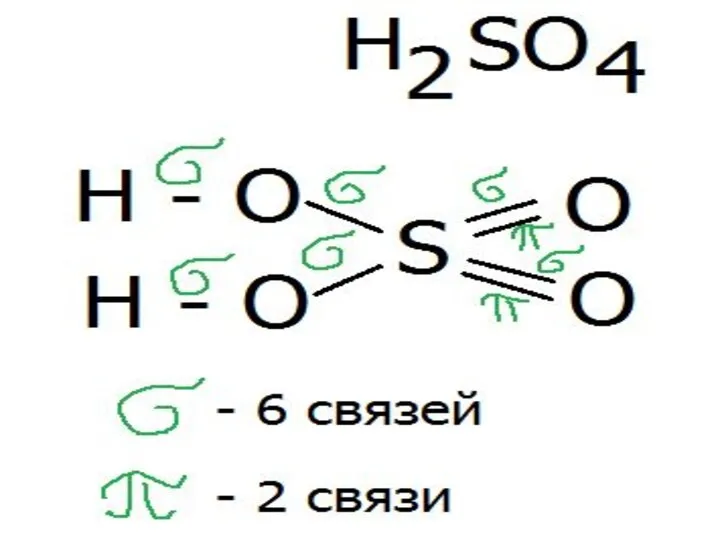
Задача №7. По щам! Команда Карбораны Производство серной кислоты H2SO4 « Едва найдется другое, искусственно добываемое вещество, столь часто применяемое в технике, к
Производство серной кислоты H2SO4 « Едва найдется другое, искусственно добываемое вещество, столь часто применяемое в технике, к Окислительно-восстановительные реакции. Химическое равновесие
Окислительно-восстановительные реакции. Химическое равновесие Методы определения основных групп токсических веществ. Этапы химико-токсикологического анализа
Методы определения основных групп токсических веществ. Этапы химико-токсикологического анализа Коррозия металлов
Коррозия металлов