Содержание
- 2. Цель : сформировать представления о свойствах углерода, уметь составлять схемы строения атома, аллотропии и его биологической
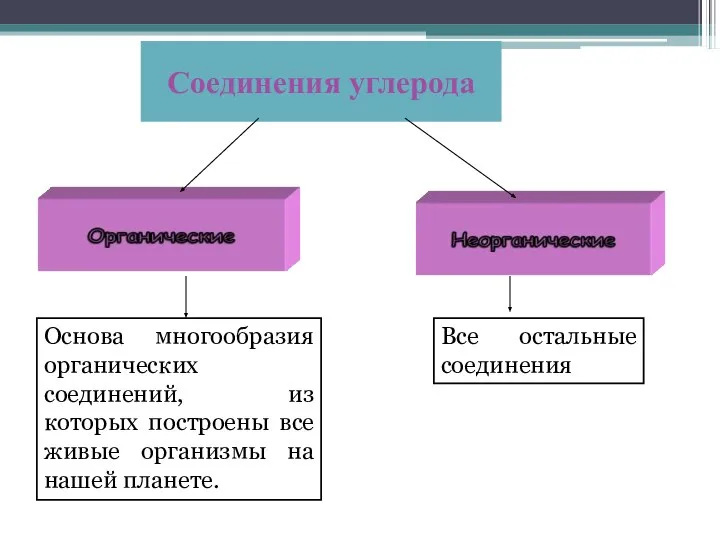
- 3. Соединения углерода Основа многообразия органических соединений, из которых построены все живые организмы на нашей планете. Все
- 4. Строение атома Углерод (Carboneum-рождающий уголь) Химический элемент IV группы периодической системы Менделеева-неметалл Атомный номер 6 На
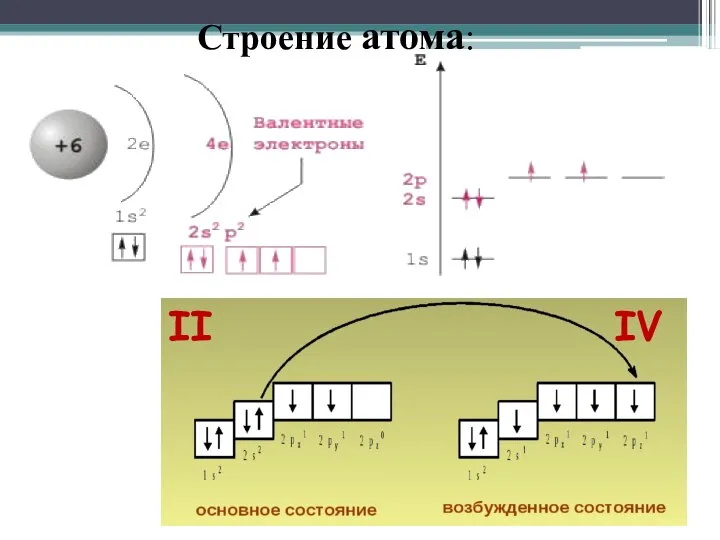
- 5. Строение атома: II IV
- 6. Степени окисления атома углерода в соединениях: -4 (SiC, CH4, Al4C3) +2 (CO) +4 (CO2 , CCl4
- 7. Нахождение углерода в природе. 11 место по распространенности в природе. 4 место на Солнце ( Н2,
- 8. АЛЛОТРОПИЯ - способность атомов одного химического элемента образовывать несколько простых веществ. ?
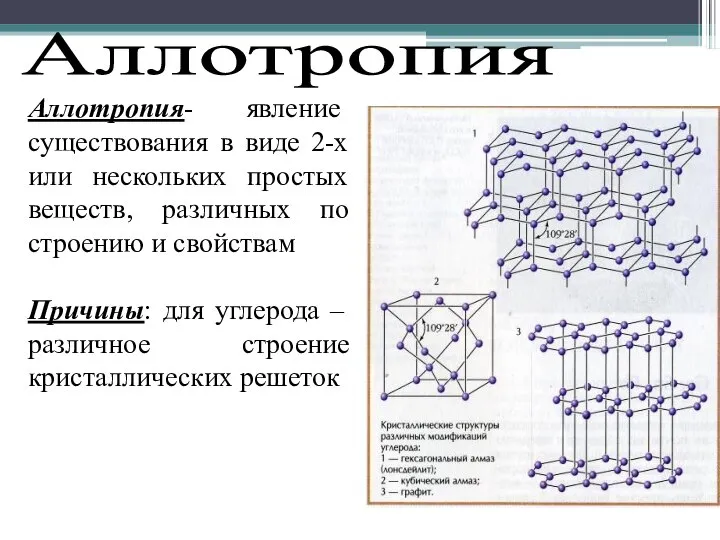
- 9. Аллотропия Аллотропия- явление существования в виде 2-х или нескольких простых веществ, различных по строению и свойствам
- 10. Простое вещество углерод. Аллотропные модификации углерода: алмаз графит лонсдейлит карбин фуллерены графен
- 11. Алмаз (adamas – непреклонный, твердый) кристаллическая решетка – атомная; каждый атом находится в вершинах тетраэдра; прозрачный,
- 12. Алмаз – бесцветное, прозрачное, сильно преломляющее свет вещество. Алмаз тверже всех найденных в природе веществ, но
- 13. Графит (grapho – пишу) кристаллическая решетка - атомная серо-черная, непрозрачная, жирная на ощупь, чешуйчатая, очень мягкая
- 14. Графит – устойчивая при нормальных условиях аллотропная модификация углерода, имеет серо-черный цвет и металлический блеск, кажется
- 15. Взаимные превращения аллотропных модификаций углерода. уголь ⭢ графит (2600˚С, давление⭡) графит ⭢ алмаз (1200МПа, 1500˚С) алмаз
- 16. Карбин мелкокристаллический порошок черного цвета; по твердости между алмазом и графитом; длинные цепочки атомов углерода, уложенные
- 17. Фуллерены получают испарением графита при высокой температуре при действии лазерного излучения в атмосфере гелия; построены из
- 18. Аморфный углерод Каменный и древесный уголь, кокс, сажа. плотность, теплоемкость, теплопроводность и электропроводность выше, чем графита.
- 19. Аморфный углерод Активированный уголь - пористое вещество, которое получают из различных углеродсодержащих материалов органического происхождения: древесный
- 20. Адсорбция (ad — на, при; sorbeo — поглощаю) Это свойство углерода удерживать на пористой поверхности растворенные
- 21. Адсорбция Так же адсорбция применяется в медицине, химической, фармацевтической и пищевой промышленностях
- 22. Химические свойства углерода Восстановительные свойства. Записать уравнения реакций взаимодействия углерода 1) с фтором , 2) с
- 23. Химические свойства углерода Углерод вступает в реакции с солями кислородсодержащих кислот, связывая кислород: BaSO4 + C
- 24. Химические свойства углерода Окислительные свойства. Записать реакции взаимодействия углерода 1) с металлами (Аl), 2) с водородом
- 25. Реакции диспропорционирования: При нагревании с оксидами активных металлов: СаО + 3С = СаС2 + СО 2Аl2О3
- 26. Химические свойства углерода При нагревании углерод соединяется с кислородом, образуя оксид углерода (IV), или углекислый газ:
- 27. Химические свойства углерода Углерод — сильный восстановитель. При нагревании с водяным паром он вытесняет из воды
- 28. С сталь сельское хозяйство топливо медицина типография ювелирные изделия адсорбент резина крем обуви Применение
- 30. Домашняя работа Составить схемы электронного баланса следующих реакций: Ca + 2C = CaC2 4A1 + 3C
- 31. Какие утверждения верны: Углерод содержится и в воздухе, и в земной коре, в болоте и в
- 33. Скачать презентацию


























 Бионеорганическая химия. Жидкие среды организма. (Лекция 2)
Бионеорганическая химия. Жидкие среды организма. (Лекция 2) Ароматичні речовини
Ароматичні речовини Коллигативные свойства растворов
Коллигативные свойства растворов Метаморфические горные породы
Метаморфические горные породы Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Chimie bioorganique
Chimie bioorganique Современные области применения изотопной продукции
Современные области применения изотопной продукции Дгебуадзе Загра Омардибировна, учитель химии, МОУ «СОШ № 14 г.Зеленокумска» Ставропольский край
Дгебуадзе Загра Омардибировна, учитель химии, МОУ «СОШ № 14 г.Зеленокумска» Ставропольский край  Хроматография. Классификации хроматографических методов
Хроматография. Классификации хроматографических методов Нуклеирующие добавки
Нуклеирующие добавки Газ тәрізді диэлектриктер. Пропан
Газ тәрізді диэлектриктер. Пропан Короткі відомості з історії хімії. Становлення хімії як науки
Короткі відомості з історії хімії. Становлення хімії як науки Массообменные процессы
Массообменные процессы Секреты химии. Проект Радуга
Секреты химии. Проект Радуга Галогены
Галогены Презентация по Химии "Гидролиз солей" - скачать смотреть бесплатно
Презентация по Химии "Гидролиз солей" - скачать смотреть бесплатно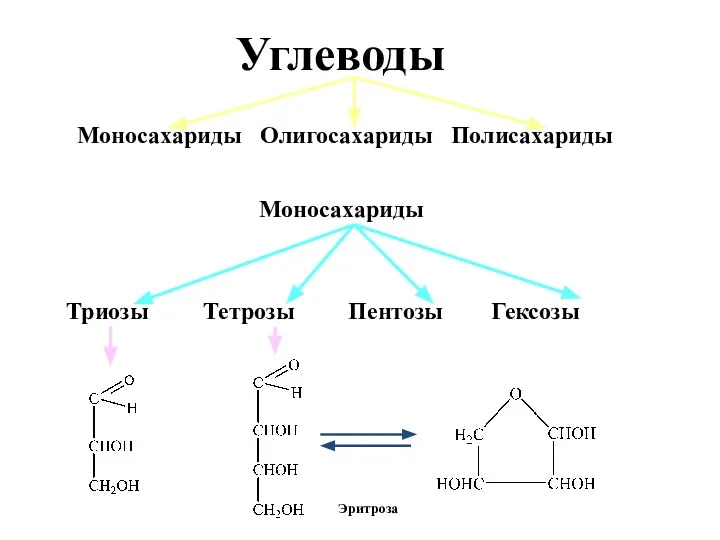 Углеводы. Моносахариды. Олигосахариды. Полисахариды
Углеводы. Моносахариды. Олигосахариды. Полисахариды Химия и сельское хозяйство
Химия и сельское хозяйство Изучение влияния азотсодержащих удобрений на качество продукции по содержанию нитратов
Изучение влияния азотсодержащих удобрений на качество продукции по содержанию нитратов Презентация по Химии "ВЛИЯНИЕ ГАЗИРОВАННЫХ НАПИТКОВ НА ОРГАНИЗМ ЧЕЛОВЕКА" - скачать смотреть
Презентация по Химии "ВЛИЯНИЕ ГАЗИРОВАННЫХ НАПИТКОВ НА ОРГАНИЗМ ЧЕЛОВЕКА" - скачать смотреть  Природные источники углеводородов и их переработка
Природные источники углеводородов и их переработка Уголь активированный
Уголь активированный Гетероциклические соединения
Гетероциклические соединения Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы
Металдар. металдардың периодтық жүйедегі орны. Металдардың құрылысы Ферменты. Уравнение Михаэлиса-Ментен
Ферменты. Уравнение Михаэлиса-Ментен МЫЛО
МЫЛО Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений
Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений 2_Galogenovodorody
2_Galogenovodorody