Содержание
- 2. УГЛЕВОДЫ Cn(H2O)m Классификация: моносахариды (монозы), олигосахариды (от 2 до 10 остатков моноз), полисахариды (более 10 остатков
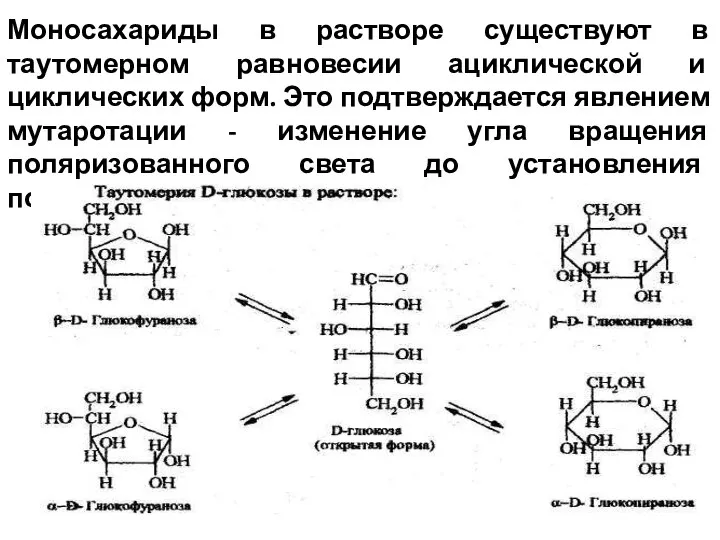
- 3. Моносахариды в растворе существуют в таутомерном равновесии ациклической и циклических форм. Это подтверждается явлением мутаротации -
- 4. В медицинской и фармацевтической практике применяют глюкозу, сахар молочный, сахарозу и крахмал. Крахмал (C6H10O5)x. Молекула крахмала
- 5. Получение 1. Сахарозу получают из сахарной свеклы или сахарного тростника. 2. Глюкоза находится в виноградном соке,
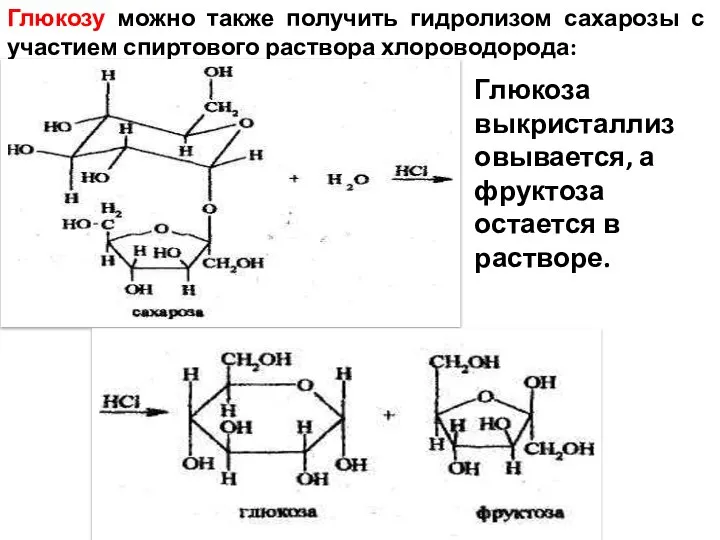
- 6. Глюкозу можно также получить гидролизом сахарозы с участием спиртового раствора хлороводорода: Глюкоза выкристаллизовывается, а фруктоза остается
- 7. Растворимость Глюкоза, сахар молочный и сахароза - растворимы в воде, очень мало или трудно растворимы в
- 8. Для качественного и количественного анализа используют главным образом восстановительные свойства углеводов и физические свойства их растворов.
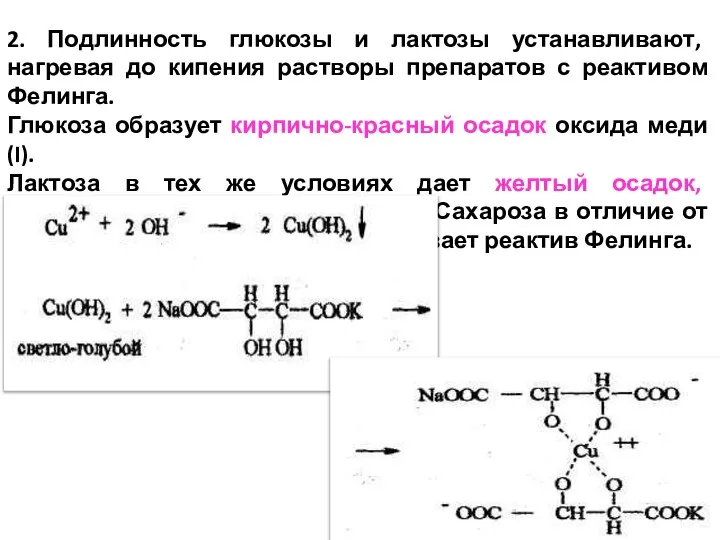
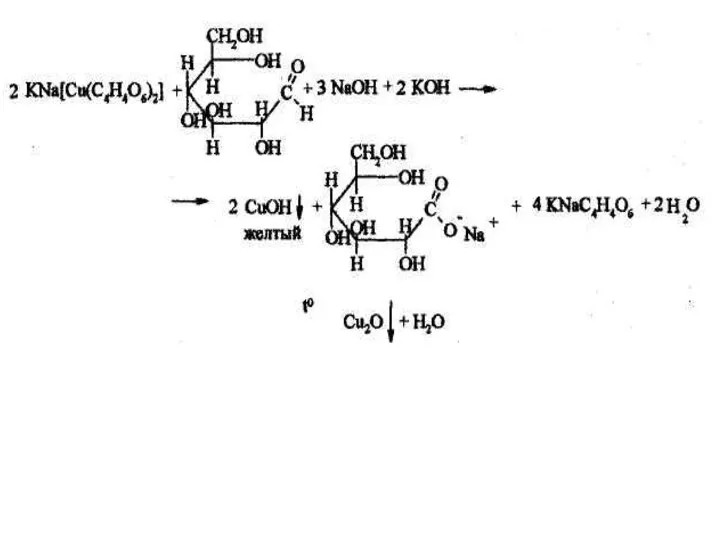
- 9. 2. Подлинность глюкозы и лактозы устанавливают, нагревая до кипения растворы препаратов с реактивом Фелинга. Глюкоза образует
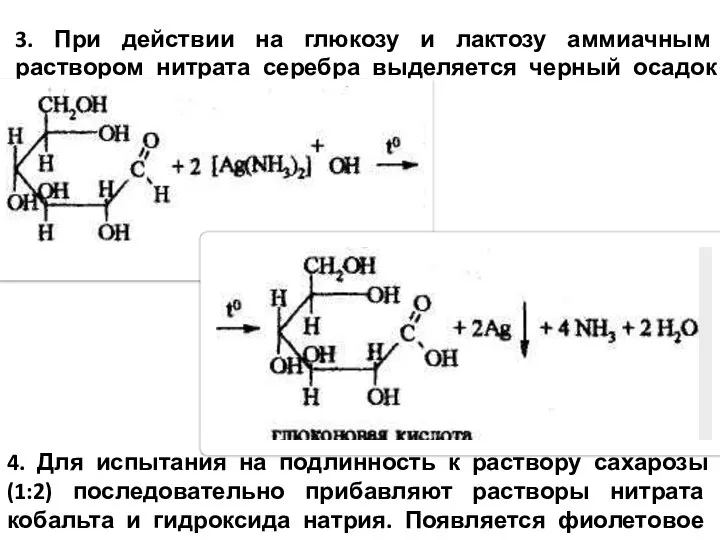
- 11. 3. При действии на глюкозу и лактозу аммиачным раствором нитрата серебра выделяется черный осадок серебра. 4.
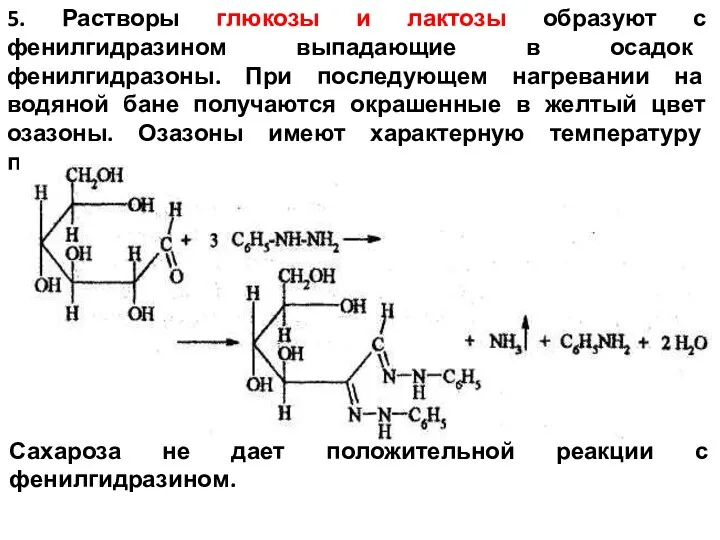
- 12. 5. Растворы глюкозы и лактозы образуют с фенилгидразином выпадающие в осадок фенилгидразоны. При последующем нагревании на
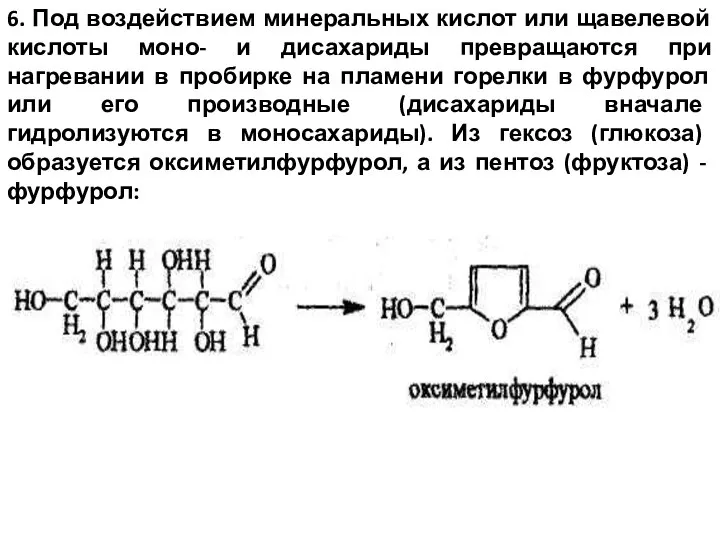
- 13. 6. Под воздействием минеральных кислот или щавелевой кислоты моно- и дисахариды превращаются при нагревании в пробирке
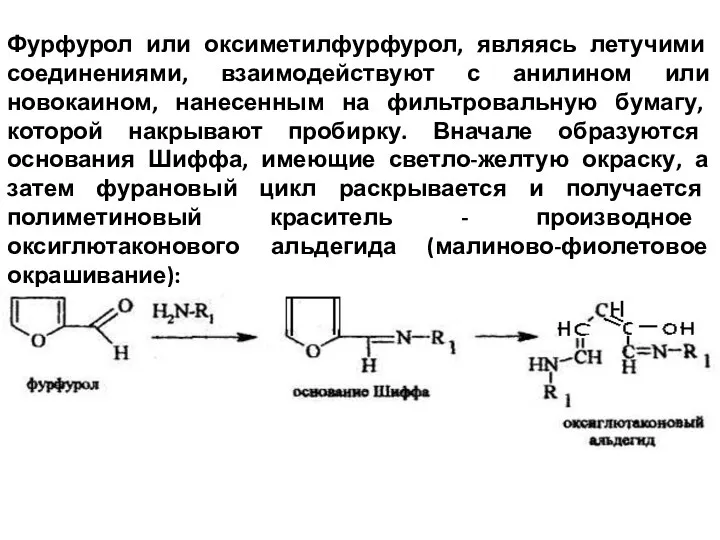
- 14. Фурфурол или оксиметилфурфурол, являясь летучими соединениями, взаимодействуют с анилином или новокаином, нанесенным на фильтровальную бумагу, которой
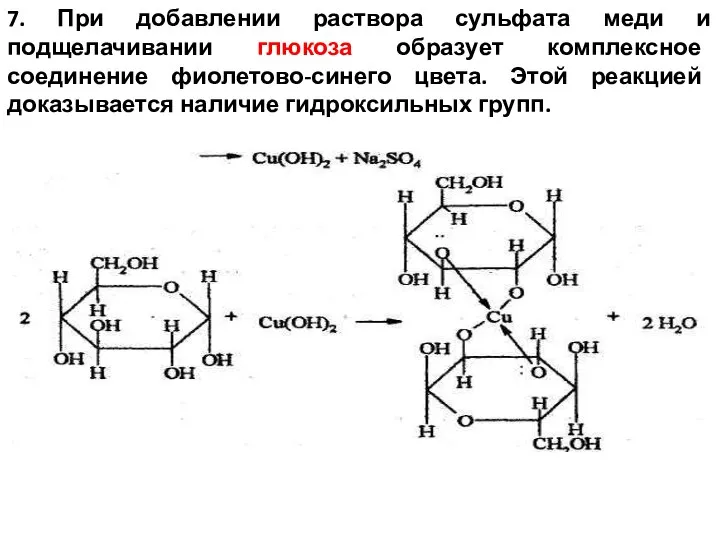
- 15. 7. При добавлении раствора сульфата меди и подщелачивании глюкоза образует комплексное соединение фиолетово-синего цвета. Этой реакцией
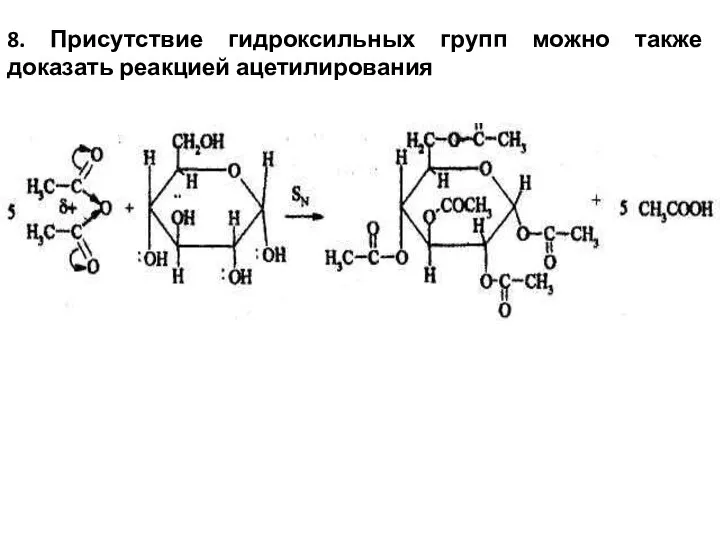
- 16. 8. Присутствие гидроксильных групп можно также доказать реакцией ацетилирования
- 17. 9. Определение подлинности крахмала проводят: при вливании в 100 мл кипящей воды при постоянном перемешивании смеси
- 18. В лактозе определяют следующие примеси: хлориды (не более 0,004%), сульфаты (не более 0,02%), кальций (не более
- 19. В сахарозе не должно быть: тяжелых металлов, хлоридов, сульфатов, кальция, бария, стронция, инвертированного сахара и других
- 20. Сахара можно определять поляриметрическим методом. Поляриметрический метод определения сахаров основан на измерении угла вращения поляризованного луча.
- 21. Карбоновые кислоты Карбоновые кислоты - это соединения, содержащие карбоксильную группу - СООН. монокарбоновые, или одноосновные, дикарбоновые,
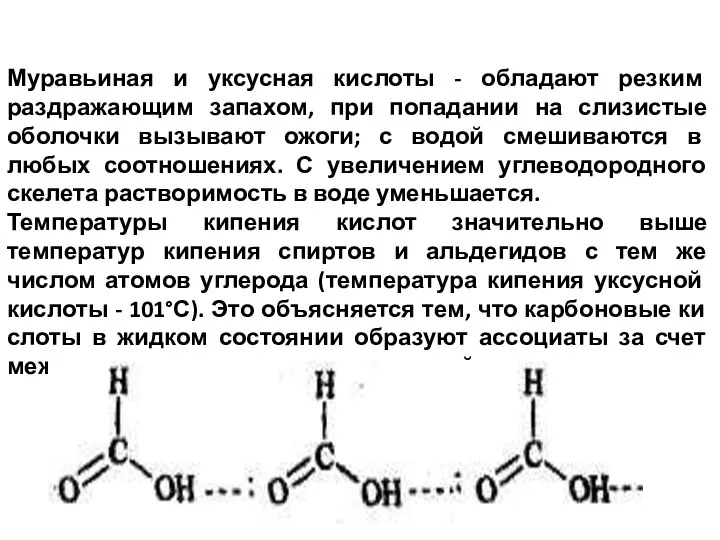
- 22. Муравьиная и уксусная кислоты - обладают резким раздражающим запахом, при попадании на слизистые оболочки вызывают ожоги;
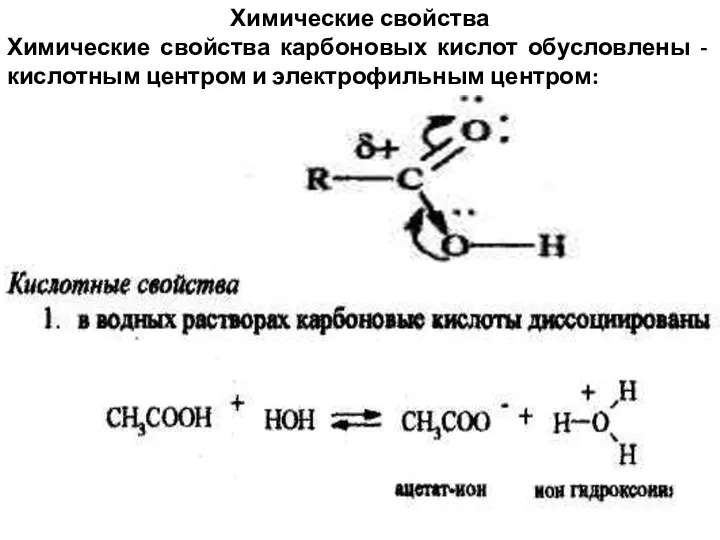
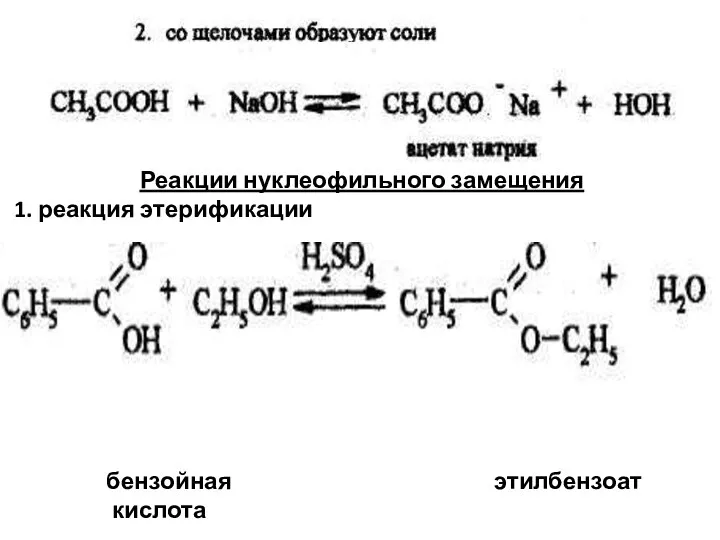
- 23. Химические свойства Химические свойства карбоновых кислот обусловлены - кислотным центром и электрофильным центром:
- 24. Реакции нуклеофильного замещения 1. реакция этерификации бензойная этилбензоат кислота
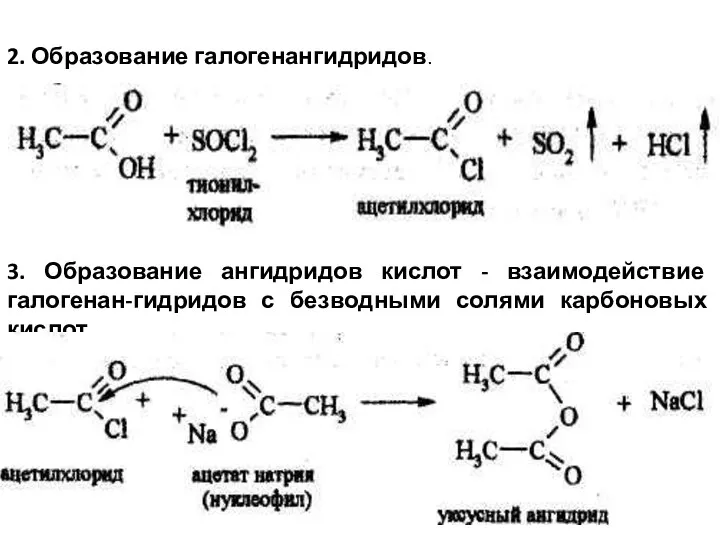
- 25. 2. Образование галогенангидридов. 3. Образование ангидридов кислот - взаимодействие галогенан-гидридов с безводными солями карбоновых кислот.
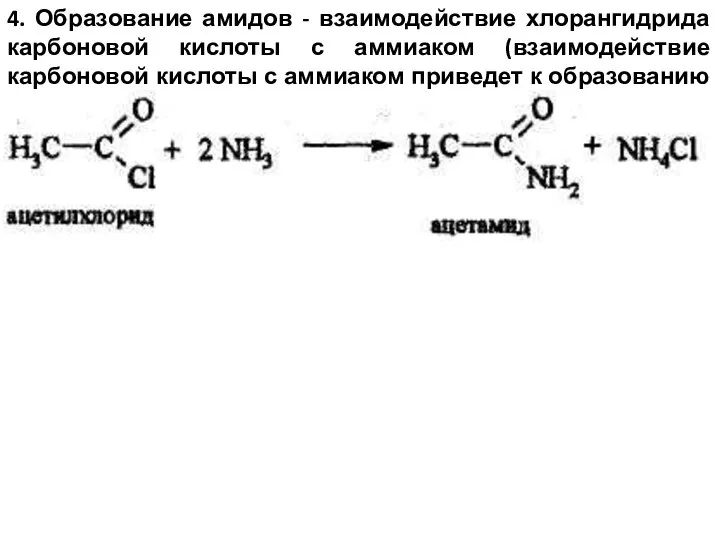
- 26. 4. Образование амидов - взаимодействие хлорангидрида карбоновой кислоты с аммиаком (взаимодействие карбоновой кислоты с аммиаком приведет
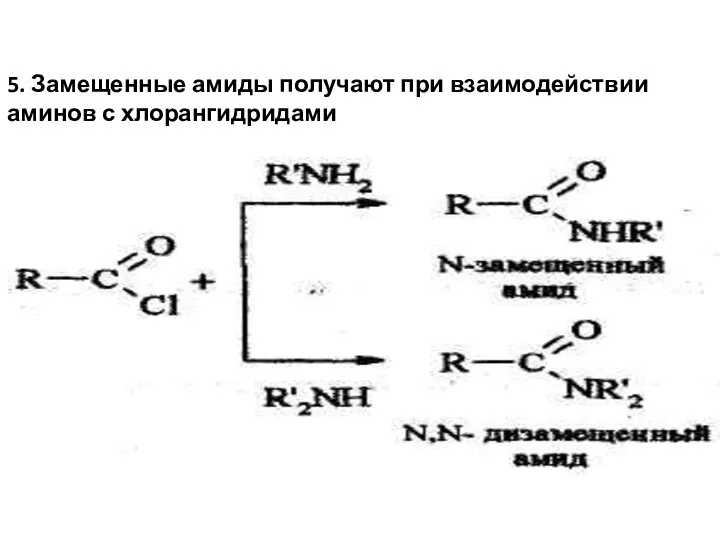
- 27. 5. Замещенные амиды получают при взаимодействии аминов с хлорангидридами
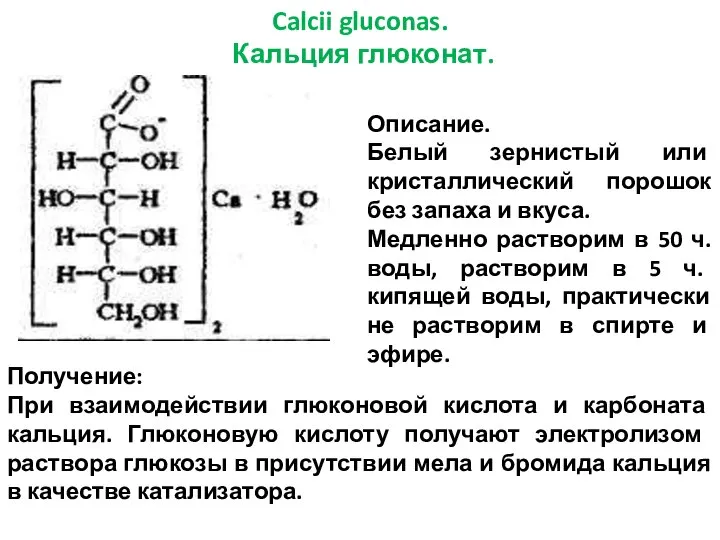
- 28. Calcii gluconas. Кальция глюконат. Описание. Белый зернистый или кристаллический порошок без запаха и вкуса. Медленно растворим
- 29. Чистота Определяют прозрачность, кислотность или щелочность (раствор должен быть нейтральным), хлориды, сульфаты, тяжелые металлы, мышьяк, декстрин,
- 30. Калия ацетат. Описание. Белый кристаллический порошок со слабым специфическим запахом уксусной кислоты, солоноватый вкус. Гигроскопичен и
- 31. Подлинность. К+ Реакции на ацетат – ион CH3COOK + C2H5OH + H2SO4 = CH3COOC2H5 + K2SO4
- 32. Чистота Определяют хлориды, сульфаты, кальций, железо, тяжелые металлы, восстанавливающие вещества, щелочность. Восстанавливающие вещества являются недопустимой примесью.
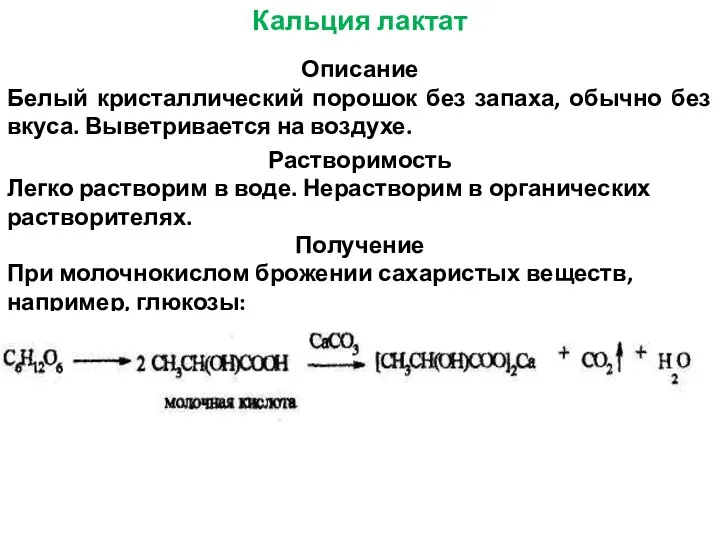
- 33. Кальция лактат Описание Белый кристаллический порошок без запаха, обычно без вкуса. Выветривается на воздухе. Растворимость Легко
- 34. Подлинность. 1) Ca2+ 2) Реакция на лактат - ион При действии окислителя, например раствора КМпО4 в
- 35. Чистота Определяют щелочность или кислотность, нерастворимые примеси, хлориды, сульфаты, железо, тяжелые металлы, мышьяк, потерю в весе
- 36. Натрия цитрат. Описание. Белый кристаллический порошок без запаха, солоноватый вкус. Выветриваются на воздухе. Растворимость. Легко растворим
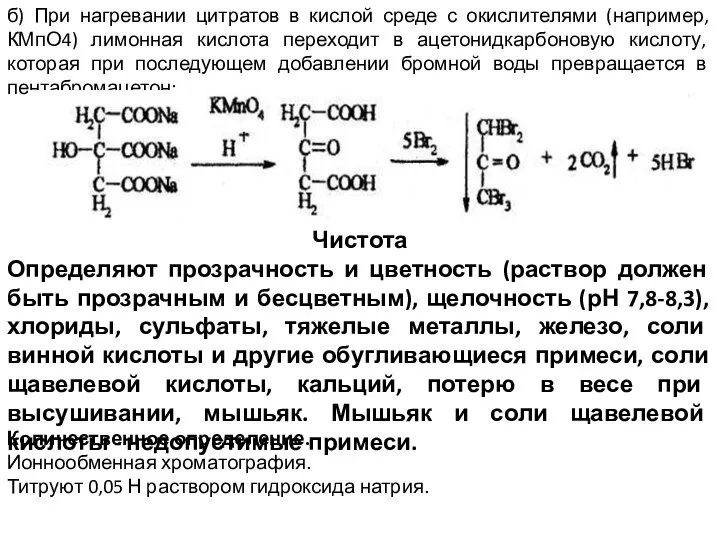
- 37. б) При нагревании цитратов в кислой среде с окислителями (например, КМпО4) лимонная кислота переходит в ацетонидкарбоновую
- 38. Применение: Натрия цитрат - для консервации (предотвращает свертывание крови). Хранение. В хорошо укупоренной таре.
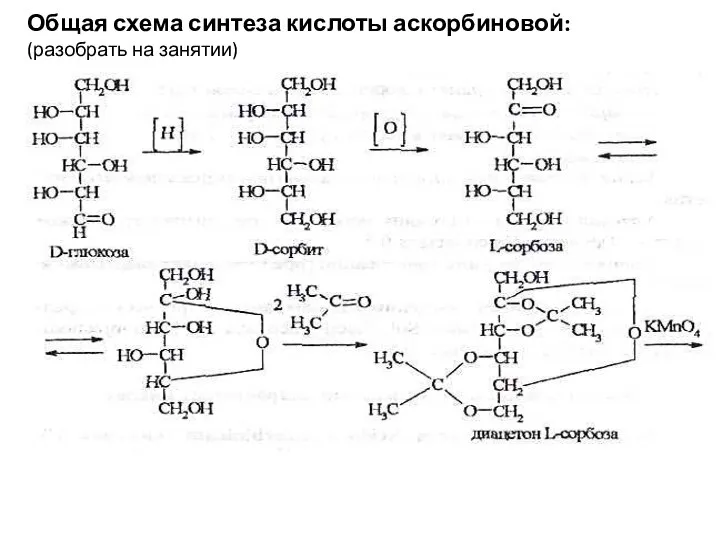
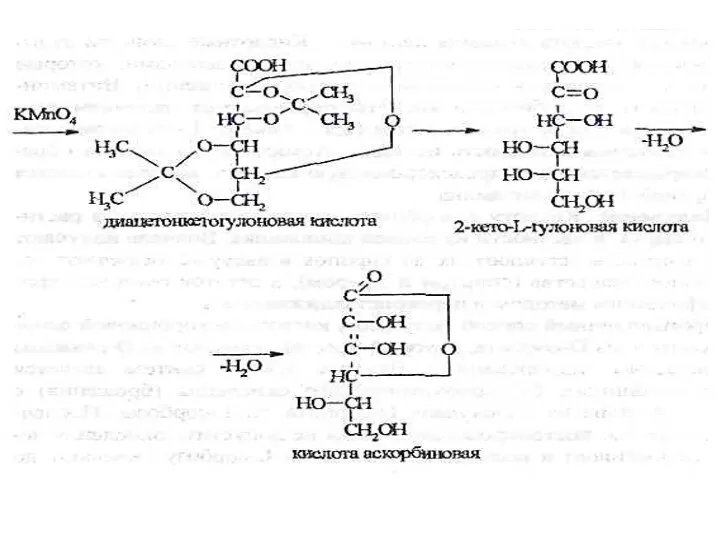
- 39. Лактоны ненасыщенных полиоксикарбоновых кислот Аскорбиновая кислота (витамин С) Acidum ascorbinicum Общая схема синтеза кислоты аскорбиновой:
- 40. Общая схема синтеза кислоты аскорбиновой: (разобрать на занятии)
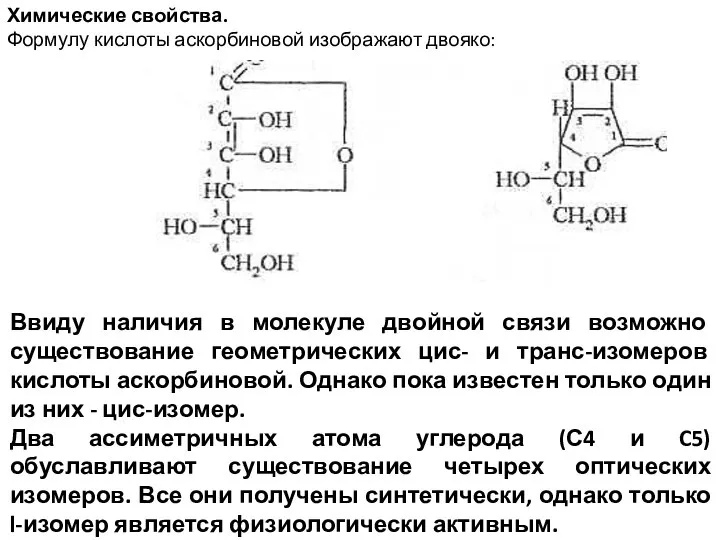
- 42. Химические свойства. Формулу кислоты аскорбиновой изображают двояко: Ввиду наличия в молекуле двойной связи возможно существование геометрических
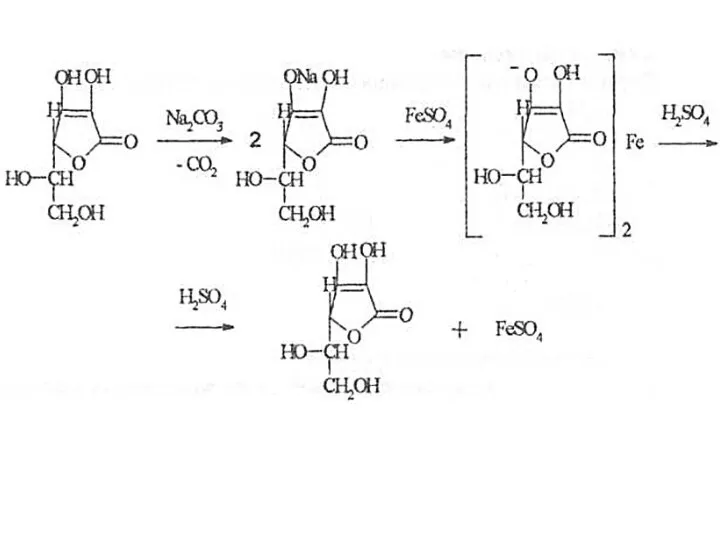
- 43. Кислота аскорбиновая - это производное полиоксикарбоновых кислот. Она проявляет восстановительные свойства за счет ендиольной группы и
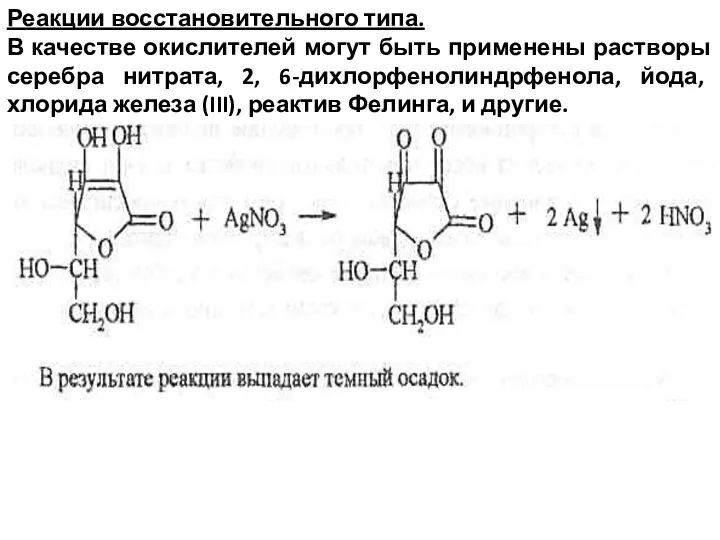
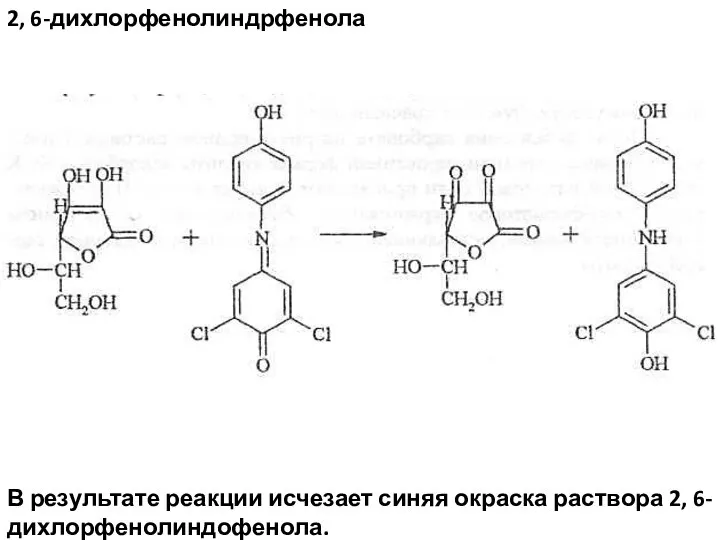
- 45. Реакции восстановительного типа. В качестве окислителей могут быть применены растворы серебра нитрата, 2, 6-дихлорфенолиндрфенола, йода, хлорида
- 46. 2, 6-дихлорфенолиндрфенола В результате реакции исчезает синяя окраска раствора 2, 6-дихлорфенолиндофенола.
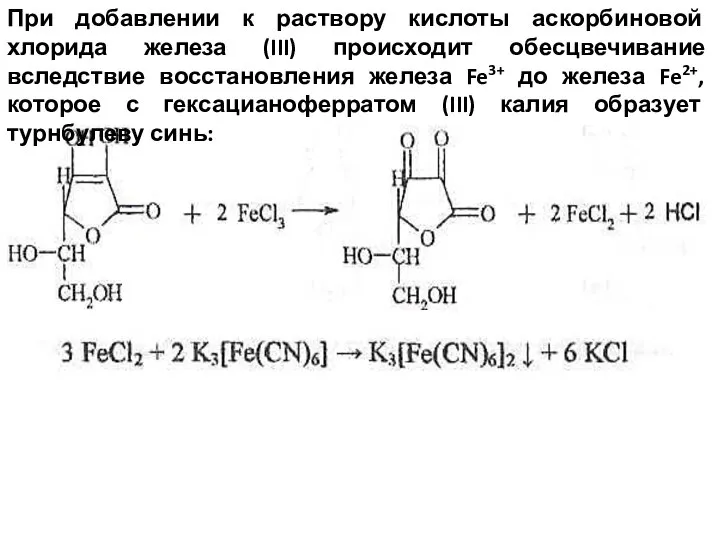
- 47. При добавлении к раствору кислоты аскорбиновой хлорида железа (III) происходит обесцвечивание вследствие восстановления железа Fe3+ до
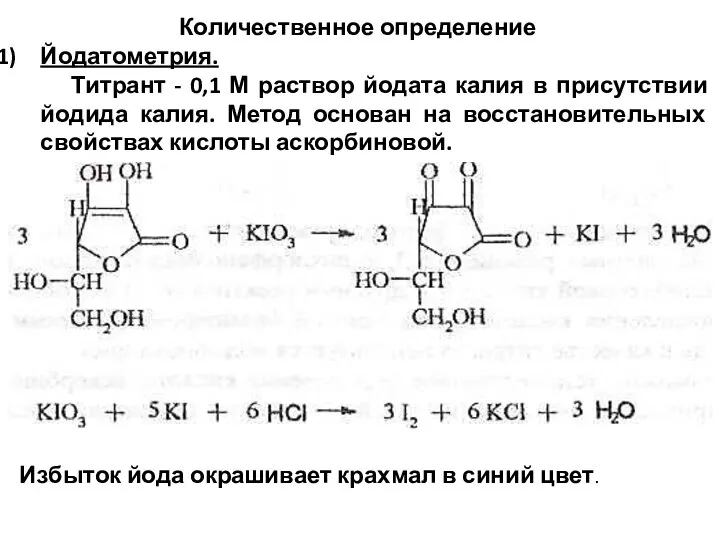
- 48. Избыток йода окрашивает крахмал в синий цвет. Количественное определение Йодатометрия. Титрант - 0,1 М раствор йодата
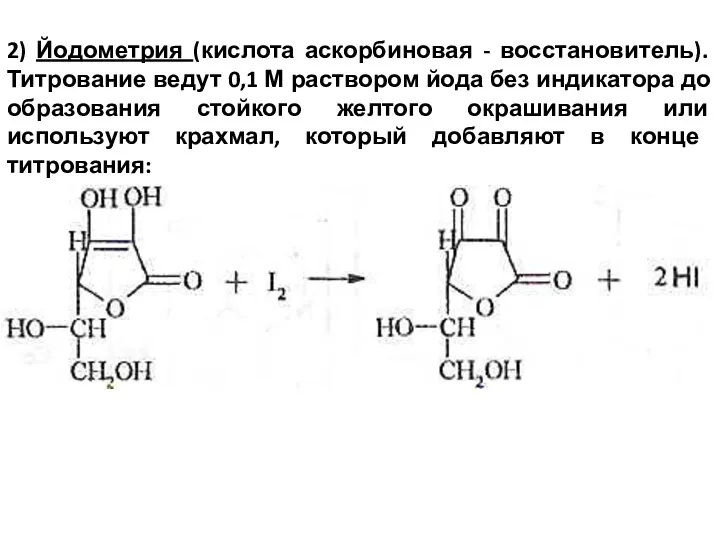
- 49. 2) Йодометрия (кислота аскорбиновая - восстановитель). Титрование ведут 0,1 М раствором йода без индикатора до образования
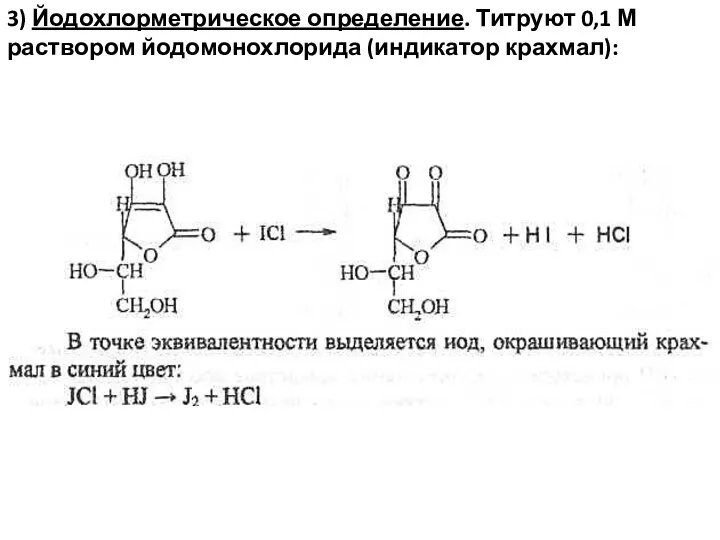
- 50. 3) Йодохлорметрическое определение. Титруют 0,1 М раствором йодомонохлорида (индикатор крахмал):
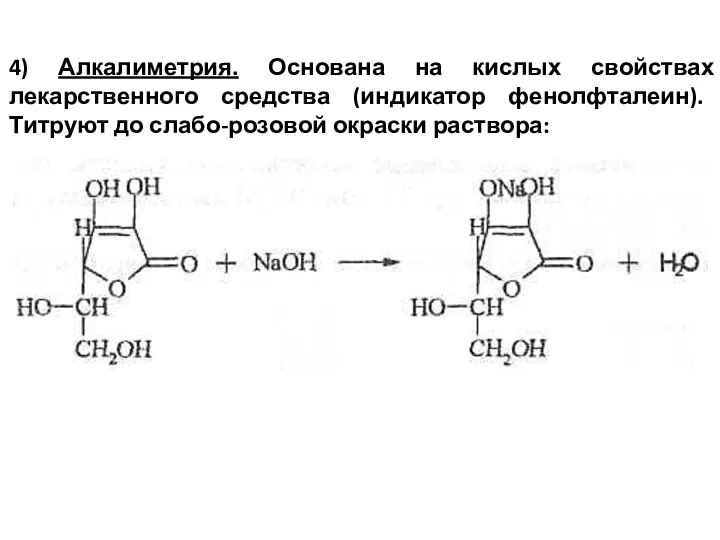
- 51. 4) Алкалиметрия. Основана на кислых свойствах лекарственного средства (индикатор фенолфталеин). Титруют до слабо-розовой окраски раствора:
- 52. 5) Фотоколориметрический способ, основан на цветных реакциях с 2, 6-дихлорфенолиндофенолом, фосфорномолибденовой кислотой и другими реактивами. 6)
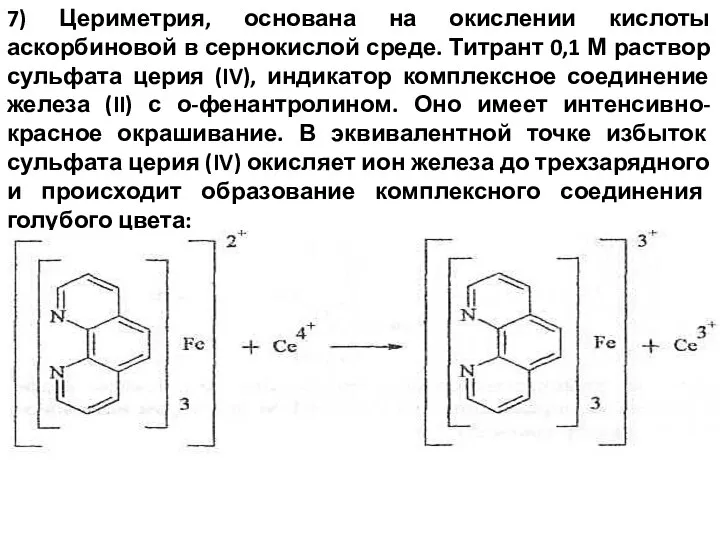
- 53. 7) Цериметрия, основана на окислении кислоты аскорбиновой в сернокислой среде. Титрант 0,1 М раствор сульфата церия
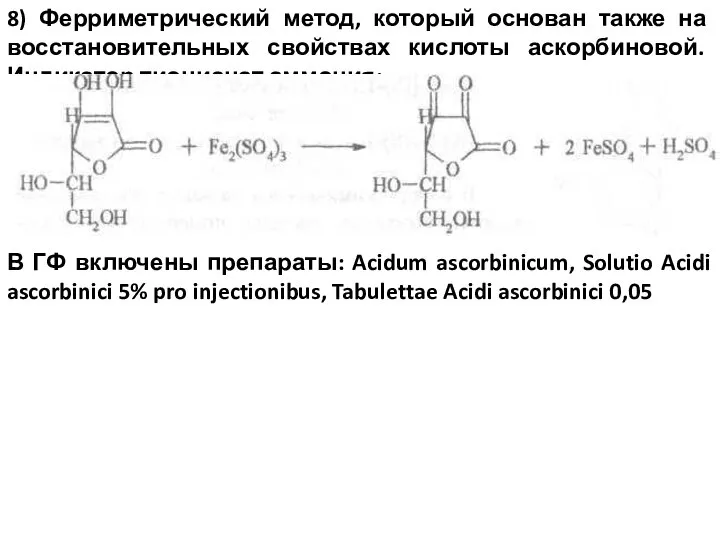
- 54. 8) Ферриметрический метод, который основан также на восстановительных свойствах кислоты аскорбиновой. Индикатор тиоцианат аммония: В ГФ
- 55. Подлинность. При добавлении к раствору препарата раствора нитрата серебра образуется темный осадок. При добавлении к раствору
- 56. Раствор аскорбиновой кислоты для инъекций содержит изотонирующие и стабилизирующие вещества (натрия гидрокарбонат, натрия метабисульфит, натрия сульфит
- 57. Играет важную роль в регулировании окислительно-восстановительных процессов, углеводного обмена, свертываемости крови, регенерации ткани. Благодаря наличию в
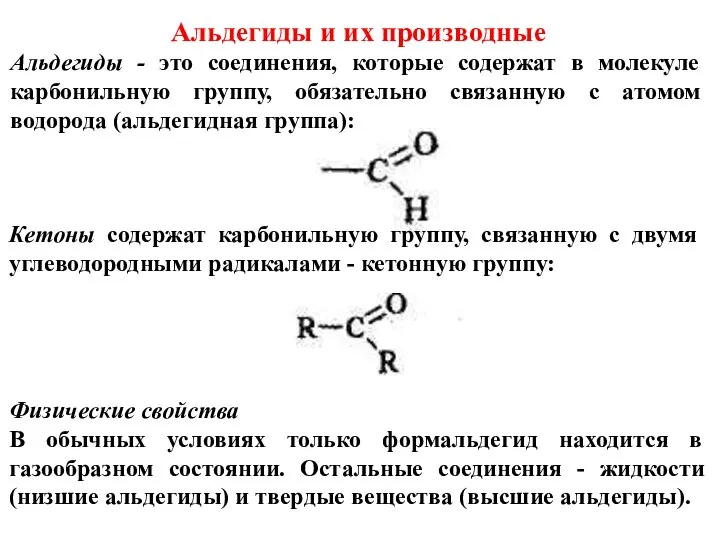
- 58. Альдегиды и их производные Альдегиды - это соединения, которые содержат в молекуле карбонильную группу, обязательно связанную
- 59. У альдегидов сохраняются наркотические свойства, присущие спиртам. Они обладают также дезинфицирующими свойствами. Удлинение цепочки R приводит
- 60. Раствор формальдегида (Solutio Formaldehydi, Formalinum) Получение. Описание. Прозрачная бесцветная жидкость своеобразного острого запаха. Смешивается во всех
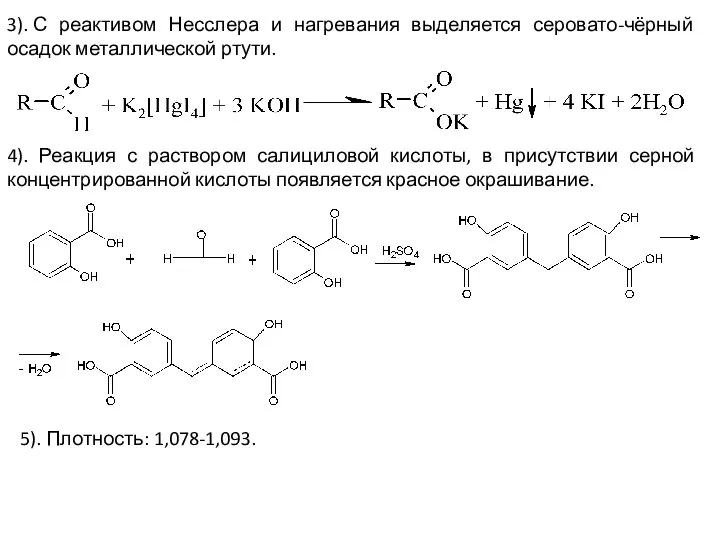
- 61. 3). С реактивом Несслера и нагревания выделяется серовато-чёрный осадок металлической ртути. 4). Реакция с раствором салициловой
- 62. Количественное определение. Обратная йодометрия в присутствии щёлочи, первый рабочий раствор-раствор йода, второй –натрия тиосульфат, индикатор крахмал.
- 63. Метенамин (Hexamethylentetraminum, Urotropinum, Methenaminum) Получение. Описание. Бесцветные кристаллы или белый кристаллический порошок, без запаха, жгучего и
- 64. Чистота. 1.Кислотность или щелочность: раствор препарата должен быть щелочным по лакмусу и не давать щелочной реакции
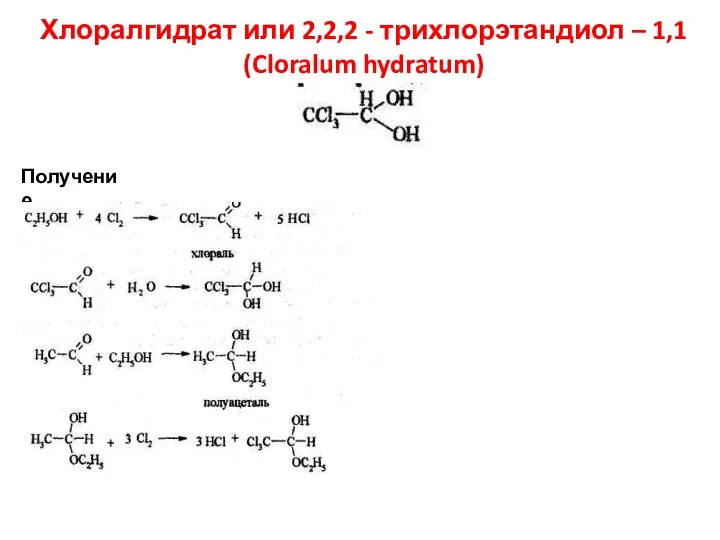
- 65. Хлоралгидрат или 2,2,2 - трихлорэтандиол – 1,1 (Cloralum hydratum) Получение.
- 66. Описание. Бесцветные прозрачные кристаллы или мелкокристаллический порошок с характерным запахом и слегка горьковатым вкусом. Гигроскопичен при
- 67. Чистота. 1.Прозрачность и цветность раствора Полученный раствор должен быть прозрачным и бесцветным. 2.Кислотность. При добавлении к
- 69. Скачать презентацию































 Презентация по Химии "Презентация Теория строения органических веществ А.М. Бутлерова" - скачать смотреть
Презентация по Химии "Презентация Теория строения органических веществ А.М. Бутлерова" - скачать смотреть  Закон постоянства состава вещества
Закон постоянства состава вещества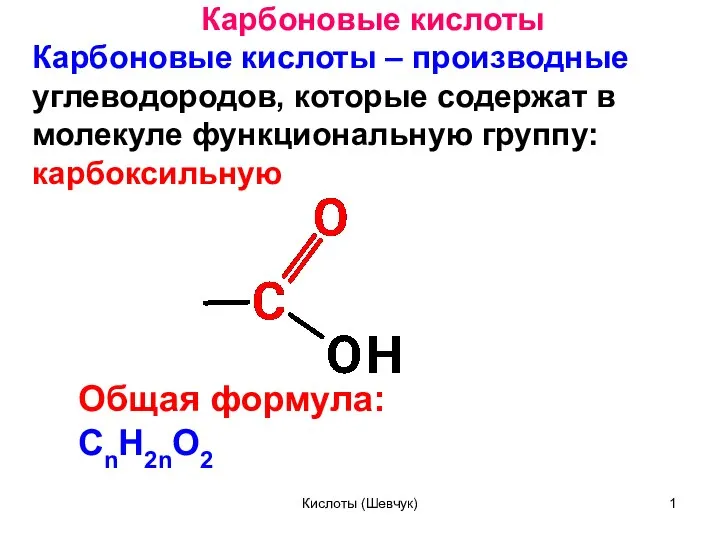 Карбоновые кислоты
Карбоновые кислоты Титан. Структура, применение, свойства (11 класс)
Титан. Структура, применение, свойства (11 класс) Современные тенденции развития химии
Современные тенденции развития химии Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразовательная школа №9 с углубленным изучением отдельн
Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразовательная школа №9 с углубленным изучением отдельн Автор учитель МОУ СОШ №3 города Волгореченска Звёздочкина С.А.
Автор учитель МОУ СОШ №3 города Волгореченска Звёздочкина С.А.  Общие свойства металлов
Общие свойства металлов Investigation of the conditions for the synthesis of a silver - containing composite
Investigation of the conditions for the synthesis of a silver - containing composite Химические реакции (11 класс)
Химические реакции (11 класс) Идеи и прогнозы Д. И. Менделеева в области улучшения плодородия почв.
Идеи и прогнозы Д. И. Менделеева в области улучшения плодородия почв. Железо. Электронное строение железа
Железо. Электронное строение железа Тепло- и массообменные процессы при синтезе Фишера-Тропша
Тепло- и массообменные процессы при синтезе Фишера-Тропша Rate of reactions. (Chapter 2)
Rate of reactions. (Chapter 2) Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность
Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность Сахарное производство Автор: Чунихина Елена Ивановна, учитель химии.
Сахарное производство Автор: Чунихина Елена Ивановна, учитель химии.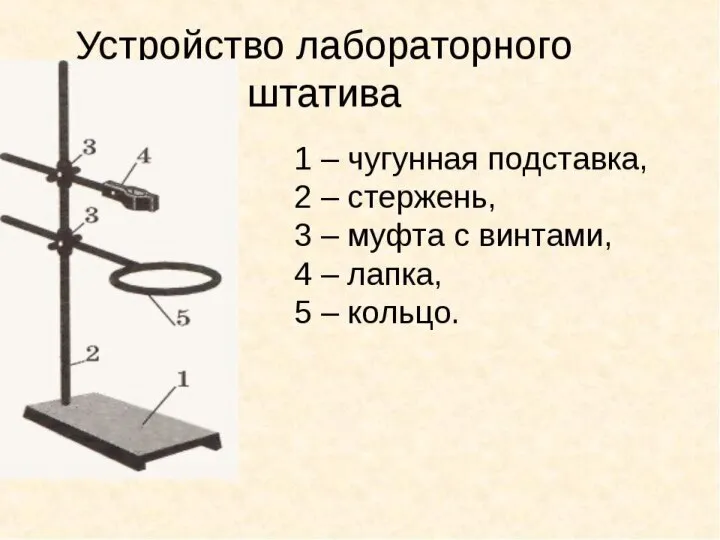 Устройство лабораторного штатива
Устройство лабораторного штатива Д.І.Менделєєв Визначні дати в його житті.
Д.І.Менделєєв Визначні дати в його житті.  Тема 1.4 Закономерности химических процессов. Основы химической термодинамики и биоэнергетики
Тема 1.4 Закономерности химических процессов. Основы химической термодинамики и биоэнергетики Простейшие операции с веществом (химический практикум)
Простейшие операции с веществом (химический практикум) Азотная кислота и ее соли - нитраты
Азотная кислота и ее соли - нитраты Теория химического строения А. М. Бутлерова. Часть II. Раздел 2
Теория химического строения А. М. Бутлерова. Часть II. Раздел 2 Взаимосвязь обмена веществ
Взаимосвязь обмена веществ Химическая связь. Метод молекулярных орбиталей
Химическая связь. Метод молекулярных орбиталей Алкилирование. Понятие
Алкилирование. Понятие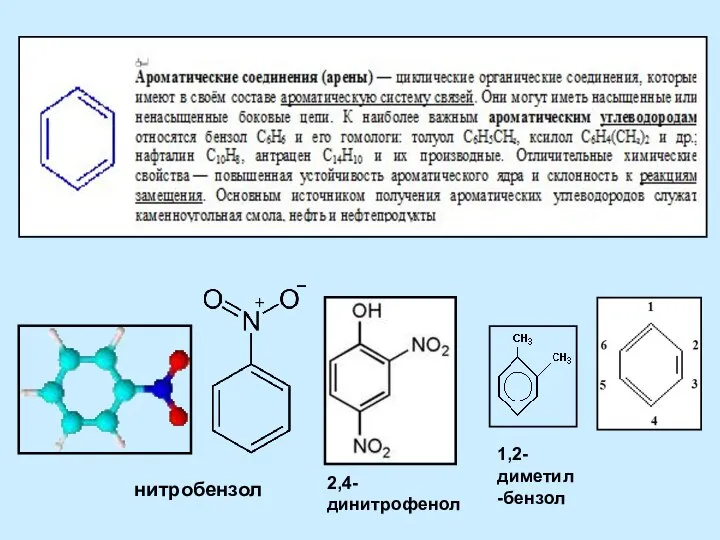 Ароматические соединения (арены)
Ароматические соединения (арены) Кристаллические и аморфные тела
Кристаллические и аморфные тела Физические и химические свойства алкенов. 10 класс
Физические и химические свойства алкенов. 10 класс