Содержание
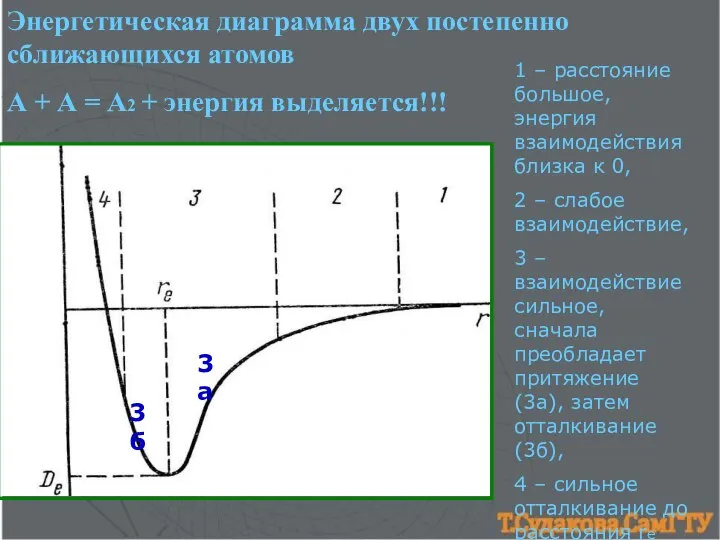
- 2. Энергетическая диаграмма двух постепенно сближающихся атомов А + А = А2 + энергия выделяется!!! 1 –
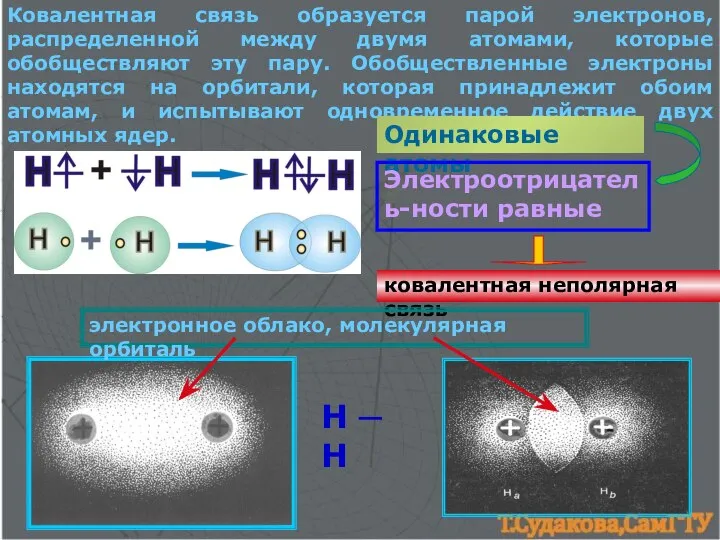
- 3. Ковалентная связь образуется парой электронов, распределенной между двумя атомами, которые обобществляют эту пару. Обобществленные электроны находятся
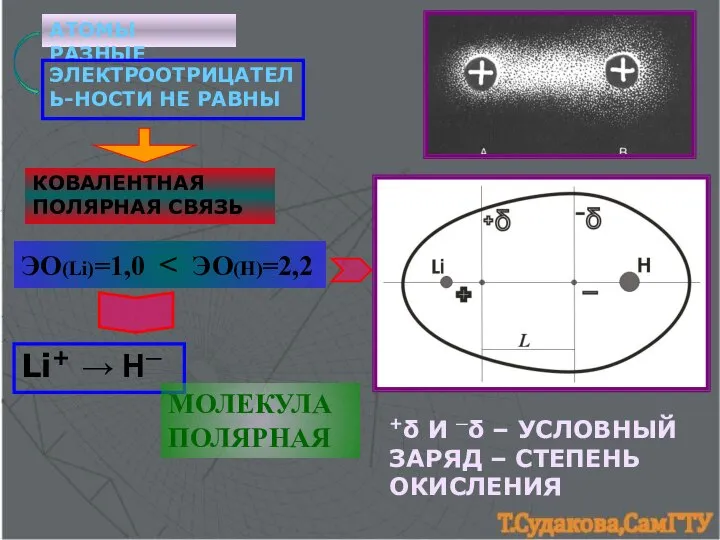
- 4. АТОМЫ РАЗНЫЕ ЭЛЕКТРООТРИЦАТЕЛЬ-НОСТИ НЕ РАВНЫ КОВАЛЕНТНАЯ ПОЛЯРНАЯ СВЯЗЬ +δ И ─δ – УСЛОВНЫЙ ЗАРЯД – СТЕПЕНЬ
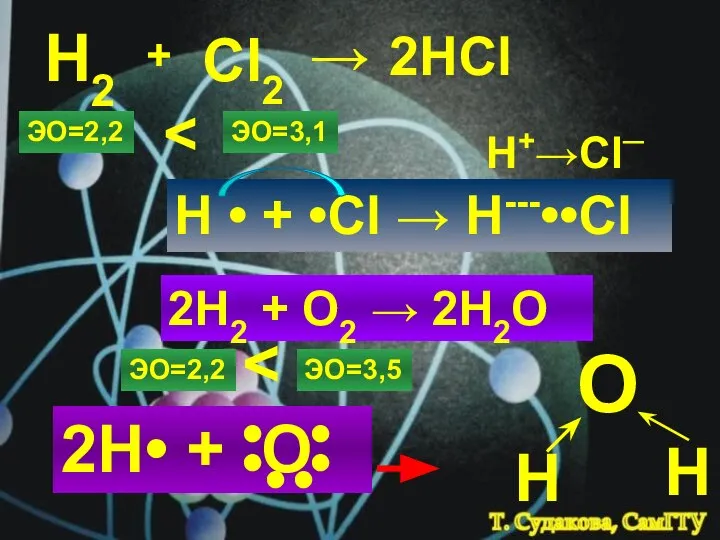
- 5. Н2 + Cl2 → 2HCl ЭО=2,2 ЭО=3,1 H • + •Cl → H---••Cl H+→Cl─ 2H2 +
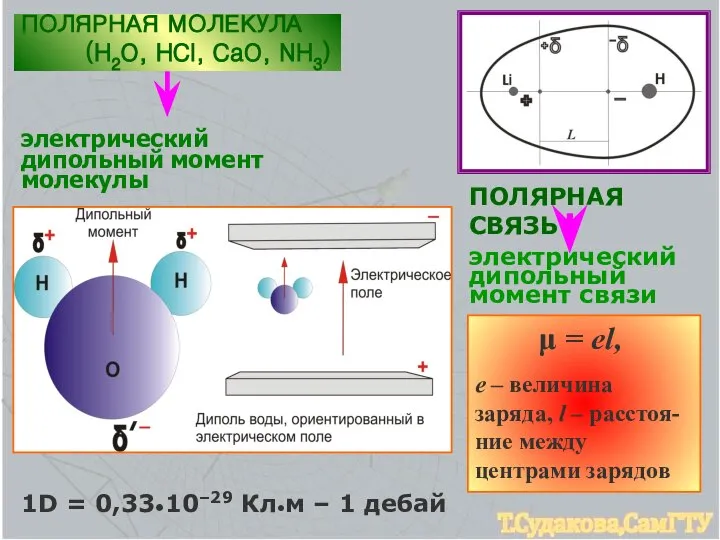
- 6. ПОЛЯРНАЯ СВЯЗЬ электрический дипольный момент связи μ = еl, е – величина заряда, l – расстоя-ние
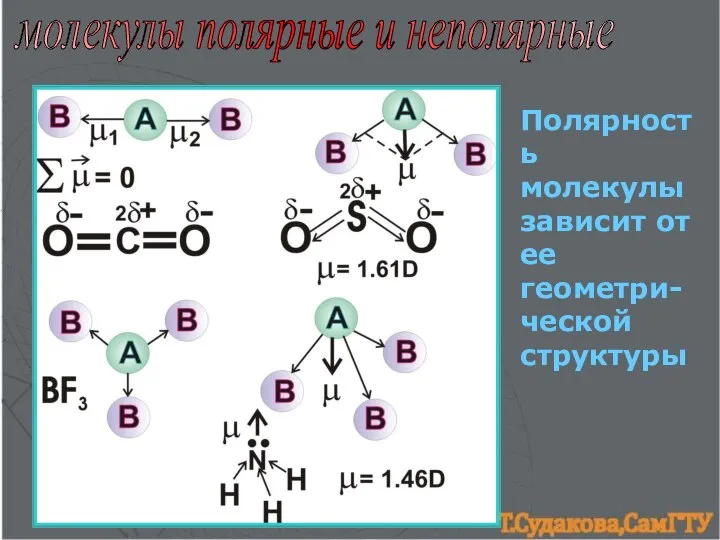
- 7. молекулы полярные и неполярные Полярность молекулы зависит от ее геометри-ческой структуры
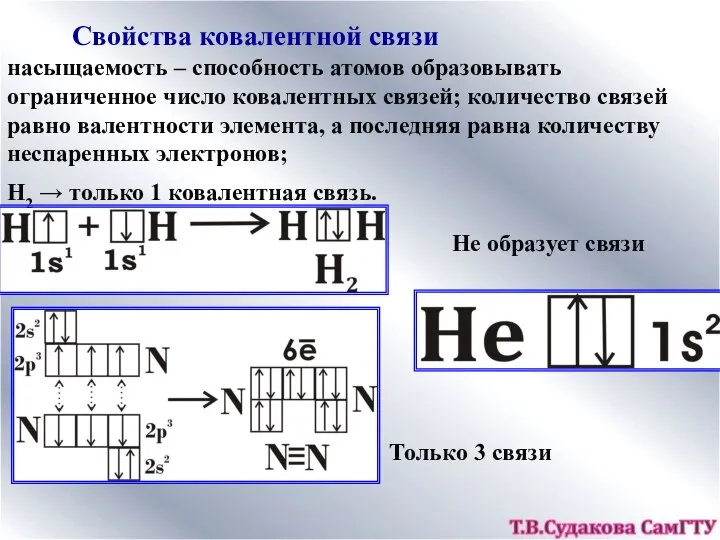
- 8. Свойства ковалентной связи насыщаемость – способность атомов образовывать ограниченное число ковалентных связей; количество связей равно валентности
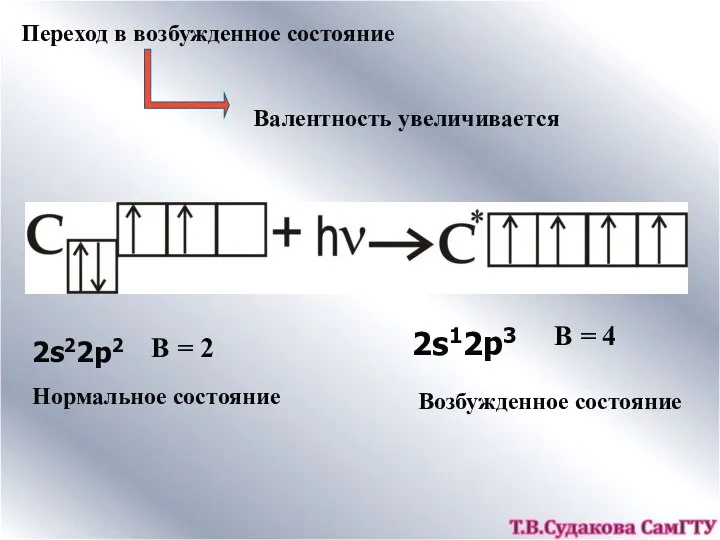
- 9. Переход в возбужденное состояние Валентность увеличивается 2s22p2 Нормальное состояние В = 2 2s12p3 В = 4
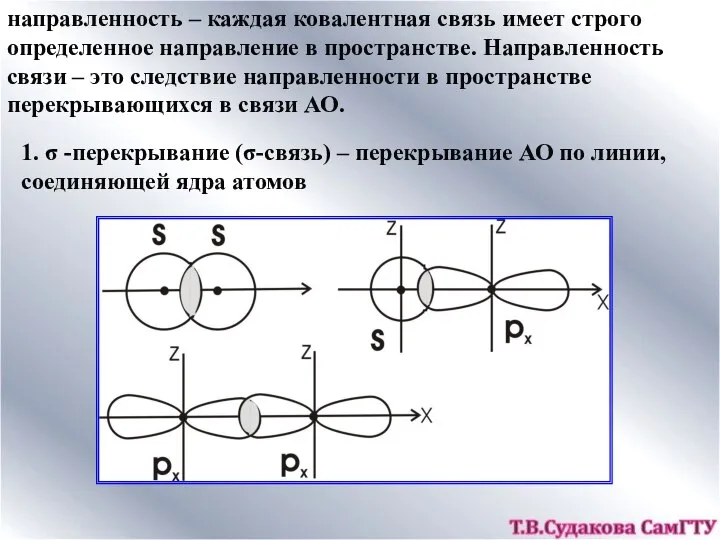
- 10. направленность – каждая ковалентная связь имеет строго определенное направление в пространстве. Направленность связи – это следствие
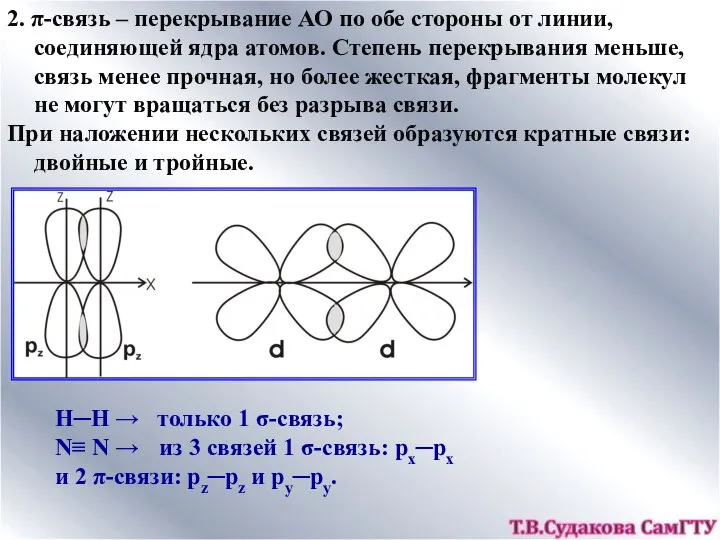
- 11. 2. π-связь – перекрывание АО по обе стороны от линии, соединяющей ядра атомов. Степень перекрывания меньше,
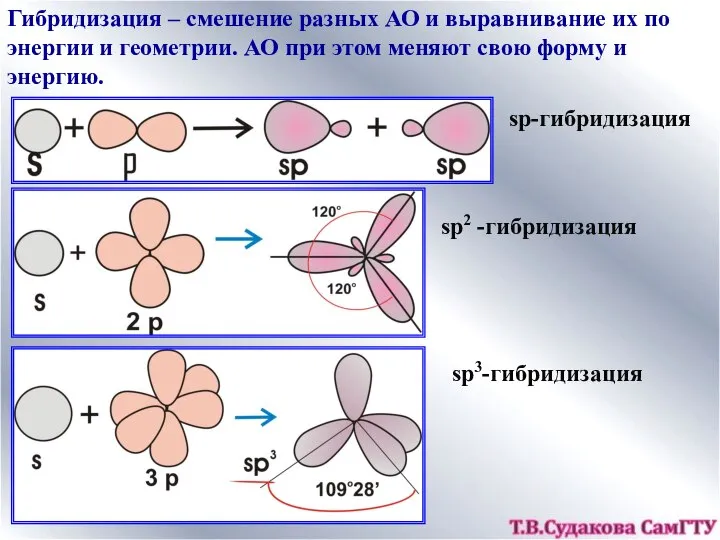
- 12. Гибридизация – смешение разных АО и выравнивание их по энергии и геометрии. АО при этом меняют
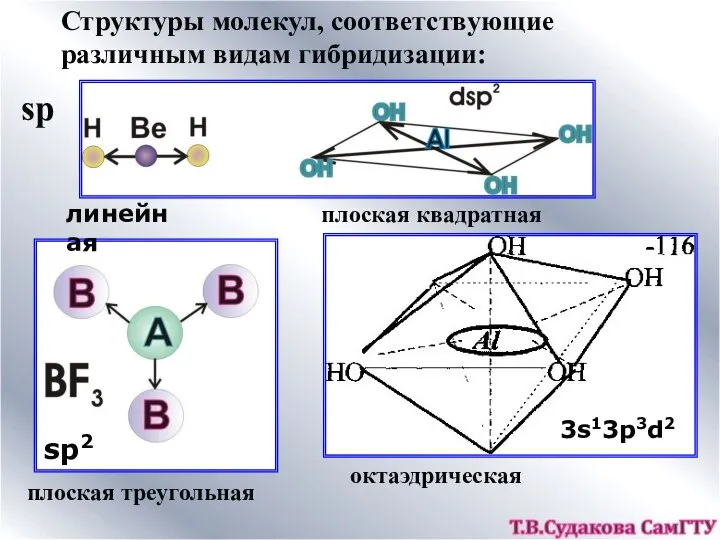
- 13. Структуры молекул, соответствующие различным видам гибридизации: sp sp2 3s13p3d2 линейная плоская квадратная плоская треугольная октаэдрическая
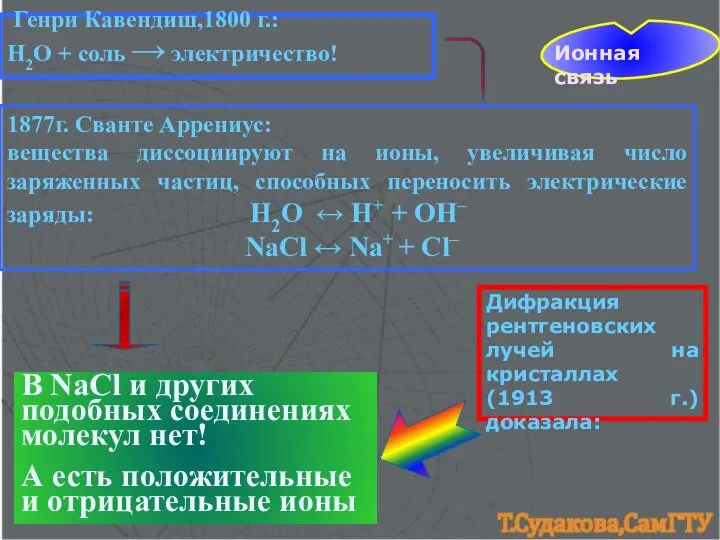
- 14. Ионная связь Генри Кавендиш,1800 г.: Н2О + соль → электричество! 1877г. Сванте Аррениус: вещества диссоциируют на
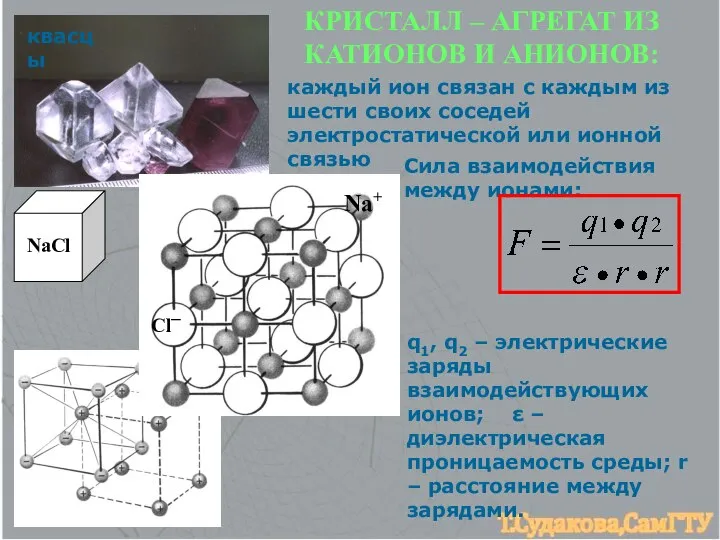
- 15. квасцы NaCl Cl─ Na+ КРИСТАЛЛ – АГРЕГАТ ИЗ КАТИОНОВ И АНИОНОВ: каждый ион связан с каждым
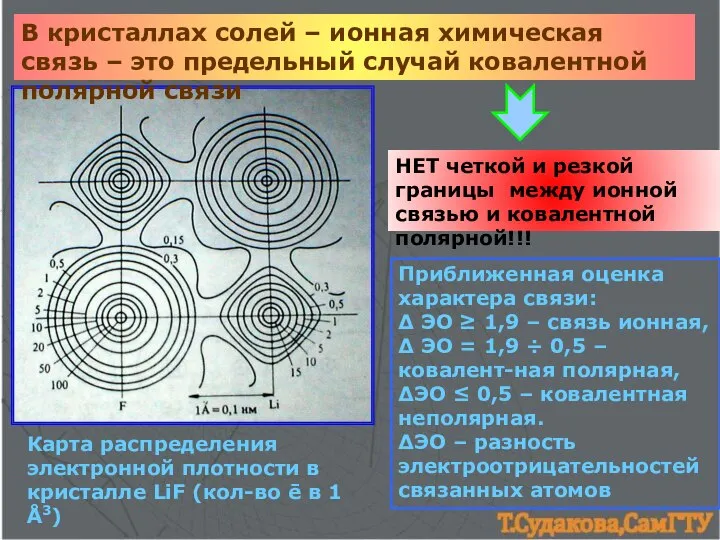
- 16. В кристаллах солей – ионная химическая связь – это предельный случай ковалентной полярной связи НЕТ четкой
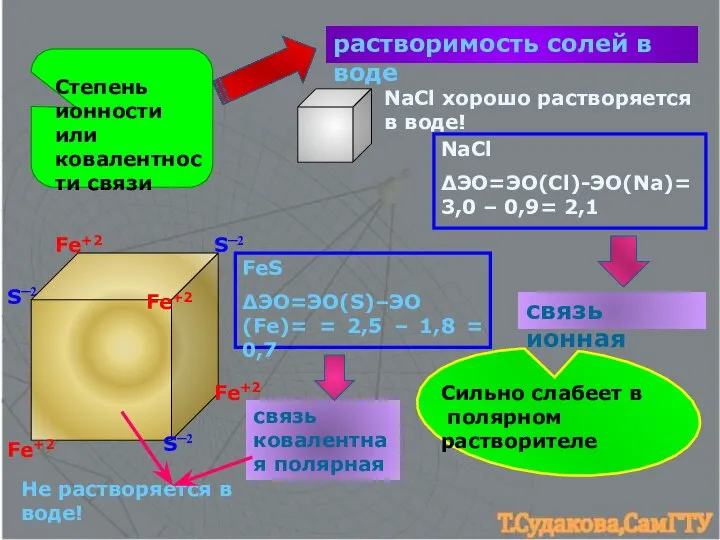
- 17. Степень ионности или ковалентности связи растворимость солей в воде Fe+2 Fe+2 Fe+2 Fe+2 S─2 S─2 S─2
- 18. ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ КОВАЛЕНТНОЙ СВЯЗИ NH3 + H-OH = [NH4]OH вакантная АО неподелен-ная пара ē комплек-сный ион
- 19. комплексные ионы Катионы [NH4]+, [Zn(NH3)4]2+ Анионы [Al(OH)4]─, [CuCl4]2─ структура комплексного иона [Zn+2(NH3)04]2+ [Cu+2Cl─4]2─ ион-комплексообразователь лиганды координаци-онное
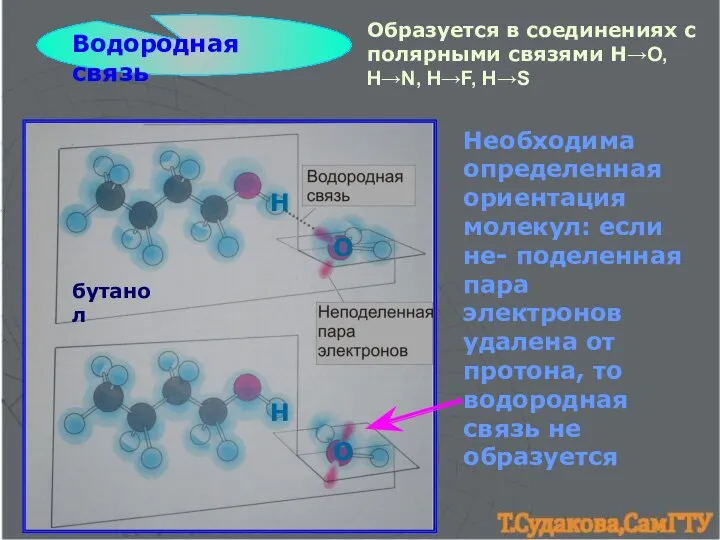
- 20. Водородная связь Образуется в соединениях с полярными связями H→O, H→N, H→F, H→S Н О Н О
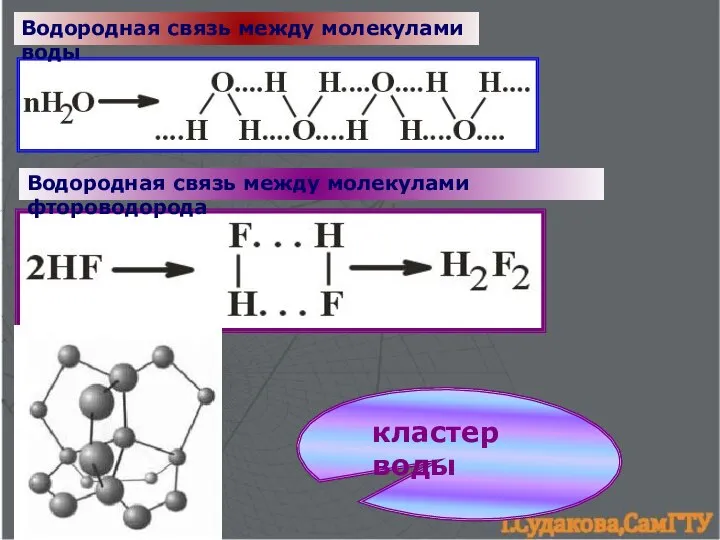
- 21. Водородная связь между молекулами воды Водородная связь между молекулами фтороводорода кластер воды
- 22. -90 -70 плотность теплоемкость Аномальные свойства воды: Плотность льда меньше плот- ности жидкой воды Теплоемкость в
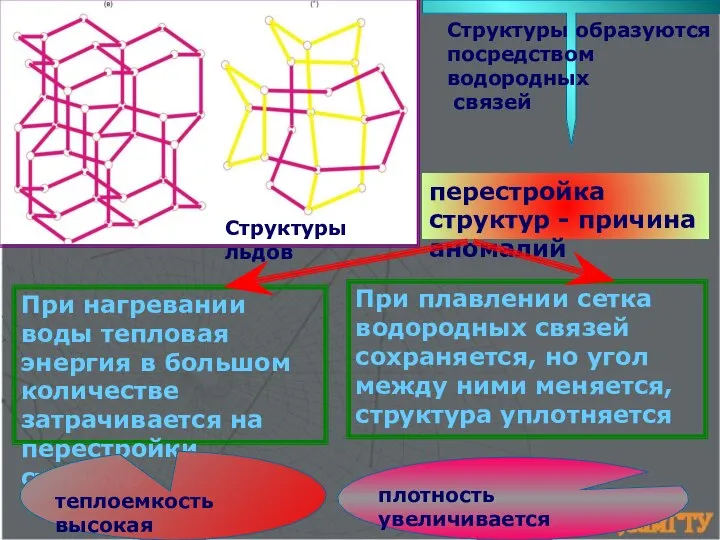
- 23. перестройка структур - причина аномалий Структуры образуются посредством водородных связей Структуры льдов При плавлении сетка водородных
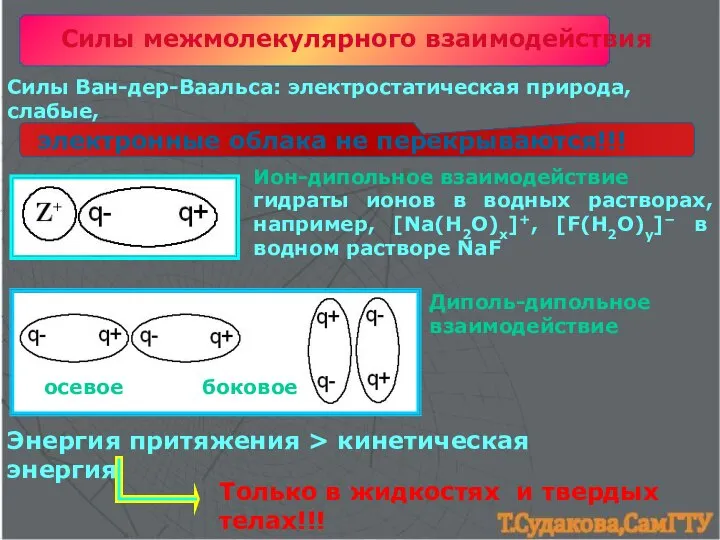
- 24. Силы межмолекулярного взаимодействия Силы Ван-дер-Ваальса: электростатическая природа, слабые, Ион-дипольное взаимодействие гидраты ионов в водных растворах, например,
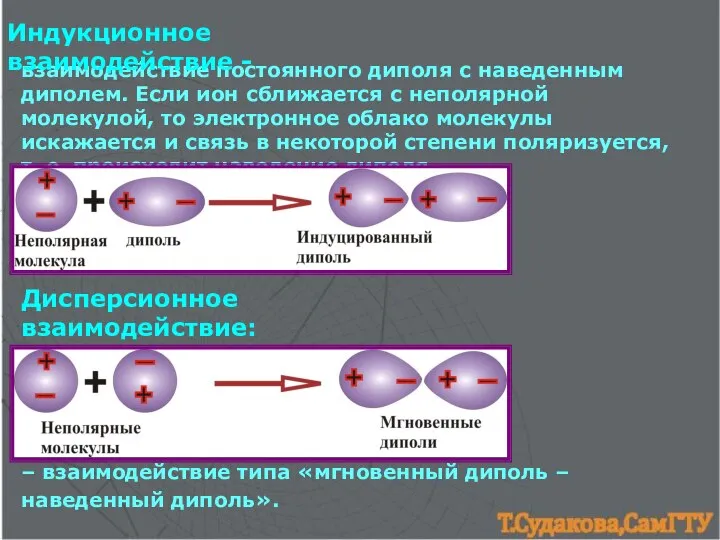
- 25. взаимодействие постоянного диполя с наведенным диполем. Если ион сближается с неполярной молекулой, то электронное облако молекулы
- 26. обусловлено отталкиванием атомных ядер разных молекул (касается только малых по размерам молекул, например, Н2) или, в
- 27. Относительная величина межмолекулярных взаимодействий чем сильнее взаимодействие, тем выше Ткип Вещество Дипольный момент Температура кипения H2
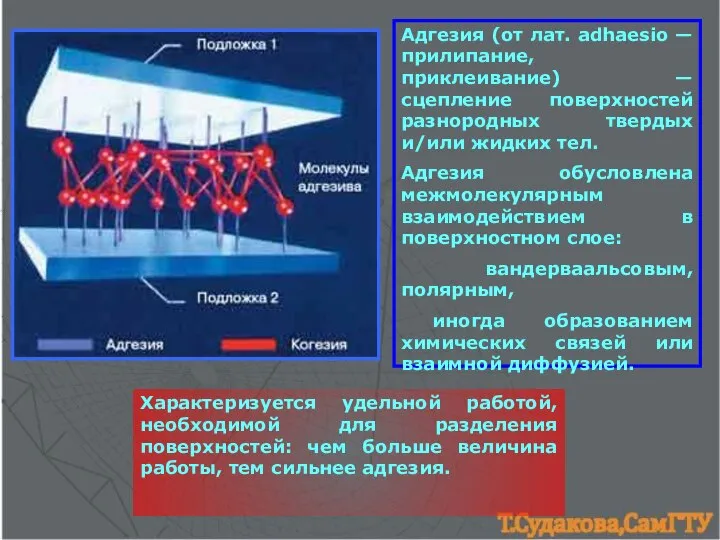
- 28. Адгeзия (от лат. adhaesio — прилипание, приклеивание) — сцепление поверхностей разнородных твердых и/или жидких тел. Адгезия
- 29. Кто это?
- 30. Геккон – безобидная красивая ящерка, обладающая уникальной способностью лазать где угодно и как угодно. Гекконы не
- 32. Скачать презентацию
![ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ КОВАЛЕНТНОЙ СВЯЗИ NH3 + H-OH = [NH4]OH вакантная АО](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397409/slide-17.jpg)
![комплексные ионы Катионы [NH4]+, [Zn(NH3)4]2+ Анионы [Al(OH)4]─, [CuCl4]2─ структура комплексного иона](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397409/slide-18.jpg)





 Валентність
Валентність  Метан и его свойства.
Метан и его свойства. Стандартизація лікарської рослинної сировини
Стандартизація лікарської рослинної сировини Литология. Кремнистые породы
Литология. Кремнистые породы Электролиз расплавов, водных растворов
Электролиз расплавов, водных растворов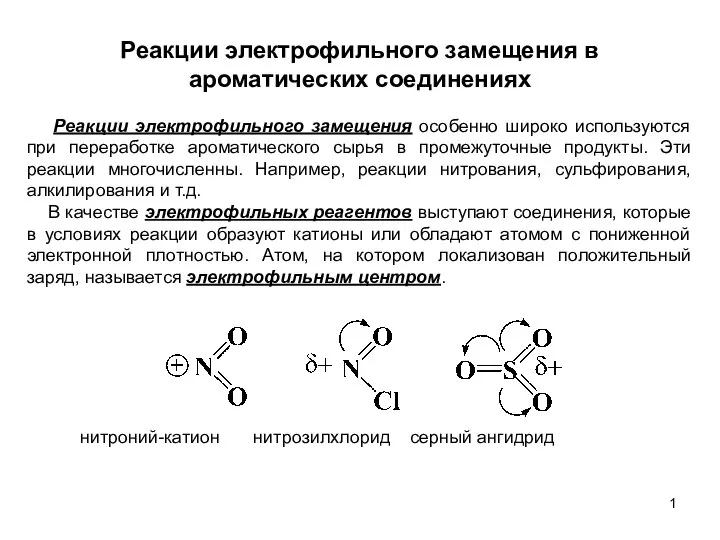 Реакции электрофильного замещения в ароматических соединениях. (Лекция 6)
Реакции электрофильного замещения в ароматических соединениях. (Лекция 6) Лантаноидтар. Лантаноидтардың қасиеттері
Лантаноидтар. Лантаноидтардың қасиеттері Способы получения оксидов, оснований, кислот и солей. Урок №2
Способы получения оксидов, оснований, кислот и солей. Урок №2 Геологические структуры МПИ. Группа доминерализационных структур
Геологические структуры МПИ. Группа доминерализационных структур Презентация по Химии "СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ" - скачать смотреть бесплатно
Презентация по Химии "СИНТЕТИЧНІ ЛІКАРСЬКІ ЗАСОБИ" - скачать смотреть бесплатно Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.
Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.  Физические величины
Физические величины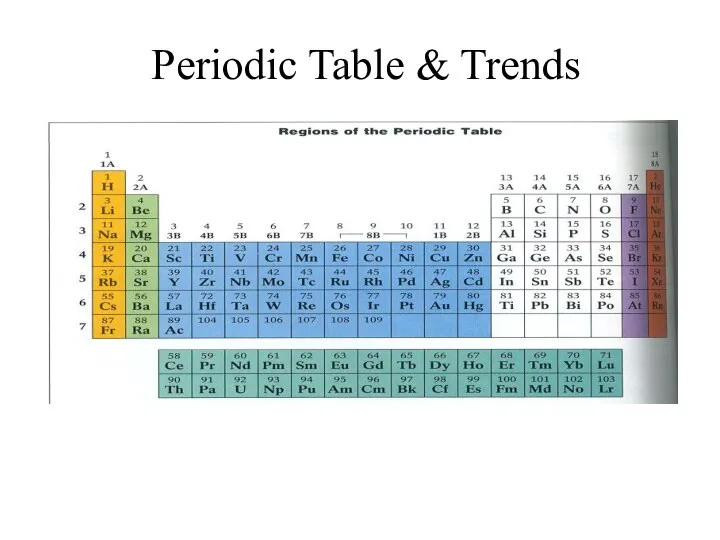 Periodic Table and Trends
Periodic Table and Trends Водород на Земле и в космосе
Водород на Земле и в космосе Образование раствора
Образование раствора Формирование химических знаний при использовании информационных технологий
Формирование химических знаний при использовании информационных технологий Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна
Жиры и масла Выполнила ученица 10 «А» класса Кобылкина Яна  Правила оформления лабораторных работ
Правила оформления лабораторных работ Выбор и назначение антибиотиков в соответствии со свойствами идентифицированного микроорганизма - возбудителя инфекции
Выбор и назначение антибиотиков в соответствии со свойствами идентифицированного микроорганизма - возбудителя инфекции Влияние этанола на организм человека
Влияние этанола на организм человека Аминокислоты алифатического ряда и их производные
Аминокислоты алифатического ряда и их производные Бензол. Физические и химические свойства
Бензол. Физические и химические свойства Свойства веществ различных классов
Свойства веществ различных классов Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы”
Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы” Темір және оның маңызды қосылыстары
Темір және оның маңызды қосылыстары Полимеры в нашей жизни (10 класс)
Полимеры в нашей жизни (10 класс) Комплексные соединения
Комплексные соединения Йод, химия, 9 класс
Йод, химия, 9 класс