Содержание
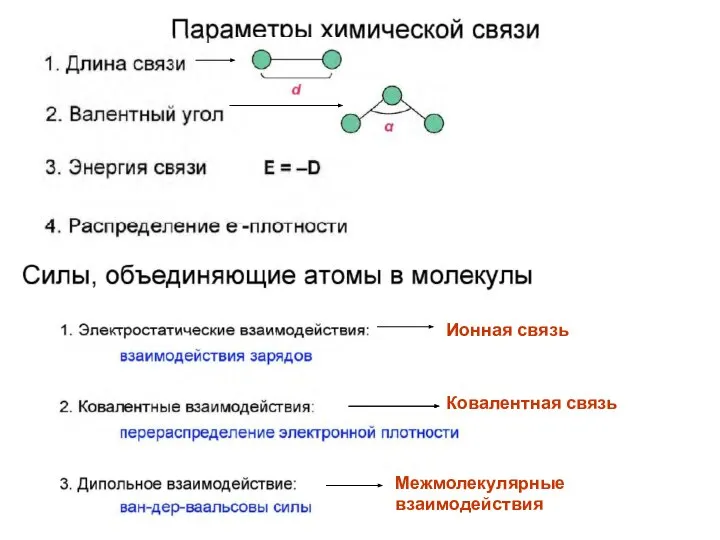
- 4. Ионная связь Ковалентная связь Межмолекулярные взаимодействия
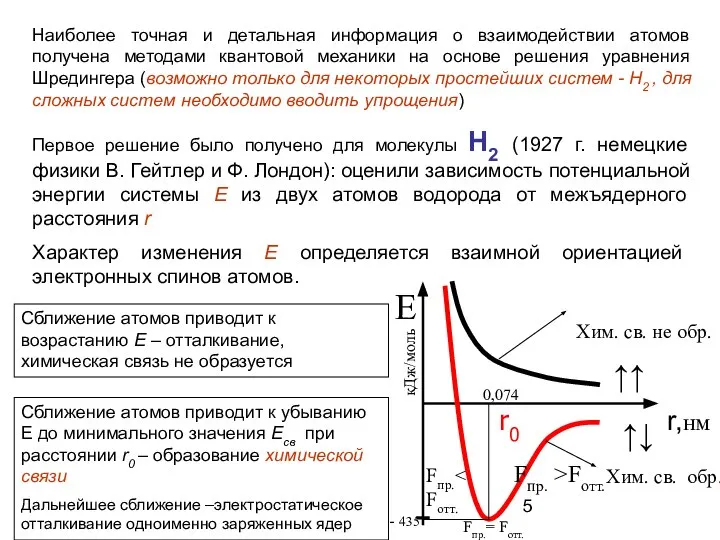
- 5. Наиболее точная и детальная информация о взаимодействии атомов получена методами квантовой механики на основе решения уравнения
- 6. РЕЗУЛЬТАТЫ: Расчетные значения энергии и длины связи оказались близки к экспериментально определенным энергии и межъядерному расстоянию
- 7. КОВАЛЕНТНАЯ СВЯЗЬ -химическая связь, за счет образования общих электронных пар. осуществляется валентными электронами ( не всеми)
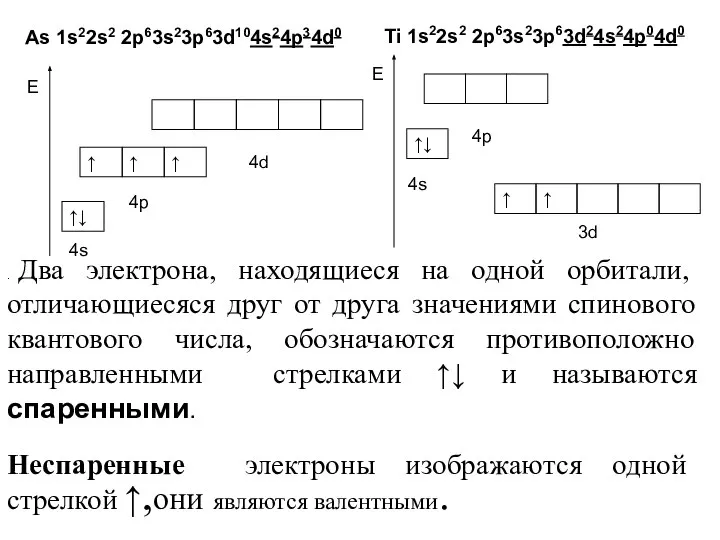
- 8. . Два электрона, находящиеся на одной орбитали, отличающиесяся друг от друга значениями спинового квантового числа, обозначаются
- 9. ОСНОВНОЕ И ВОЗБУЖДЕННОЕ СОСТОЯНИЯ АТОМА Для атома углерода электроны разместятся по уровням и подуровням следующим образом,
- 10. Бериллий в нормальном состоянии нульвалентен. При возбуждении атома бериллия(Ве + 324 кДж/моль → Ве*) происходит разделение
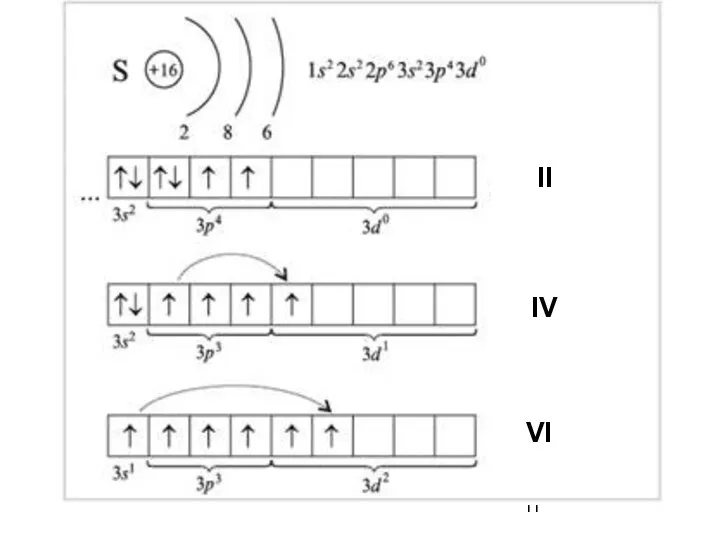
- 11. II IV VI
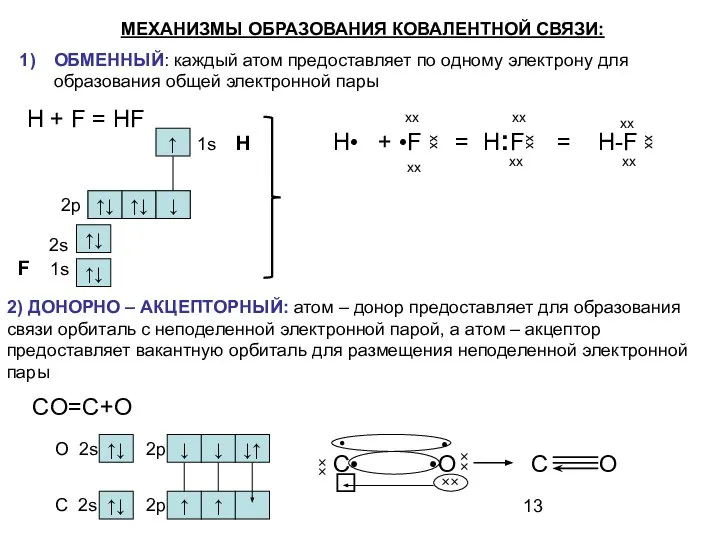
- 12. ПОДХОДЫ К ОПИСАНИЮ ХИМИЧЕСКОЙ СВЯЗИ В МОЛЕКУЛАХ ( с позиций квантово-механической теории) Метод валентных связей (МВС)
- 13. 2) ДОНОРНО – АКЦЕПТОРНЫЙ: атом – донор предоставляет для образования связи орбиталь с неподеленной электронной парой,
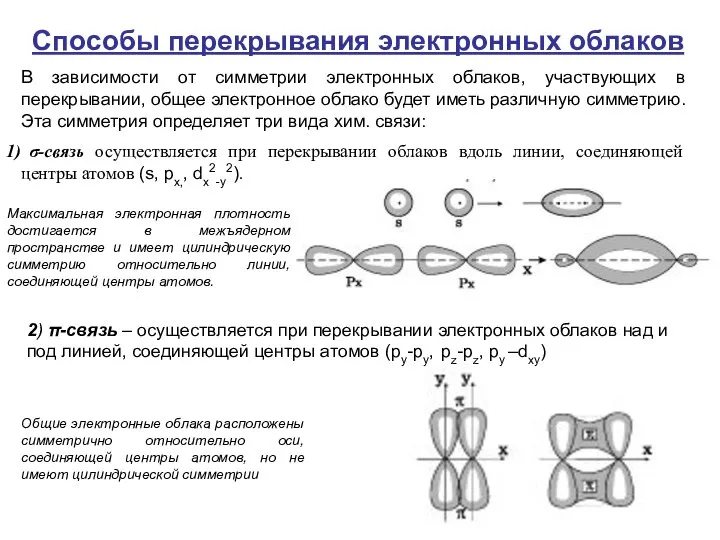
- 14. Способы перекрывания электронных облаков В зависимости от симметрии электронных облаков, участвующих в перекрывании, общее электронное облако
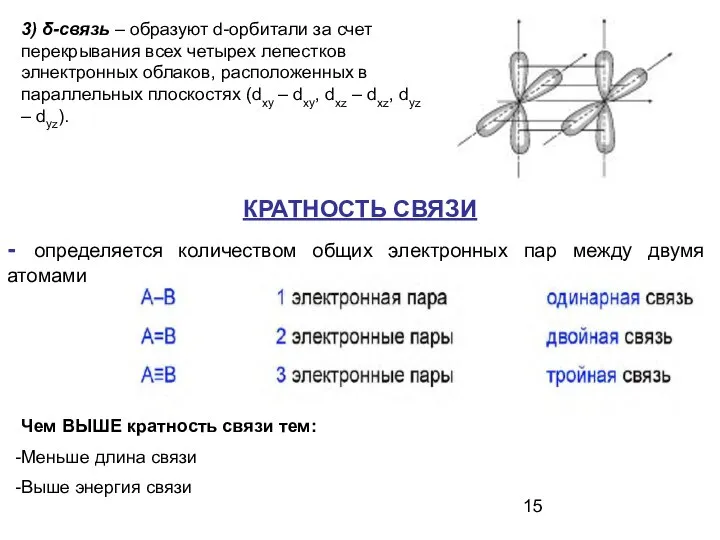
- 15. 3) δ-связь – образуют d-орбитали за счет перекрывания всех четырех лепестков элнектронных облаков, расположенных в параллельных
- 16. НАПРАВЛЕННОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ МОЛЕКУЛ Участие в образовании химической связи атомов в возбужденном состоянии Валентные
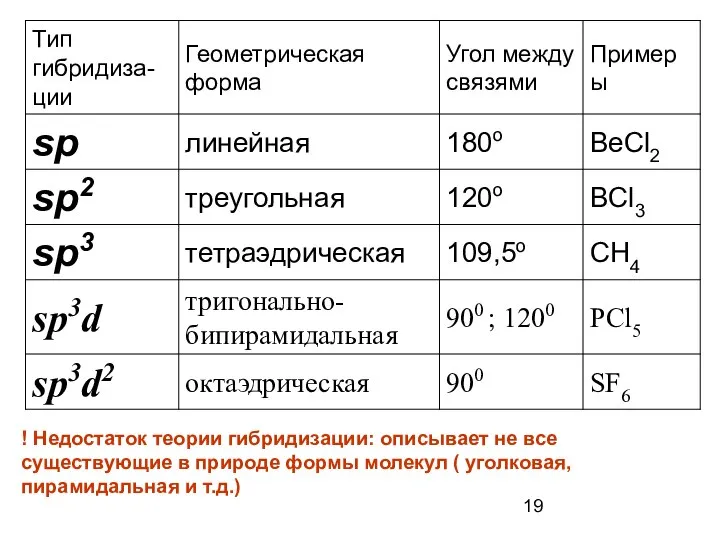
- 19. ! Недостаток теории гибридизации: описывает не все существующие в природе формы молекул ( уголковая, пирамидальная и
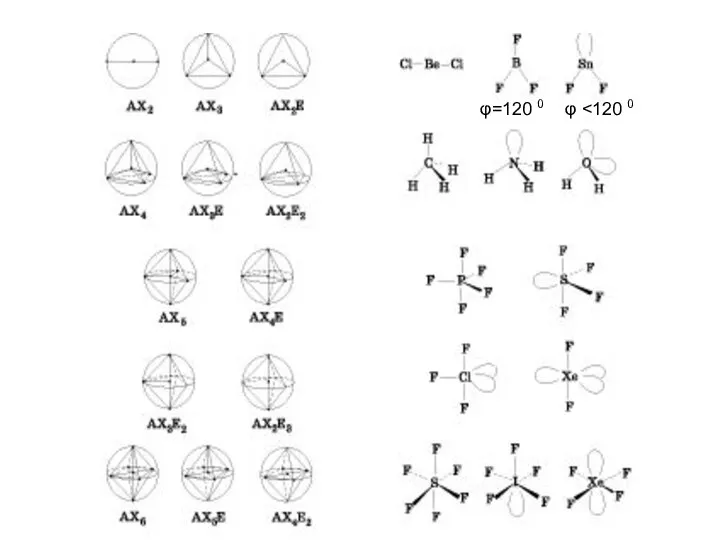
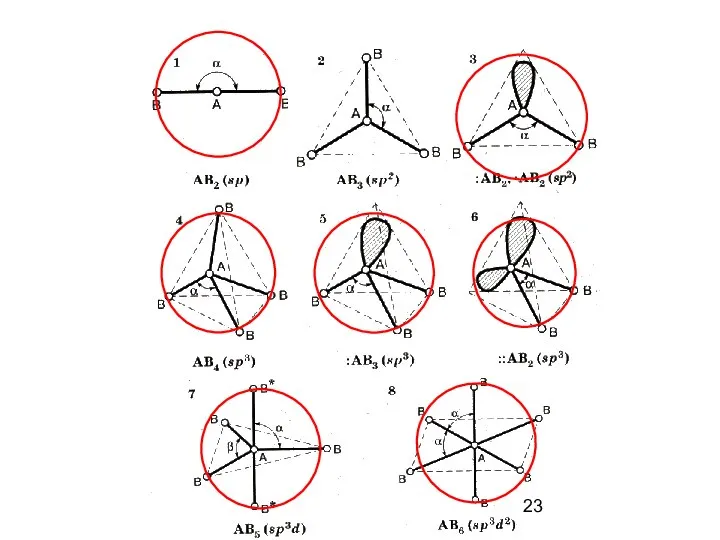
- 20. Метод Гиллеспи ( более общий) Основан на электростатических представлениях Геометрия молекулы или иона определяется числом электронных
- 21. Для описания геометрии молекул используют следующие обозначения: А – многовалентый атом ( центральный) Х – атомы,
- 22. φ=120 0 φ
- 24. ↓ϕ связано с ↑ числа несвязывающих гибр. орбиталей тетраэдрическая пирамидальная угловая СН4 NН3 Н2O ВЛИЯНИЕ НЕПОДЕЛЕННОЙ
- 27. 1. При образовании молекулы по ММО изменяют своё состояние не только валентные электроны, а все электроны
- 28. 3.Для получения МО используют метод линейной комбинации атомных орбиталей МЛКАО. Из двух АО разных атомов образуется
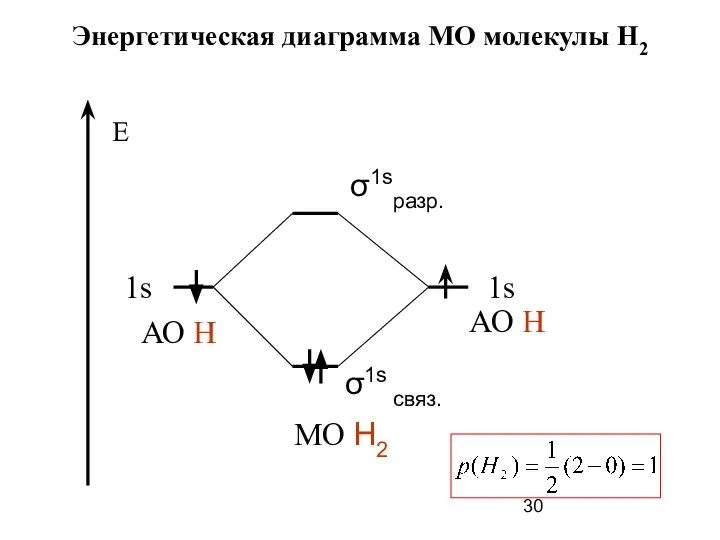
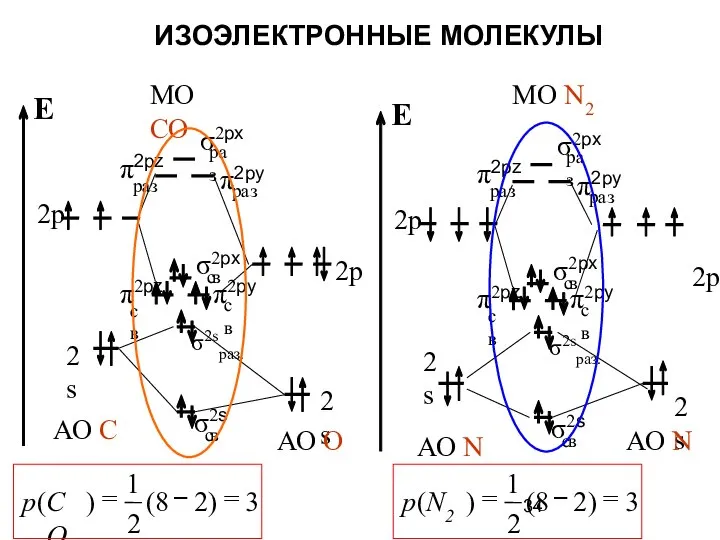
- 29. 6. Химическая связь в ММО характеризуется энергией связи и кратностью. Кратность связи (р) определяется по формуле:
- 30. Энергетическая диаграмма МО молекулы Н2
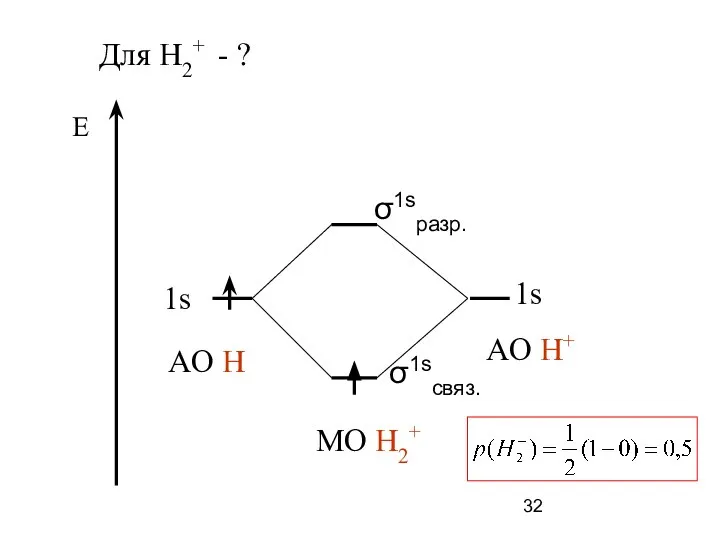
- 31. Для Н2- - ?
- 32. Е AO Н 1s 1s σ1sсвяз. МО H2+ σ1sразр. Для Н2+ - ? AO Н+
- 36. Наличие спаренных или неспаренных электронов в атомах, молекулах и кристаллах устанавливается экспериментально путем изучения магнитных свойств
- 37. Сравнительная характеристика методов: ВС и МО ВС достоинства: нагляден; описывает геометрию молекул недостатки: ∙не рассматривает вклад
- 38. МО достоинства: ∙общий подход при описании всех хим. соед.; !Выбор метода определяется объектом исследования и поставленной
- 39. 1. Энергия связи 2. Длина связи 3. Кратность связи 4. Насыщаемость 5. Направленность 6. Полярность 7.
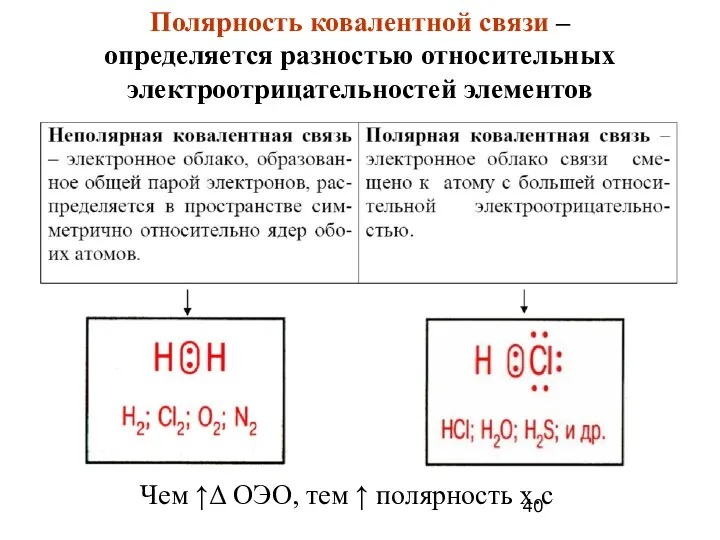
- 40. Чем ↑Δ ОЭО, тем ↑ полярность х.с Полярность ковалентной связи – определяется разностью относительных электроотрицательностей элементов
- 42. Дипольный момент связи (μ) l - Длина связи q- Эффективный заряд Векторная величина
- 43. Неполярные молекулы Молекула неполярна, если суммарный μ всех связей = 0.
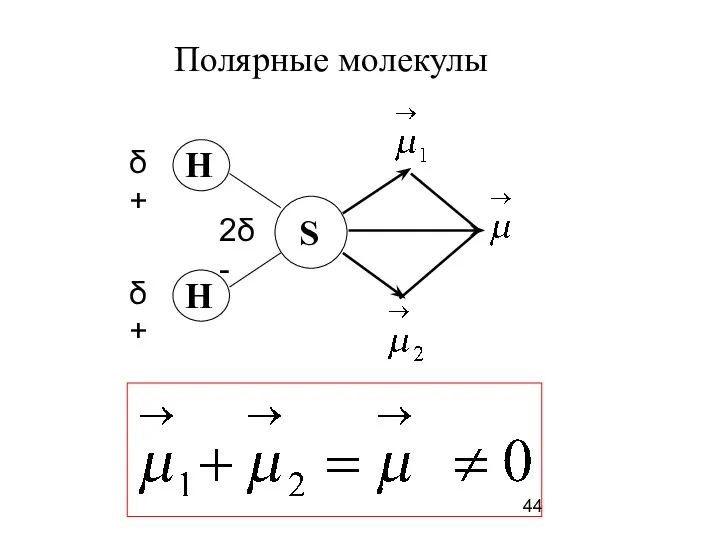
- 44. Полярные молекулы
- 46. Дипольный момент молекулы зависит: ∙от полярности связей; ∙от геометрии молекулы; ∙от наличия неподелённых пар электронов.
- 48. т.е. степень ионности равна 83%. Полного перетягивания связующих пар электронов от более электроположительного к более электроотрицательному
- 50. ВОДОРОДНАЯ СВЯЗЬ связь между атомом водорода, соединенным с атомом сильноэлектроотрицательного элемента одной молекулы и сильно электроотрицательными
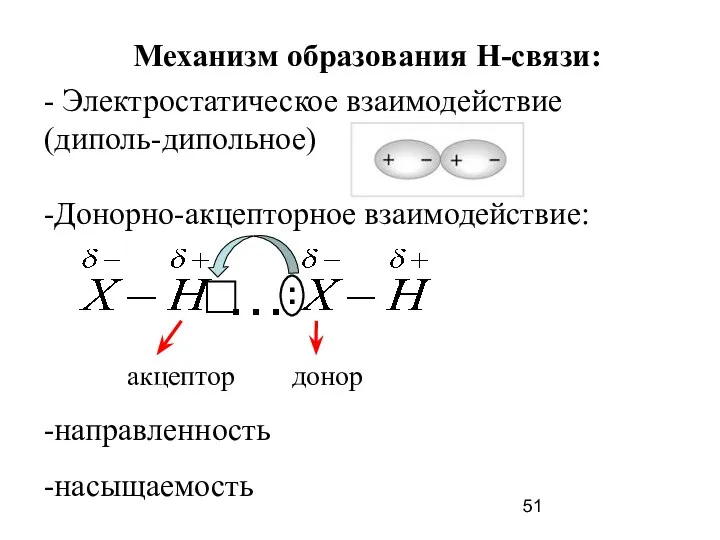
- 51. Механизм образования Н-связи: - Электростатическое взаимодействие (диполь-дипольное) -Донорно-акцепторное взаимодействие: -направленность -насыщаемость
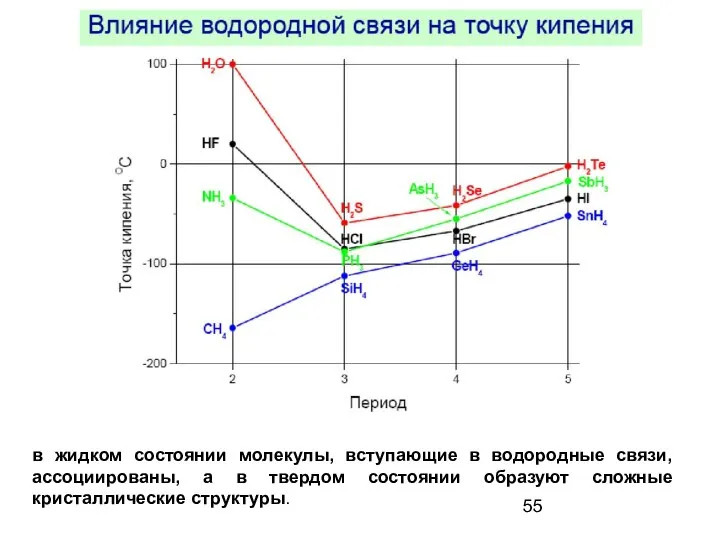
- 55. в жидком состоянии молекулы, вступающие в водородные связи, ассоциированы, а в твердом состоянии образуют сложные кристаллические
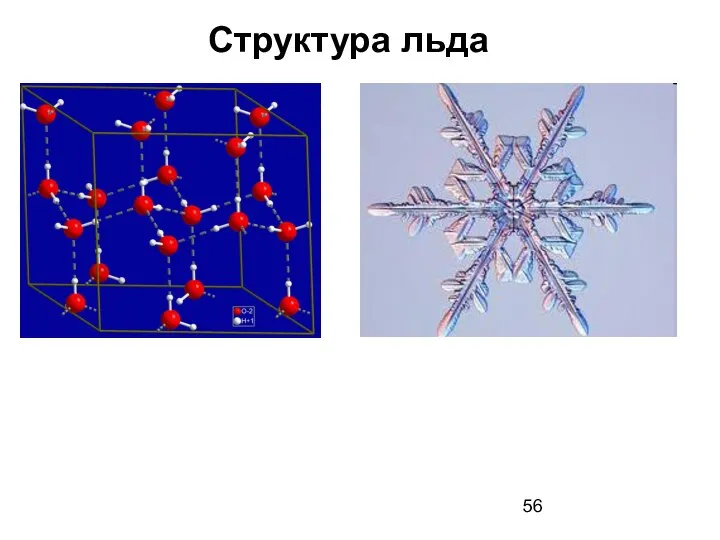
- 56. Структура льда
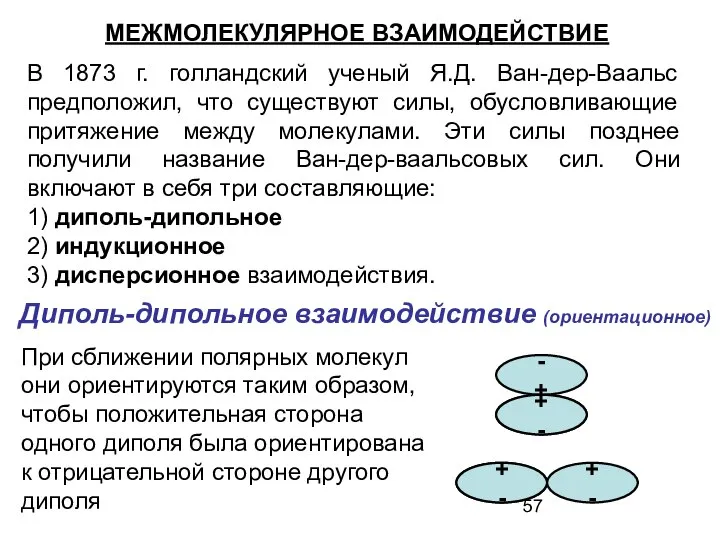
- 57. В 1873 г. голландский ученый Я.Д. Ван-дер-Ваальс предположил, что существуют силы, обусловливающие притяжение между молекулами. Эти
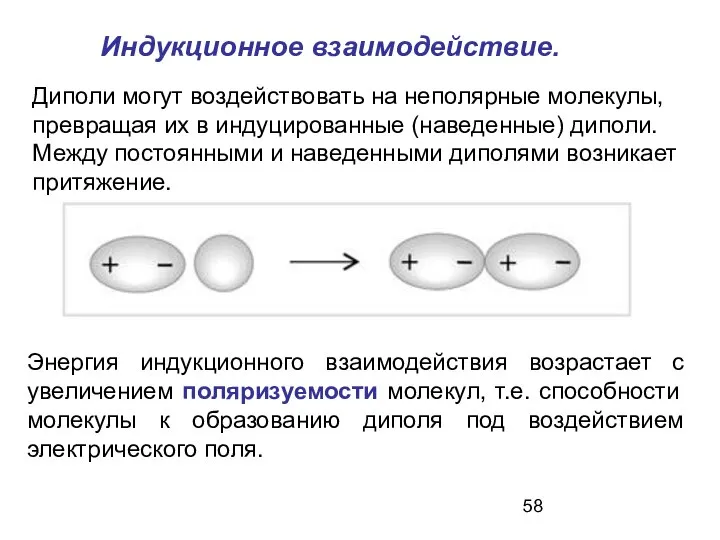
- 58. Индукционное взаимодействие. Диполи могут воздействовать на неполярные молекулы, превращая их в индуцированные (наведенные) диполи. Между постоянными
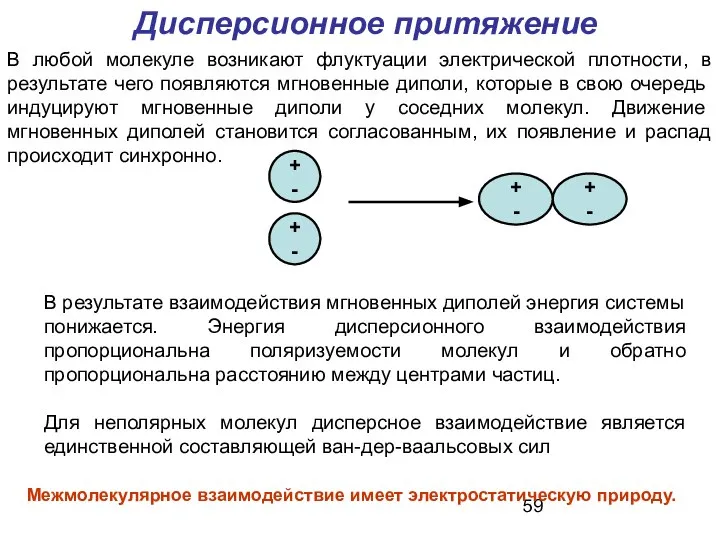
- 59. В любой молекуле возникают флуктуации электрической плотности, в результате чего появляются мгновенные диполи, которые в свою
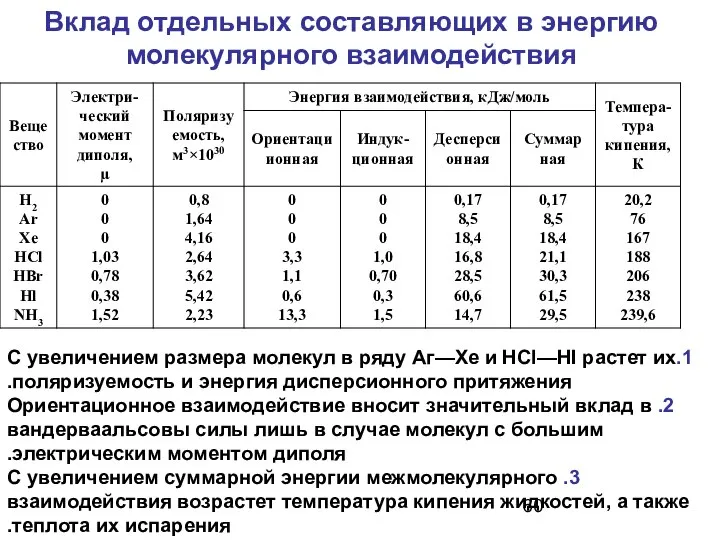
- 60. Вклад отдельных составляющих в энергию молекулярного взаимодействия 1.С увеличением размера молекул в ряду Аг—Хе и НСl—HI
- 61. ЭНЕРГИЯ СВЯЗИ
- 62. Группа ученых «Гекко» возглавляют физиолог К.Отан из колледжа Льюиса и Кларка в г. Портленд (США) и
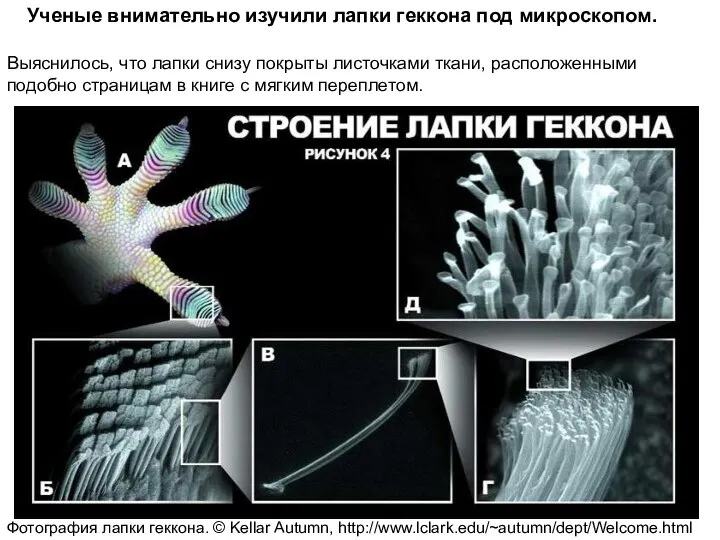
- 63. Выяснилось, что лапки снизу покрыты листочками ткани, расположенными подобно страницам в книге с мягким переплетом. Ученые
- 64. При большом увеличении видно, что каждый листочек покрыт сотнями тысяч тонких волосообразных щетинок. А щетинки, в
- 66. НАНОКЛАСТЕРЫ ЗОЛОТА (КОЛЛОИДНЫЙ РАСТВОР) Увеличение размера наночастиц
- 70. Скачать презентацию












































 Двойной электрический слой (ДЭС)
Двойной электрический слой (ДЭС) Эколого-химическая характеристика качества почвы
Эколого-химическая характеристика качества почвы Основания, их классификация и свойства (8 класс)
Основания, их классификация и свойства (8 класс) Поверхневі явища. Адсорбція
Поверхневі явища. Адсорбція Пируватдегидрогеназный комплекс
Пируватдегидрогеназный комплекс Техника безопасности при работе с серной кислотой
Техника безопасности при работе с серной кислотой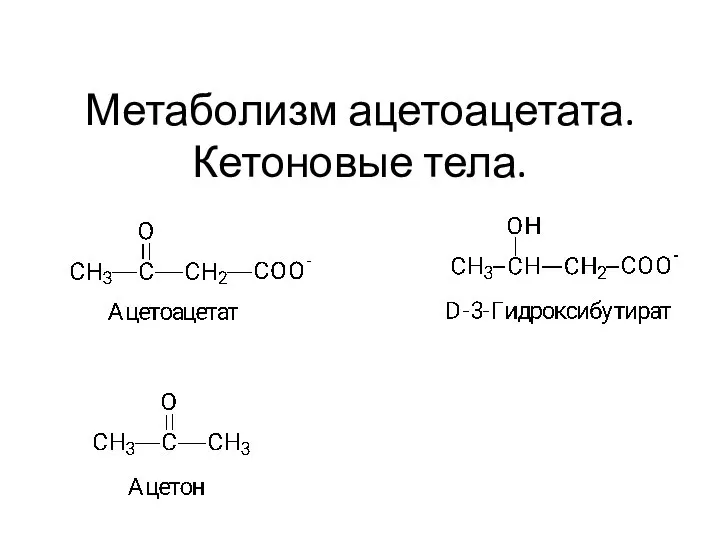 Метаболизм ацетоацетата. Кетоновые тела.Тема 10
Метаболизм ацетоацетата. Кетоновые тела.Тема 10 Гідроліз солей
Гідроліз солей Коррозия металлов
Коррозия металлов Алкены. Непредельные углеводороды ряда этилена
Алкены. Непредельные углеводороды ряда этилена Простой борный суперфосфат
Простой борный суперфосфат Природные смолы: канифоль, янтарь, сандарак (2)
Природные смолы: канифоль, янтарь, сандарак (2) Закономерности управления простым обратимым гомогенным процессом
Закономерности управления простым обратимым гомогенным процессом Проблема содержания нитратов в пищевых продуктах
Проблема содержания нитратов в пищевых продуктах Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Өсімдіктердегі су алмасу физиологиясы. Судың өсiмдiк тiршiлiгiндеri маңызы
Өсімдіктердегі су алмасу физиологиясы. Судың өсiмдiк тiршiлiгiндеri маңызы Липиды. Насыщенные и ненасыщенные жирные кислоты
Липиды. Насыщенные и ненасыщенные жирные кислоты ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии
ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии Гранулометрический метод контроля
Гранулометрический метод контроля Colligative properties of solutions
Colligative properties of solutions Общая геохимия
Общая геохимия Презентация по химии Электролиз
Презентация по химии Электролиз  Химическое сопротивление алюминий и его сплавов
Химическое сопротивление алюминий и его сплавов Атом құрылысы
Атом құрылысы Учебно - исследовательский проект «Выращивание кристаллов в домашних условиях»
Учебно - исследовательский проект «Выращивание кристаллов в домашних условиях» Презентация по Химии "Химия – наука о веществах" - скачать смотреть
Презентация по Химии "Химия – наука о веществах" - скачать смотреть  Азот и фосфор
Азот и фосфор Механизмы рекомбинации
Механизмы рекомбинации